2022年中考化学真题汇编:计算题(word版 有答案)
A、甲醇的极性比水强,所以甲醇的洗脱能力比水强
B、甲醇的极性比水弱,所以甲醇的洗脱能力比水强
C、甲醇的极性比水强,所以甲醇的洗脱能力比水弱
D、甲醇的极性比水弱,所以甲醇的洗脱能力比水弱
A、0.30
B、0.43
C、0.19
D、0.55
N(NO2)3是科学家2011年发现的一种新型火箭燃料。试计算:
(1)N(NO2)3的相对分子质量;
(2)N(NO2)3中氮元素和氧元素的质量比;
(3) N(NO2)3中氮元素的质量分数。
工业酒精中常含有甲醇(CH3OH),误食后会使人眼睛失明,甚至死亡。下列有关甲醇的说法中不正确的是
A.甲醇由碳、氢、氧三种元素组成 B.甲醇中碳、氢、氧三种元素的质量比为3:1:4
C.甲醇由甲醇分子构成 D.一个甲醇分子中共有5个原子
的题目.
(1)求元素的物质的量之比即原子个数比——求最简式
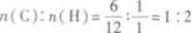
此有机物分子中碳原子与氢原子的个数比为I:2,即CH2(习惯叫做最简式).
(2)求有机物的相对分子质量M
M=21×2=42
(3)求分子式
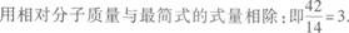
所以分子式为C3H6.
(g)求结构简式
题目告知此有机物是链烃,所以只能是烯烃——丙烯,其结构简式为CH3-CH=CH2.
2022年中考化学真题汇编:计算题1.(2022天津)甲醇(CH3OH)是一种燃料。计算:(1)甲醇的相对分子质量为_;(2)甲醇中碳、氢元素的质量比为_(填最简比);(3)甲醇中氧元素的质量分数为_。2.(2022铁岭葫芦岛)疫情防控期间,常用到一种免洗手消毒凝胶,其成分中含有正丙醇(化学式为C3H8O)。请计算:(1)正丙醇中碳、氢、氧元素的质量比为_(填最简整数比)。(2)正丙醇中碳元素的质量分数为_。3.(2022铁岭葫芦岛)硫酸亚铁在工农业生产中有重要用途,也有较高医用价值。在实验室里,模拟工业上制取硫酸亚铁的原理,向5.6g铁屑中加入100g稀硫酸,二者恰好完全反应。请计算:(1)生成硫酸亚铁的质量为_g。(2)所用稀硫酸中溶质的质量分数。4.(2022新疆)一定浓度的次氯酸钠(NaClO)溶液能有效杀灭“新冠”病毒。利用次氯酸钠发生器,通过电解食盐水能够制得次氯酸钠溶液,该反应方程式为:。要制取7.45gNaClO,理论上需要NaCl的质量是_?5.(2022昆明)ZnO用于制作油漆、药物等。将一定量的ZnO加入到100gNaOH溶液中,恰好完全反应,反应后溶液质量为108.1g。计算:(1)ZnO的质量为_g。(2)NaOH溶液中溶质的质量分数是多少?(化学方程式:)6.(2022梧州)实验室用质量分数为20.0%的稀硫酸处理含Ba(OH)2的废液。向100.0g废液中加入稀硫酸至溶液恰好呈中性,最终得到2.33 g沉淀。请计算:(1)配制490.0 g 20.0%的稀硫酸需质量分数为98.0%的浓硫酸_g。(2)废液中Ba(OH)2的质量分数。7.(2022云南)学习小组用已知浓度的氢氧化钠溶液测定某硫酸溶液的浓度。取该硫酸溶液20g,滴加10%的氢氧化钠溶液,恰好完全反应时,共消耗氢氧化钠溶液40g。计算。(1)消耗的NaOH溶液中溶质的质量为_g:(2)该硫酸溶液的溶质质量分数_。(温馨提示:)8.(2022邵阳)取一定量NaCl和NaHCO3组成的固体样品放入烧杯中,然后将一定溶质质量分数的盐酸逐滴加入样品中,边加边搅拌,测得生成气体的质量与所加盐酸的质量关系如下图所示。请分析并计算:(1)恰好完全反应时产生气体的质量是_g;(2)a点时溶液中含有的溶质是_(填化学式);(3)计算所加盐酸的溶质质量分数_。(写出计算过程,结果精确到0.01%)9.(2022桂林)我国明代科技著作天工开物中有利用炉甘石(主要成分是ZnCO3)火法炼锌的工艺记载,主要反应原理为ZnCO3+2CZn+3CO,现用200 kg炉甘石与足量碳充分反应,产生CO的质量与加热时间的关系如图所示。(1)此过程中产生CO的质量是_kg。(2)列式计算此炉甘石中ZnCO3的质量分数。10.(2022遂宁)化学兴趣小组整理药品时,发现一瓶标签受损的稀盐酸。为测定该稀盐酸的溶质质量分数,同学们进行了下图的实验(所选石灰石中的杂质不溶于水,也不与其他物质反应;生成气体全部逸出)。请完成下列问题:(1)生成二氧化碳的质量为_g:(2)计算稀盐酸的溶质质量分数_(写出计算过程)。11.(2022荆州)硫酸铜对过氧化氢(H2O2)的分解有催化作用。取8.5%的过氧化氢溶液40g倒入锥形瓶中,向其中加入15%的硫酸铜溶液6.6g,使过氧化氢完全分解,若产生的气体全部逸出,请计算:(1)过氧化氢的相对分子质量为 _。(2)产生氧气的质量(写出计算过程)。(3)反应后所得硫酸铜溶液中溶质的质量分数为 _。12.(2022天津)现有Na2SO4和CuSO4的混合物,化学兴趣小组的同学欲除去Na2SO4固体中混有的CuSO4,得到Na2SO4溶液。可供选择的试剂有:NaOH溶液、KOH溶液、BaCl2溶液。该小组的同学称取固体样品20g,向其中加入135.9g水全部溶解,再加入40g所选试剂,恰好完全反应,得到Na2SO4溶液和4.9g沉淀。回答并计算:(1)该同学选择的试剂为_溶液;(2)所选试剂中溶质的质量;(3)反应后所得溶液中溶质的质量分数。13.(2022重庆B卷)硫氧粉(Na2SO3)可用作染漂脱氧剂,常因氧化变质生成Na2SO4。向20g可能被氧化的样品中,加入质量分数为10%的稀硫酸至恰好不再产生气泡(假设气体全部逸出)。消耗稀硫酸98g。已知:Na2SO3+H2SO4=Na2SO4+SO2+H2O(1)根据化学式判断Na2SO4和Na2SO3中钠元素的质量分数较小的是_。(2)若用5g质量分数为98%的浓硫酸配制10%的稀硫酸,求所需水的质量。(3)求反应后溶液中溶质的质量分数。(精确到小数点后一位)14.(2022天津)金属及金属材料在生产、生活中应用广泛。(1)铝具有很好的抗腐蚀性,是因为其表面生成一层致密的薄膜,该薄膜是_(填化学式)。(2)向一定质量的氧化铜中加入一定量稀硫酸使其完全溶解,得到蓝色溶液。再加入铁粉充分反应,过滤,得到滤渣和滤液。向滤渣中加入稀硫酸,有气泡冒出,则滤液中的溶质是_(填化学式)。(3)早在春秋战国时期,我国就开始生产和使用铁器。炼铁原理是利用一氧化碳与氧化铁在高温条件下反应,该反应的化学方程式为_。现将某铁合金(只含铁和碳)8.7 g 放入盛有 100 g 稀盐酸的烧杯中,恰好完全反应,得到 108.1 g 溶液,则该样品中碳的质量分数为_(结果精确到 0.1%)。该铁合金属于_(填“钢”或“生铁”)。15.(2022重庆A卷)化学泡沫灭火器是常用灭火器之一,其反应原理为:Al2(SO4)3+6NaHCO3=3Na2SO4+2Al(OH)3+6CO2。现将34.2 kg质量分数为10%的Al2(SO4)3溶液与270 kg NaHCO3溶液混合,恰好完全反应(假设生成的气体全部逸出)。已知相对分子质量:Al2(SO4)3 342;Na2SO4 142;Al(OH)3 78试计算:(1)Al2(SO4)3中O元素与S元素的质量比为_。(2)最后所得溶液中Na2SO4的质量分数。(3)将34.2 kg Al2(SO4)3溶液的溶质质量分数由10%变为20%可以用不同方法。请选择一种方法进行计算(只写出计算过程,不答具体操作)。16.(2022南通)二氧化锰因应用广泛而备受关注。某研究小组采用下图装置通过焙烧MnCO3制取MnO2,发生反应的化学方程式为:(1)实验过程中,石英管内剩余固体的质量和成分随温度的变化如上图所示,则焙烧MnCO3制取MnO2应该控制反应的温度不高于_C。(2)若加热到300900C时,锰的氧化物会分解产生一种常见气体,该气体为_(填化学式)。(3)试根据化学方程式求46.0gMnCO3通过熔烧最多制得的MnO2的质量是多少?(请写出计算过程)(4)若把反应温度控制在900C,充分反应后管内剩余固体的质量为_g17.(2022聊城)实际生产的纯碱产品中往往会含有少量的氯化钠,化学实践小组的同学通过实验来测定某品牌工业品纯碱的指标等级。国家标准规定工业品纯碱指标等级指标项目指标I类类类优等品一等品优等品合格品总碱量(Na2CO3计)%99.298.899.198.0实践小组成员进行的实验和有关数据如下图所示。(1)实验过程中滴加几滴酚酞试液的目的是_。(2)通过计算判断该品牌工业品纯碱属于哪一指标等级。(写出计算过程,结果数值四舍五入精确到0.1%)2022年中考化学真题汇编:计算题参考答案1.(2022天津)甲醇(CH3OH)是一种燃料。计算:(1)甲醇的相对分子质量为_;(2)甲醇中碳、氢元素的质量比为_(填最简比);(3)甲醇中氧元素的质量分数为_。【答案】(1)32 (2)31 (3)50%2.(2022铁岭葫芦岛)疫情防控期间,常用到一种免洗手消毒凝胶,其成分中含有正丙醇(化学式为C3H8O)。请计算:(1)正丙醇中碳、氢、氧元素的质量比为_(填最简整数比)。(2)正丙醇中碳元素的质量分数为_。【答案】(1)9:2:4 (2)60%3.(2022铁岭葫芦岛)硫酸亚铁在工农业生产中有重要用途,也有较高医用价值。在实验室里,模拟工业上制取硫酸亚铁的原理,向5.6g铁屑中加入100g稀硫酸,二者恰好完全反应。请计算:(1)生成硫酸亚铁的质量为_g。(2)所用稀硫酸中溶质的质量分数。【答案】(1)15.2 (2)9.8%解:设硫酸的质量为x所用稀硫酸中溶质的质量分数= 答:稀硫酸的溶质质量分数为9.8%。4.(2022新疆)一定浓度的次氯酸钠(NaClO)溶液能有效杀灭“新冠”病毒。利用次氯酸钠发生器,通过电解食盐水能够制得次氯酸钠溶液,该反应方程式为:。要制取7.45gNaClO,理论上需要NaCl的质量是_?【答案】解:设理论上需要NaCl的质量是,答:理论上需要NaCl的质量是5.85g。5.(2022昆明)ZnO用于制作油漆、药物等。将一定量的ZnO加入到100gNaOH溶液中,恰好完全反应,反应后溶液质量为108.1g。计算:(1)ZnO的质量为_g。(2)NaOH溶液中溶质的质量分数是多少?(化学方程式:)【答案】(1)8.1 (2)解:设氢氧化钠溶质质量为xx=8gNaOH溶液中溶质的质量分数为答:NaOH溶液中溶质的质量分数是8%。6.(2022梧州)实验室用质量分数为20.0%的稀硫酸处理含Ba(OH)2的废液。向100.0g废液中加入稀硫酸至溶液恰好呈中性,最终得到2.33 g沉淀。请计算:(1)配制490.0 g 20.0%的稀硫酸需质量分数为98.0%的浓硫酸_g。(2)废液中Ba(OH)2的质量分数。【答案】(1)100.0 (2)解:设废液中Ba(OH)2的质量为x。废液中Ba(OH)2的质量分数答:废液中Ba(OH)2的质量分数1.71%。7.(2022云南)学习小组用已知浓度的氢氧化钠溶液测定某硫酸溶液的浓度。取该硫酸溶液20g,滴加10%的氢氧化钠溶液,恰好完全反应时,共消耗氢氧化钠溶液40g。计算。(1)消耗的NaOH溶液中溶质的质量为_g:(2)该硫酸溶液的溶质质量分数_。(温馨提示:)【答案】(1)4 (2)解:设该硫酸溶液的溶质质量分数为x x=24.5%答:该硫酸溶液的溶质质量分数为24.5%8.(2022邵阳)取一定量NaCl和NaHCO3组成的固体样品放入烧杯中,然后将一定溶质质量分数的盐酸逐滴加入样品中,边加边搅拌,测得生成气体的质量与所加盐酸的质量关系如下图所示。请分析并计算:(1)恰好完全反应时产生气体的质量是_g;(2)a点时溶液中含有的溶质是_(填化学式);(3
在碳的一种氧化物中,碳元素与氧元素的质量比为3:8,则该氧化物中碳原子与氧原子的个数比也为3:8。
正确答案:错误
计算题:甲醇水溶液质量百分浓度92%,请把甲醇浓度换算成摩尔浓度。(甲醇水溶液的比重d=0.86;)
正确答案: 甲醇摩尔浓度=1000*0.86*0.92/32=24.73mol/l
甲醇,化学式CH3OH,是一种无色透明、易燃、有毒、无味的液体。
正确答案:错误
甲醇,化学式CH3OH,是一种无色透明、易燃、有毒、无味的液体。
正确答案:错误
甲醇与水混合物中,甲醇的质量分率为0.9,则该混合液的的密度约为()。(已知甲醇的密度为791kg/m3,水的密度为998kg/m3。)
- A、811
- B、808
- C、712
- D、800
正确答案:A
