在0.1 mol/L的CH3COOH溶液中存在如下电离平衡,对该平衡下列叙述中,正确的是( )。A.加入水后,平衡向逆反应方向移动B.加入0.1 mol/L的HCl溶液,溶液中c(H+)减小C.加入少量NaOH固体,平衡向正反应方向移动D.加入少量CH3COONa固体.平衡向正反应方向移动
题目
 ,对该平衡下列叙述中,正确的是( )。
,对该平衡下列叙述中,正确的是( )。
B.加入0.1 mol/L的HCl溶液,溶液中c(H+)减小
C.加入少量NaOH固体,平衡向正反应方向移动
D.加入少量CH3COONa固体.平衡向正反应方向移动
相似考题
更多“在0.1 mol/L的CH3COOH溶液中存在如下电离平衡,对该平衡下列叙述中,正确的是( )。 ”相关问题
-
第1题:
在0.1mol/L HAc溶液中,下列叙述中不正确的是哪一个?A.加入少量NaOH溶液,HAc电离平衡向右移动
B.加H2O稀释后,HAc的电离度增加
C.加入浓HAc,由于增加反应物浓度,使HAc电离平衡向右移动,结果使HAc电离度增加
D.加入少量HCl,使HAc电离度减小答案:C解析:提示:HAc是弱电解质,存在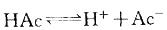 平衡。当加入少量酸或碱时,均可使平衡移动。电离度与浓度有关:
平衡。当加入少量酸或碱时,均可使平衡移动。电离度与浓度有关: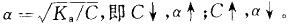 。
。 -
第2题:
有一弱酸HR,在0.1mol·L-1的溶液中有2%电离,试确定该酸在0.05mol·L-1溶液中的电离度()
- A、4.1%
- B、4%
- C、2.8%
- D、3.1%
正确答案:C -
第3题:
在一定温度下,下列因素中使0.1mol·L-1HAc溶液中pH增加的因素是()
- A、加HCl溶液
- B、加0.1mol·L-1NaCl溶液
- C、加0.1mol·L-1NaAc
- D、加入0.1mol·L-1HAc溶液
正确答案:C -
第4题:
在0.1mol·L-1HAc溶液中加入NaCl固体,使其浓度为0.1mol·L-1,溶液中H浓度和HAc的电离度都(),这种作用被称为()
正确答案:增大;盐效应 -
第5题:
下列溶液中,在检查重金属的硫代乙酰胺法中使用到的是()。
- A、0.1mol/L盐酸溶液
- B、0.1mol/L高氯酸溶液
- C、醋酸盐缓冲溶液(pH3.5)
- D、0.9mol/L氯化钠溶液
- E、0.1mol/L氢氧化钠溶液
正确答案:C -
第6题:
在1MOL/L的醋酸溶液中,存在着HAC=H++AC-的电离平衡,要使溶液中氢离子浓度增大,并且醋酸的电离度减小,可采用()。
- A、加NAOH
- B、加水
- C、加冰醋酸
- D、加醋酸钠
正确答案:C -
第7题:
在0.1mol/LHAc溶液中,下列叙述中不正确的是哪一个?()
- A、加入少量NaOH溶液,HAc电离平衡向右移动
- B、加H2O稀释后,HAc的电离度增加
- C、加入浓HAc,由于增加反应物浓度,使HAc电离平衡向右移动,结果使HAc电离度增加
- D、加入少量HCl,使HAc电离度减小
正确答案:C -
第8题:
在水溶液中可能电离的物质都能达到电离平衡。
正确答案:错误 -
第9题:
单选题在1MOL/L的醋酸溶液中,存在着HAC=H++AC-的电离平衡,要使溶液中氢离子浓度增大,并且醋酸的电离度减小,可采用()。A加NAOH
B加水
C加冰醋酸
D加醋酸钠
正确答案: C解析: 暂无解析 -
第10题:
单选题在0.1mol·L-1HAc溶液中,存在电离平衡,根据平衡移动原理,下列说法不正确的是()。A加入浓HAc,由于增加反应物浓度,平衡向右移动,结果HAc解离度增大
B加入少量NaOH溶液,平衡向右移动
C加水稀释,解离度增加
D加入少量HCl,HAc的解离度减少
正确答案: C解析: 暂无解析 -
第11题:
单选题将一植物细胞放入0.1mol·L-1的蔗糖溶液中,水分交换达到平衡时该细胞的阈值( )。A等于0.1MPa
B大于0.1MPa
C等于0MPa
D小于0MPa
正确答案: C解析:
将一植物细胞放入某种溶液中,水分交换达到平衡时该细胞的水势等于溶液的水势。溶液的Ψw=Ψs=-RTC,0.1mol·L-1的蔗糖溶液的Ψw一定小于0MPa。 -
第12题:
单选题有关EDTA叙述正确的是()。AEDTA在溶液中总共有7种型体存在
BEDTA是一个二元有机弱酸
C在水溶液中EDTA一共有5级电离平衡
DEDTA不溶于碱性溶液中
EEDTA易溶于酸性溶液中
正确答案: E解析: 暂无解析 -
第13题:
下列比较中,正确的是()。
A.同温和同物质的量浓度时,HF比HCN易电离,则溶液pH:NaF>NaCN
B.物质的量浓度相等的H2S和NaHS混合溶液中: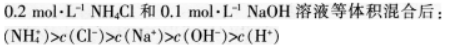
C.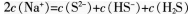
D.将①0.01mol·L-1的CH3COOH溶液;②0.01mol·L-1的盐酸;③pH=12的氨水;④pH=12的NaOH溶液稀释相同倍数后溶液的pH:③>④>②>①答案:B解析:同温和同物质的量浓度时,HF比HCN易电离,这说明HF的酸性强于HCN,酸性越弱,相应的钠盐越容易水解.所得溶液碱性越强.DH越大.则溶液DH:NaF<NaCN.A项错误:根据物料守恒可知,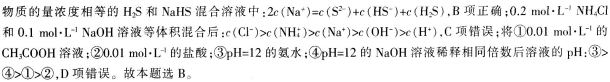
-
第14题:
在一定条件下,电离达到平衡时,下列说法正确的是()。
- A、电离是一种静态平衡
- B、电离是一种动态平衡
- C、分子电离成离子的速度等于离子结合成分子的速度
- D、在同一瞬间内,溶液中的离子和分子的浓度保持不变
正确答案:B,C,D -
第15题:
强电解质的特点是()
- A、溶液的导电能力较强
- B、在溶液中存在电离平衡
- C、在溶液中不存在分子,完全电离为离子
- D、温度一定,电离常数一定
- E、一般浓度时电离度较小
正确答案:A,C -
第16题:
设弱酸HA的电离度为α,0.1mol/L溶液中的氢离子的浓度是:()
- A、αmol/L
- B、0.1αmol/L
- C、0.01αmol/L
- D、0.001αmol/L
- E、0.0001αmol/L
正确答案:B -
第17题:
关于电离平衡,下列叙述不正确的是()。
- A、强电解质不存在电离平衡
- B、弱电解质是可逆电离
- C、在电离方程式中,阳离子和阴离子电荷的代数和为零
- D、多元酸为一步电离
正确答案:D -
第18题:
0.10 mol.L-1HAc溶液在1升0.10mol.L-1NaAc水溶液中,HAc的电离度为()
- A、10Kθa%
- B、1000θa%
- C、100θa%
- D、100θa0.1%
正确答案:B -
第19题:
在0.1mol·L-1HAc溶液中,存在电离平衡,根据平衡移动原理,下列说法不正确的是()。
- A、加入浓HAc,由于增加反应物浓度,平衡向右移动,结果HAc解离度增大
- B、加入少量NaOH溶液,平衡向右移动
- C、加水稀释,解离度增加
- D、加入少量HCl,HAc的解离度减少
正确答案:A -
第20题:
单选题下列说法中,正确的是( )。A某4.000mol/L H2SO4溶液,其H+浓度为4.000mol/L
BH3BO3的平衡常数Ka1=5.6×10-10,不能用标准碱溶液直接滴定
C在0.1mol/L HAc溶液中[H+]=0.1mol/L
DNaAc水溶液呈碱性
ENaAc水溶液呈酸性
正确答案: D解析: 暂无解析 -
第21题:
单选题设弱酸HA的电离度为α,0.1mol/L溶液中的氢离子的浓度是:()Aαmol/L
B0.1αmol/L
C0.01αmol/L
D0.001αmol/L
E0.0001αmol/L
正确答案: A解析: 暂无解析 -
第22题:
单选题向一定体积的0.1mol/L的醋酸溶液中加入等体积的蒸馏水后,则下列叙述正确的是()A溶液的pH值变小
B醋酸的电离度增大
C溶液的导电能力减弱
D中和此溶液所需的0.1mol/LNaOH溶液的体积增加
正确答案: B解析: 暂无解析 -
第23题:
单选题在0.1mol/LHAc溶液中,下列叙述中不正确的是哪一个()?A加入少量NaOH溶液,HAc电离平衡向右移动
B加H2O稀释后,HAc的电离度增加
C加入浓HAc,由于增加反应物浓度,使HAc电离平衡向右移动,结果使HAc电离度增加
D加入少量HCl,使HAc电离度减小
正确答案: D解析: 暂无解析
