下列物质中,能用来除去硫酸锌溶液中含有的少量Cu2+,而又不引入其他离子的是( )A.氢氧化钠 B.锌粉 C.铝粉 D.铁屑
题目
下列物质中,能用来除去硫酸锌溶液中含有的少量Cu2+,而又不引入其他离子的是( )
A.氢氧化钠
B.锌粉
C.铝粉
D.铁屑
B.锌粉
C.铝粉
D.铁屑
相似考题
更多“下列物质中,能用来除去硫酸锌溶液中含有的少量Cu2+,而又不引入其他离子的是( )”相关问题
-
第1题:
要除去FeCl2溶液中含有的少量Fe3+和Cu2+,应选择的试剂是(??)A.锌粉
B.铁粉
C.氯气
D.氢氧化钠答案:B解析: -
第2题:
采用什么方法和装置,可除去下列各物质中的少量杂质:
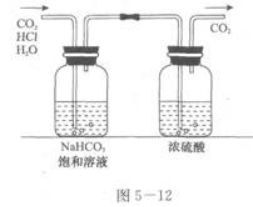
(1)二氧化碳气体中含有少量氯化氢、水蒸气.
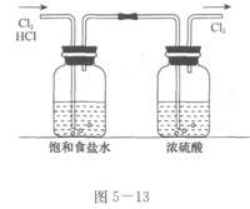
(2)氯气中含有少量氯化氢气体.答案:解析:(1)氯化氢极易溶于水,将气体通入饱和NaHC03溶液中,就可以除去氯化氢气体,然后将气体通入浓硫酸中,除去水蒸气(如图5~12所示)。 (2)氯气在饱和食盐水中溶解度很小,可将气体通人饱和食盐水中除去氯化氢气体,然后用浓硫酸干燥氯气(如图5~13所示).
-
第3题:
右图是a、b两种固体物质的溶解度曲线。下列说法中正确的是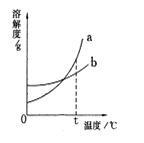 A.a物质的溶解度受温度变化的影响较大,b物质的溶解度受温度变化的影响较小
A.a物质的溶解度受温度变化的影响较大,b物质的溶解度受温度变化的影响较小
B.t℃时,等质量的a、b饱和溶液中含有相同质量的溶质
C.当温度大于t℃时,a溶液一定比b溶液浓
D.a中含有少量b时,用溶解、蒸发、结晶的方法除去a中的b答案:C解析: -
第4题:
用括号内的试剂和方法除去下列各物质的少量杂质,不正确的是( )A.苯中含有苯酚(浓溴水,过滤)
B.乙酸钠中含有碳酸钠(乙酸、蒸发)
C.乙酸乙酯中含有乙酸(饱和碳酸钠溶液、分液)
D.溴乙烷中含有醇(水、分液)答案:A解析: -
第5题:
比较CO和CO2的性质。如何除去CO中含有的少量CO2?如何除去CO2中含有的少量CO?
正确答案: 通过赤热的碳粉;通过赤热的CuO粉末。 -
第6题:
对电解质的正确叙述是()。
- A、溶于水能够导电的物质
- B、在溶液中能离解为离子的化合物
- C、在水中能生成离子的物质
- D、熔融态能够导电的物质
正确答案:B -
第7题:
在滴定分析中能导致系统误差的情况是()。
- A、试样未混均匀
- B、滴定管读数读错
- C、滴定时有少量溶液溅出
- D、所用试剂中含有干扰离子
正确答案:D -
第8题:
如果试液中含有Fe3+、Al3+、Ca2+、Mg2+、Mn2+、Cr3+、Cu2+和Zn2+等离子,加入NH4Cl和氨水缓冲溶液,控制pH为9.0左右,哪些离子以什么形式存在于溶液中?哪些离子以什么形式存在于沉淀中?分离是否完全?
正确答案:加入氨性缓冲溶液后,Ca2+和Mg2+以游离离子形式,Cu2+和Zn2+分别形成Cu(NH3)2+4、Zn(NH3)2+4存在于溶液中;Fe3+、Al3+、Mn2+、Cr3+等离子分别形成氢氧化物形式存在于沉淀中;分离基本完全。 -
第9题:
单选题下列除去杂质的方法错误的是( ).AH2中含有少量H2S,通过NaOH溶液除去
BCH4中含有少量CO2,通过Ca(OH)2溶液除去
CCO2中含有少量SO2,通过饱和NaHCO3除去
DCl2中含有少量HCl,通过NaOH溶液除去
正确答案: A解析:
Cl2中含有少量HCl,用NaOH溶液处理则Cl2与NaOH也发生反应.应当用饱和食盐水处哩,HCl被吸收,而Cl2在饱和食盐水溶液中的溶解度很小,除杂不能生成新的杂质,也不能将非杂质的物质除去. -
第10题:
单选题括号内的物质是除去下列各种物质中的杂质所选用的试剂,其中不正确的是( ).ACO中混有少量SO2(NaHCO3饱和溶液)
BCH4中混有少量HCI(NaOH水溶液)
C氢气中混有水蒸气(浓硫酸)
DFeSO4溶液中混有少量CuSO3(锌片)
正确答案: D解析:
锌片不仅能与硫酸铜溶液反应,也能与硫酸亚铁溶液反应,引入新的杂质锌离子.除杂引入新的杂质不可以. -
第11题:
填空题除去FeCl2溶液中混有的少量CuCl2,应使用的试剂为____;除去FeCl3溶液中混有的少量FeCl2,应使用的试剂为____;除去FeCl2溶液中混有的少量FeCl3,应使用的试剂为____.正确答案: 铁粉,氯气,铁粉解析:
为了出去氯化铜且不带入新杂质,可以使用铁粉除杂;出去氯化铁中的氯化亚铁可以使用还原性气体氯气,且不带入新杂质;出去二价铁中的三价铁,可以放入具有还原性的铁粉. -
第12题:
填空题原溶液中含有的溶质是____,该物质可用来做____和____.正确答案: NH4NO3,氮肥,炸药解析:
由(1)知,氨气遇浓硝酸冒白烟,生成原物质,则原物质为NH4NO3,NH4NO3可制作氮肥和炸药. -
第13题:
若要除去硫酸亚铁中含有的少量Fe3+和Cu2+,最好加入.答案:解析:铁粉 【解题指要】除杂质有以下要求:
(1)把杂质除去或使其变成能与所需要的有效成分分离开的物质.如此题为除去FeSO4中
的Fe3+和Cu2+,加入铁粉后发生如下反应:
第一个反应把杂质(Fe3+)变成了有效成分(Fe2+),这种结果最好.第二个反应把混在溶液中
的Cu2+变成了不溶于水的Cu单质,用过滤法即可与Fe2+分开.
(2)不能引入新杂质.只从与Fe3+、Cu2+反应的角度看,不加铁粉加锌粉也可以.因为加锌粉
后,发生如下反应:
从反应方程式看,的确除去了Fe3+和Cu2+,但却引入了Zn2+,不符合要求. -
第14题:
某无色透明溶液,仅由下列离子中的一种或几种组成,向该溶液中通入二氧化碳,有白色沉淀生成,滴加盐酸沉淀消失。若向溶液中滴入少量硝酸银亦会生成白色沉淀,加入硝酸沉淀不溶解,试分析下列离子中Ba2+、Fe3+、Cu2+、Cl-、CO2-3、NO-3,则溶液中一定存在的离子是______;一定不存在的离子是______;可能存在的离子是______。答案:解析:Ba2+、Cl-;
Fe3+、Cu2+、CO32-;
NO3-
溶液为无色透明,故一定不存在Fe3+、Cu2+,因为Fe3+为红褐色,Cu2+为蓝色;通入二氧化碳有白色沉淀生成,滴加盐酸后沉淀又消失,故推测一定存在Ba2+;生成的沉淀为碳酸钡白色沉淀,故溶液中一定没有CO32-;向溶液中滴入少量硝酸银,有白色沉淀生成,且加入硝酸沉淀不溶解,可推测出一定存在Cl-,生成白色沉淀为氯化银。 -
第15题:
下列物质分离方法错误的是A、除去CO2中混有少量的CO:导出点燃
B、粗盐提纯的步骤:溶解→过滤→蒸发
C、除去H2中混有的HCl:将气体通过装有NaOH溶液的洗气瓶
D、除去铜粉中混有的CuO:用足量的稀硫酸浸泡后过滤、洗涤、答案:A解析: -
第16题:
溶液中,能溶解其他物质的物质叫(),被溶解的物质叫()。
正确答案:溶剂;溶质 -
第17题:
欲除去小苏打溶液中含有的少量苏打杂质,加入的物质最宜选用()
- A、二氧化碳;
- B、盐酸;
- C、碳酸氢钙;
- D、氢氧化钙。
正确答案:A -
第18题:
下列选项中属于溶液的是()。
- A、牛奶
- B、氨水
- C、水中含有少量泥沙
正确答案:B -
第19题:
下列物质中()不宜用来除去炼厂气中的硫化氢组分
- A、乙酸铅溶液
- B、碳酸钠溶液
- C、碘液
- D、水
正确答案:D -
第20题:
单选题欲除去小苏打溶液中含有的少量苏打杂质,加入的物质最宜选用()A二氧化碳;
B盐酸;
C碳酸氢钙;
D氢氧化钙。
正确答案: D解析: 暂无解析 -
第21题:
单选题把Cl2通入下列各物质的溶液中,阳离子能被氧化的是()AK2S
BHBr
CNaI
DFeBr2
正确答案: B解析: 暂无解析 -
第22题:
单选题将下列物质加入HAc溶液中,能产生同离子效应的是()AHCl
BNaCl
CNa2CO3
DH2O
正确答案: A解析: 暂无解析 -
第23题:
问答题如果试液中含有Fe3+、Al3+、Ca2+、Mg2+、Mn2+、Cr3+、Cu2+和Zn2+等离子,加入NH4Cl和氨水缓冲溶液,控制pH为9.0左右,哪些离子以什么形式存在于溶液中?哪些离子以什么形式存在于沉淀中?分离是否完全?正确答案: 加入氨性缓冲溶液后,Ca2+和Mg2+以游离离子形式,Cu2+和Zn2+分别形成Cu(NH3)2+4、Zn(NH3)2+4存在于溶液中;Fe3+、Al3+、Mn2+、Cr3+等离子分别形成氢氧化物形式存在于沉淀中;分离基本完全。解析: 暂无解析
