2、O原子的核外电子排布式为1s22s2p4,根据价键理论,O2中能够形成的共价键类型是A.π键B.σ键C.σ键、π键D.头碰头成键
题目
2、O原子的核外电子排布式为1s22s2p4,根据价键理论,O2中能够形成的共价键类型是
A.π键
B.σ键
C.σ键、π键
D.头碰头成键
相似考题
更多“2、O原子的核外电子排布式为1s22s2p4,根据价键理论,O2中能够形成的共价键类型是”相关问题
-
第1题:
某原子失去2个核外电子后的核外电子排布与Ar原子相同。该原子的元素符号为(),原子序数为()。参考答案: Ca;20。
-
第2题:
简述电子在原子核外排布的规则,并写出N、Cu的核外电子排布式。
正确答案: (1)能量最低-多电子原子在基态时,核外电子总是尽可能分布到能量最低的轨道,这称为能量最低原理。
(2)保里不相容原理-在同一个原子中没有四个量子数完全对应相同的电子。
(3)洪特规则-电子分布到能量相同的等价轨道时,总是尽量先以自旋相同的方向单独占据能量相同的轨道。
洪特规则的特例-由光谱实验结果得到,等价轨道全充满、半充满或全空的状态是比较稳定的。 -
第3题:
已知某元素+2价离子的核外电子排布式为:[Ar]3d5,该元素在周期表中处于()周期、()族、()区,元素符号是()。
正确答案:第四;ⅦB;d;Mn -
第4题:
由极性共价键组成的分子是()。
- A、Cl2
- B、HCl
- C、H2
- D、O2
正确答案:B -
第5题:
杂化轨道理论认为,由于原子轨道侧面重叠所形成的共价键叫做σ键。
正确答案:错误 -
第6题:
H2O2分子中O-O键级为(),O2分子中O-O键级为(),O3分子中O-O键级为()
正确答案:1.0;2.0;1.5 -
第7题:
原子序数为17的元素,其原子核外电子排布式为();未成对电子数为1。
正确答案:1s22s22p63s23p5 -
第8题:
写出下列元素原子或离子的核外电子排布式: (1)Cr3+:()。 (2)P:() (3)Ca2+:()。 (4)Ni:()。
正确答案: 1S22S22P63S23P64d3;1S22S22P63S23P3;1S22S22P63S23P6;1S22S22P63S23P64d84S2 -
第9题:
价键理论指出,根据原子轨道的重叠方式不同,可把共价键分两大类,即()键。
正确答案:σ、π -
第10题:
氧分子的键级为(),而O2-的键级为()。O2的键级()于O2-的,O2键长()于O2-的。O2的键解离能比O2-的要()些。O2具有()磁性,而O2-具有()磁性。
正确答案:2;3/2;大于;小于;大;顺;顺 -
第11题:
多选题与Ne核外电子排布相同的离子跟与Ar核外电子排布相同的离子形成的化合物是()AMgBr2
BNa2S
CKCl
DKF
正确答案: C,D解析: 暂无解析 -
第12题:
判断题碳原子与碳原子之间容易形成共价键,与其它原子则不能形成共价键。()A对
B错
正确答案: 对解析: 暂无解析 -
第13题:
下列各种表述中,两个微粒属于同种元素的原子的是( )。
A.3D能级有一个空轨道的基态原子和核外电子排布为1s22s22p63s23p2的原子
B.2p能级有一个未成对电子的基态原子和价电子排布为2s22p5的原子
C.M层全充满而N层4s2的原子和核外电子排布为1s22s22p63s23p63d24s2的原子
D.最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p3的原子答案:A解析:A项,3p能级有一个空轨道的基态原子的核外电子排布为1s22s22p63s23p2,A项描述的是同种元素的原子;B项,2p能级有一个未成对电子的基态原子的核外价电子排布有两种情况:2s22p1、2s22p5,B项描述的不一定是同种元素的原子:C项.M层全充满而N层为4s:的原子的核外电子排布为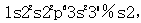 ,c项描述的不是同种元素的原子;D项.最外层电子数是核外电子总数的1/5的原子是Br,其核外电子排布为 )
,c项描述的不是同种元素的原子;D项.最外层电子数是核外电子总数的1/5的原子是Br,其核外电子排布为 )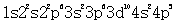 .D项描述的不是同一种元素的原子;故本题选A。
.D项描述的不是同一种元素的原子;故本题选A。 -
第14题:
两原子之间形成共价键时,首先形成的一定是σ型共价键。
正确答案:正确 -
第15题:
关于共价键的描述,下列说法正确的是()。
- A、共价键是原子之间通过相互吸引而形成的相互作用
- B、形成共价键的两个原子有共用的电子对
- C、金属与非金属元素都可以形成共价键
- D、共价键分为极性键和非极性键
正确答案:D -
第16题:
碳原子与碳原子之间容易形成共价键,与其它原子则不能形成共价键。()
正确答案:错误 -
第17题:
配合物(NH4)2[FeF5(H2O)]的系统命名为(),配离子的电荷是(),配位体是(),配位原子是(),中心离子的配位数是()。根据价键理论,中心原子的杂化轨道为(),属()型配合物。
正确答案:五氟·一水合铁(Ⅲ)酸铵;-2;5个F和1个H2OF和O6;sp3d2;外轨八面体 -
第18题:
已知某副族元素A的原子,电子最后排入3d,最高氧化数为+4;元素B的原子,电子最后排入4p,最高氧化数为+5。回答下列问题: ⑴写出A、B元素原子的核外电子排布式。 ⑵根据核外电子排布式,指出它们在周期表中的位置(周期、族)。
正确答案:⑴A:1s22s22p63s23p63d24s2;B:1s22s22p63s23p63d104s24p3。
⑵A:第四周期ⅣB族;B:第四周期ⅤA族。 -
第19题:
O2+的键级是2.5,O2的键级是2,说明O2+比O2稳定。
正确答案:正确 -
第20题:
下面选项中说法正确的为()
- A、原子形成的共价键数等于游离气态原子中不成对电子数
- B、同种原子双键的键能为单键键能的两倍
- C、键长是指成键原子的核间距离
- D、线性分子如A-B-C是非极性的
- E、共价键的极性是由成键元素的电负性差造成的
正确答案:C,E -
第21题:
与Ne核外电子排布相同的离子跟与Ar核外电子排布相同的离子形成的化合物是()
- A、MgBr2
- B、Na2S
- C、KCl
- D、KF
正确答案:B,D -
第22题:
问答题简述电子在原子核外排布的规则,并写出N、Cu的核外电子排布式。正确答案: (1)能量最低-多电子原子在基态时,核外电子总是尽可能分布到能量最低的轨道,这称为能量最低原理。
(2)保里不相容原理-在同一个原子中没有四个量子数完全对应相同的电子。
(3)洪特规则-电子分布到能量相同的等价轨道时,总是尽量先以自旋相同的方向单独占据能量相同的轨道。
洪特规则的特例-由光谱实验结果得到,等价轨道全充满、半充满或全空的状态是比较稳定的。解析: 暂无解析 -
第23题:
判断题杂化轨道理论认为,由于原子轨道侧面重叠所形成的共价键叫做σ键。A对
B错
正确答案: 对解析: 暂无解析 -
第24题:
问答题有关O2配位作用的讨论中认定氧有O2、O2-和O22-等三种形式。试根据O2的分子轨道能级图,讨论这些物种作为配体时的键级、键长和净自旋。正确答案: O2双键,较短,三重态;
O2-键级1.5,键较长,二重态;
O22-较长的单键,单重态。解析: 暂无解析
