名词解释题试验用药品
题目
相似考题
更多“试验用药品”相关问题
-
第1题:
在临床试验方案中有关试验药品管理的规定不包括:()
A.药品保存
B.药品分发
C.药品的登记与记录
D.如何移交给非试验人员
答案D -
第2题:
负责对临床试验用的所有药品作适当的包装与标签,并标明为临床试验未用的是
A.
B.
C.
D.
E.
正确答案:A
-
第3题:
为评价药品安全性,在实验室条件下,用实验系统进行的各类毒性试验应遵循A.GMPB.GAPSX为评价药品安全性,在实验室条件下,用实验系统进行的各类毒性试验应遵循
A.GMP
B.GAP
C.GCP
D.GLP
E.GSP
正确答案:D
本题考查的是药事管理体制。《药物非临床研究质量管理规范》其英文全称GoodLaboratoryPraCtiCe,简称GLP:为了提高药物临床研究的质量,确保实验资料的真实性、完整和可靠性,保障人民用药安全,并与国际上的新管理相接轨,依据《药品管理法》有关条款的规定国家药品监督管理部门制定了《药物非临床研究量管理规范》。它是为申请药品注册而进行的非床研究必须遵守的规定。要求药物研究过程中,物非临床安全性评价研究机构必须执行药物非床研究质量管理规范。药品非临床研究是指为价药品安全性,在实验室条件下,用实验系统进的各种毒性试验,包括单独给药的毒性试验、反给药的毒性试验、致癌试验、生殖毒性试验、致突试验、依赖性试验、局部用药的毒性试验及与评药物安全性有关的其他毒性试验。 -
第4题:
甲药品生产企业研发出的乙药品经国家药品监督管理部门批准后,进入了临床试验阶段。
甲药品生产企业在完成乙药品的哪一期临床试验后,可以申请新药证书和药品批准文号A.Ⅰ期临床试验
B.Ⅱ期临床试验
C.Ⅲ期临床试验
D.Ⅳ期临床试验答案:C解析:Ⅰ期临床试验的主要目的是观察人体对于新药的耐受程度和药代动力学,为制定给药方案提供依据,试验病例数为20~30例;完成Ⅲ期临床试验后,可以申请新药证书和药品批准文号。 -
第5题:
在临床试验方案中有关试验药品管理的规定不包括:()
- A、药品保存
- B、药品分发
- C、药品的登记与记录
- D、如何移交给非试验人员
正确答案:D -
第6题:
非临床研究是指为评价药品安全性,在实验室条件下,用试验系统进行各种毒性试验。
正确答案:正确 -
第7题:
()是临床试验中用于试验或参比的任何药品或安慰剂。
- A、试验用药品
- B、药品
- C、标准操作规程
- D、药品不良反应
正确答案:A -
第8题:
在申请新药临床试验时首先应制订“生产用试行质量标准”,经SFDA批准后,按此标准生产药品,供各医院临床试验用。其目的是保证临床试验用药品的安全性,使临床试验结论可靠。
正确答案:错误 -
第9题:
单选题药物临床研究中,试验用药品的管理正确的是()A试验用药品在市场上经销
B研究中的试验用药品与对照药品或安慰剂在外形、气味、包装、标签和其他特征上应有区别
C剩余的药品退回申办者
D医疗机构负责对临床试验用的所有药品做适当的包装与标签
E伦理委员会负责对试验用药品的供给、使用、储藏及剩余药品的处理过程进行检查
正确答案: A解析: 《药品临床试验管理规范》第五十三条:试验用药品不得在市场上经销。第五十四条:试验用药品的使用记录应包括数量、装运、递送、接受、分配、应用后剩余药品的回收与销毁等方面的信息。第五十五条:临床试验用药品的使用由研究者负责,研究者必须保证所有试验用药品仅用于该临床试验的受试者,其剂量与用法应遵照试验方案,剩余的药品退回申办者,上述过程需由专人负责并记录在案。研究者不得把试验用药品转交任何非临床试验参加者。第五十六:申办者负责对临床试验用的所有药品做适当的包装与标签,并标明为临床试验专用。在双盲临床试验中,研究中的试验用药品与对照药品或安慰剂在外形、气味、包装、标签和其他特征上均应一致。第五十七条:监查员负责对试验用药品的供给、使用、储藏及剩余药品的处理过程进行检查。 -
第10题:
单选题在临床试验方案中有关试验药品管理的规定不包括:()A药品保存
B药品分发
C药品的登记与记录
D如何移交给非试验人员
正确答案: A解析: 暂无解析 -
第11题:
判断题非临床研究是指为评价药品安全性,在实验室条件下,用试验系统进行各种毒性试验。A对
B错
正确答案: 对解析: 暂无解析 -
第12题:
《药品临床试验管理规范》适用于药品各期临床试验。()
答案√ -
第13题:
下列说法正确的是
A、麻醉药品和第一类精神药品不需要进行临床试验
B、麻醉药品和第一类精神药品进行临床试验,不得以健康人为受试对象
C、麻醉药品和第一类精神药品进行临床试验,必须以健康人为受试对象
D、麻醉药品不需要进行临床试验
E、第一类精神药品不需要进行临床试验
参考答案:B
-
第14题:
试验用的标准品、对照药品或安慰剂由( )提供A.有资质的公司
B.医院
C.药检所
D.申办者
E.食品药品监督管理局答案:D解析:临床试验用药品、标准品、对照品或安慰剂由申办者提供,必须易于识别、有正确编码并贴有特殊标签的并保证质量合格。 -
第15题:
关于药品有效期的说法,正确的是A.根据化学动力学原理,用高温试验按照药物降解1%所需的有效期(10%)
B.有效期可用加速试验预测,用长期试验确定
C.有效期按照药物降解50%所需时间进行推算(10%)
D.有效期按照t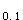 =0.1054/k公式进行推算,用影响因素试验确定
=0.1054/k公式进行推算,用影响因素试验确定
E.有效期按照t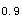 =0.693/k公式进行推算,用影响因素试验确定答案:B解析:有效期按照药物降解10%所需时间进行,加速试验推算,长期试验确定。
=0.693/k公式进行推算,用影响因素试验确定答案:B解析:有效期按照药物降解10%所需时间进行,加速试验推算,长期试验确定。 -
第16题:
不得以健康人为受试对象的是()
- A、麻醉药品和第二类精神药品的临床试验
- B、麻醉药品的临床试验
- C、精神药品的临床试验
- D、麻醉药品和第一类精神药品的临床试验
- E、麻醉药品和精神药品的临床试验
正确答案:D -
第17题:
下列哪项不正确?()
- A、《药品临床试验管理规范》是有关临床试验的准则
- B、《药品临床试验管理规范》是有关临床试验的技术标准
- C、《药品临床试验管理规范》是关于临床试验方案设计、组织实施、监查、审视、记录、分析、总结和报告标准
- D、《药品临床试验管理规范》是临床试验全过程的标准
正确答案:B -
第18题:
卫生部门和医疗机构,应当适时组织医疗事故隐患专项治理,主要解决下列哪些问题()。
- A、违反药物过敏试验规定
- B、医疗垃圾不按规定处理
- C、院内感染控制不当
- D、错用药品、滥用药品、用假药品
正确答案:A,B,C,D -
第19题:
单选题不得以健康人为受试对象的是()A麻醉药品和第二类精神药品的临床试验
B麻醉药品的临床试验
C精神药品的临床试验
D麻醉药品和第一类精神药品的临床试验
E麻醉药品和精神药品的临床试验
正确答案: E解析: 《麻醉药品和精神药品管理条例》第十三条规定麻醉药品和第一类精神药品的临床试验,不得以健康人为受试对象。 -
第20题:
单选题()是临床试验中用于试验或参比的任何药品或安慰剂。A试验用药品
B药品
C标准操作规程
D药品不良反应
正确答案: B解析: 暂无解析 -
第21题:
单选题为评价药品安全性,在实验室条件下,用实验系统进行的各类毒性试验应遵循( )。AGMP
BGSP
CGCP
DGLP
正确答案: C解析:
非临床安全性评价研究,指为评价药物安全性,在实验室条件下用实验系统进行的试验,初步目的是通过毒理学试验对受试物的毒性反应进行暴露,在非临床试验中提示受试物的安全性。药物非临床安全性评价研究的相关活动应当遵守非临床研究质量管理规范(GLP)。 -
第22题:
判断题在申请新药临床试验时首先应制订“生产用试行质量标准”,经SFDA批准后,按此标准生产药品,供各医院临床试验用。其目的是保证临床试验用药品的安全性,使临床试验结论可靠。A对
B错
正确答案: 对解析: 在申请新药临床试验时首先应制订“临床研究用质量标准”,经SFDA批准后,按此标准生产药品,仅供临床试验医院用。
