单选题向原电池(-)Ag,AgCl|Cl-‖Ag+|Ag(+)的负极中加入NaCl,则原电池电动势的变化是( )。[2013年真题]A 变大B 变小C 不变D 不能确定
题目
变大
变小
不变
不能确定
相似考题
参考答案和解析
原电池发生氧化还原反应,负极为:Ag-e-+Cl-=AgCl,正极为:Ag++e-=Ag。根据电极电势的能斯特方程式,有φ=φϴ+0.059lg[1/c(Cl-)]。由于负极中加入NaCl,Cl-浓度增加,则负极电极电势减小,正极电极电势不变,所以原电池的电动势E=φ正-φ负增大。
更多“向原电池(-)Ag,AgCl|Cl-‖Ag+|Ag(+)的负极中加入NaCl,则原电池电动势的变化是( )。[2013”相关问题
-
第1题:
某原电池符号为: ,向AgN03溶液中通入H2S气体,使Ag+生成Ag2S沉淀,这时原电池的电动势将( )。
,向AgN03溶液中通入H2S气体,使Ag+生成Ag2S沉淀,这时原电池的电动势将( )。
A.增大
B.减小
C.不变
D.不能确定答案:B解析:
-
第2题:
当溶液中同时存在Ag+和Cl-时,产生沉淀的条件为()。
A[Ag+]>[Cl-]>KspAgCl
B[Ag+]²[Cl-]>KspAgCl
C[Ag+]²[Cl-]
B
略 -
第3题:
在标准条件下将氧化还原反应Fe2++Ag+Fe3++Ag装配成原电池,原电池符号为()
- A、(-)Fe2+|Fe3+‖Ag+½Ag(+)
- B、(-)Ag|Ag+‖Fe3+½Fe2+(+)
- C、(-)Pt|Fe2+,Fe3+‖Ag+½Ag(+)
- D、(-)Ag|Ag+‖Fe2+,Fe3+½Pt(+)
正确答案:C -
第4题:
已知φθAg+/Ag=0.80V,φθZn2+/Zn=-0.76V。将两电对组成原电池,该原电池的标准电动势为()
- A、2.36V
- B、0.04V
- C、0.84V
- D、1.56V
正确答案:D -
第5题:
将反应Fe2++Ag+→Fe3++Ag构成原电池,其电池符号为()。
- A、(-)Fe2+∣Fe3+‖Ag+∣Ag(+)
- B、(-)Pt∣Fe2+∣Fe3+‖Ag+∣Ag(+)
- C、(-)Pt∣Fe2+.Fe3+‖Ag+∣Ag(+)
- D、(-)Pt∣Fe2+,Fe3+‖Ag+∣Ag∣Pt(+)
正确答案:C -
第6题:
银-氯化银电极的电极电位决定于溶液中()
- A、Ag+浓度
- B、AgCl浓度
- C、Ag+和AgCl浓度和
- D、Cl-活度
正确答案:D -
第7题:
下列反应中ΔrGmΘ等于产物ΔfGmΘ的是哪个?()
- A、Ag+(aq)+Cl-(aq)→AgCl(s)
- B、2Ag(s)+Cl2(g)→2AgCl(s)
- C、Ag(s)+1/2Cl2(g)→AgCl(s)
- D、Ag(s)+1/2Cl2(l)→AgCl(s)
正确答案:C -
第8题:
(2013)向原电池(一)Ag,AgCl│Cl-‖Ag+│Ag(+)的负极中加入NaCl,则原电池电动势的变化是:()
- A、变大
- B、变小
- C、不变
- D、不能确定
正确答案:A -
第9题:
向原电池(-)Ag、的负极中加入NaCl,则原电池电动势变化是()。
- A、变大
- B、变小
- C、不变
- D、不能确定
正确答案:A -
第10题:
电池Ag(s),AgCl(s)︱Cl-(aq)‖Ag+(aq)︱Ag可选用()做盐桥。
正确答案:NH4NO3或KNO3 -
第11题:
单选题(2013)向原电池(一)Ag,AgCl│Cl-‖Ag+│Ag(+)的负极中加入NaCl,则原电池电动势的变化是:()A变大
B变小
C不变
D不能确定
正确答案: D解析: 暂无解析 -
第12题:
单选题向原电池(-)Ag、的负极中加入NaCl,则原电池电动势变化是()。A变大
B变小
C不变
D不能确定
正确答案: D解析: 暂无解析 -
第13题:
向原电池(-)Ag,AgCl Cl- Ag+ Ag(+)的负极中加入NaCl,则原电池电动势的变化是:A.变大
B.变小
C.不变
D.不能确定答案:A解析:提示 负极氧化反应:Ag+Cl- =AgCl+e
正极还原反应:Ag++e=Ag
电池反应为:Ag++Cl-=AgCl
原电池负极能斯特方程式为: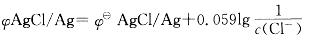
由于负极中加入NaCl,Cl-浓度增加,则负极电极电势减小,正极电极电势不变,
则电池的电动势增大。 -
第14题:
把氧化还原反应Zn+2Ag+Zn2++2Ag组成原电池,欲使该原电池的电动势增大,可采取的措施是()
- A、降低Zn2+浓度
- B、降低Ag+浓度
- C、增加Zn2+浓度
- D、加大Ag电极的表面积
正确答案:A -
第15题:
Ag+在过量的NaCl溶液中形成沉淀,则AgCl沉淀表面的吸附层主要由()构成,扩散层主要由()构成。
正确答案:Cl-;Na+ -
第16题:
增加电池(-)Cu︱Cu2+‖Ag+︱Ag(+)电动势的方法是()
- A、正极加入氨水
- B、负极加氨水
- C、正极加NaCl
- D、正极加NaBr
正确答案:B -
第17题:
电池Ag|Ag+(aq)||Cl-(aq)|Cl2(g),Pt与Ag(s),AgCl-(s)|Cl-(aq)|Cl2(g),Pt对应一个电池反应.
正确答案:错误 -
第18题:
任何AgCl溶液中,[c(Ag+)/cӨ]]和[c(Cl-)/cӨ]的乘积都等于KspӨ(AgCl)。
正确答案:错误 -
第19题:
向原电池(一)Ag,AgCl│Cl-‖Ag+│Ag(+)的负极中加入NaCl,则原电池电动势的变化是:()
- A、变大
- B、变小
- C、不变
- D、不能确定
正确答案:A -
第20题:
对原电池(-)Zn|Zn2+(c1)‖Ag(c2)|Ag(+)而言,欲使其电动势增加可采取的措施有()。
- A、增大Zn2+的浓度
- B、增加Ag+的浓度
- C、加大锌电极面积
- D、增加Ag电极的面积
正确答案:B -
第21题:
在原电池Cu∣Cu2+‖Ag+∣Ag中,若使Cu2+浓度降低,则E将(),EΘ将(),电池反应的ΔrGmΘ将()。
正确答案:增大;不变;不变 -
第22题:
电池Ag∣AgCl(s)∣Cl-∣∣Ag+∣Ag的盐桥应采用()溶液。
- A、KCL
- B、KNO3
- C、NH4CL
- D、AgNO3
正确答案:B -
第23题:
单选题对原电池(-)Zn|Zn2+(c1)‖Ag(c2)|Ag(+)而言,欲使其电动势增加可采取的措施有()。A增大Zn2+的浓度
B增加Ag+的浓度
C加大锌电极面积
D增加Ag电极的面积
正确答案: C解析: 暂无解析 -
第24题:
单选题向原电池(-)Ag,AgCl|Cl-‖Ag+|Ag(+)的负极中加入NaCl,则原电池电动势的变化是( )。[2013年真题]A变大
B变小
C不变
D不能确定
正确答案: D解析:
原电池发生氧化还原反应,负极为:Ag-e-+Cl-=AgCl,正极为:Ag++e-=Ag。根据电极电势的能斯特方程式,有φ=φϴ+0.059lg[1/c(Cl-)]。由于负极中加入NaCl,Cl-浓度增加,则负极电极电势减小,正极电极电势不变,所以原电池的电动势E=φ正-φ负增大。
