下列原子的核外电子排布,价层电子(n-1)d不为半满的是()。ACrBMoCWDMn
题目
ACr
BMo
CW
DMn
相似考题
更多“下列原子的核外电子排布,价层电子(n-1)d不为半满的是()。 ACrBMoCWDMn”相关问题
-
第1题:
下列各种表述中,两个微粒属于同种元素的原子的是( )。
A.3D能级有一个空轨道的基态原子和核外电子排布为1s22s22p63s23p2的原子
B.2p能级有一个未成对电子的基态原子和价电子排布为2s22p5的原子
C.M层全充满而N层4s2的原子和核外电子排布为1s22s22p63s23p63d24s2的原子
D.最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p3的原子答案:A解析:A项,3p能级有一个空轨道的基态原子的核外电子排布为1s22s22p63s23p2,A项描述的是同种元素的原子;B项,2p能级有一个未成对电子的基态原子的核外价电子排布有两种情况:2s22p1、2s22p5,B项描述的不一定是同种元素的原子:C项.M层全充满而N层为4s:的原子的核外电子排布为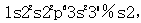 ,c项描述的不是同种元素的原子;D项.最外层电子数是核外电子总数的1/5的原子是Br,其核外电子排布为 )
,c项描述的不是同种元素的原子;D项.最外层电子数是核外电子总数的1/5的原子是Br,其核外电子排布为 )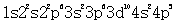 .D项描述的不是同一种元素的原子;故本题选A。
.D项描述的不是同一种元素的原子;故本题选A。 -
第2题:
关于原子核外电子的叙述,错误的是A.原子均由核及核外电子组成
B.电子沿一定轨道绕核旋转
C.核外电子具有不同壳层
D.K层最多容纳8个电子
E.K层电子离原子核最近答案:D解析:半径最小的壳层叫K层(n=1),最多容纳2n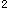 即2个电子。
即2个电子。 -
第3题:
简述电子在原子核外排布的规则,并写出N、Cu的核外电子排布式。
正确答案: (1)能量最低-多电子原子在基态时,核外电子总是尽可能分布到能量最低的轨道,这称为能量最低原理。
(2)保里不相容原理-在同一个原子中没有四个量子数完全对应相同的电子。
(3)洪特规则-电子分布到能量相同的等价轨道时,总是尽量先以自旋相同的方向单独占据能量相同的轨道。
洪特规则的特例-由光谱实验结果得到,等价轨道全充满、半充满或全空的状态是比较稳定的。 -
第4题:
核外电子总是尽先排布在能量最低的电子层里,然后再由里向外,依次排布在能量逐步升高的电子层里。
正确答案:正确 -
第5题:
元素的性质随着元素原子序数的递增而周期性变化,是由于()引起的。
- A、原子量的递增
- B、原子的核外电子的递增
- C、原子的核外电子排布的周期性变化
- D、原子的质子数发生周期性变化
正确答案:C -
第6题:
已知某副族元素A的原子,电子最后排入3d,最高氧化数为+4;元素B的原子,电子最后排入4p,最高氧化数为+5。回答下列问题: ⑴写出A、B元素原子的核外电子排布式。 ⑵根据核外电子排布式,指出它们在周期表中的位置(周期、族)。
正确答案:⑴A:1s22s22p63s23p63d24s2;B:1s22s22p63s23p63d104s24p3。
⑵A:第四周期ⅣB族;B:第四周期ⅤA族。 -
第7题:
原子序数为17的元素,其原子核外电子排布式为();未成对电子数为1。
正确答案:1s22s22p63s23p5 -
第8题:
多电子原子体系核外电子的排布遵循哪些规律?
正确答案:多电子原子体系核外电子的排布遵循保利不相容原理、能量最低原理和洪特规则三规律。 -
第9题:
写出下列元素原子或离子的核外电子排布式: (1)Cr3+:()。 (2)P:() (3)Ca2+:()。 (4)Ni:()。
正确答案: 1S22S22P63S23P64d3;1S22S22P63S23P3;1S22S22P63S23P6;1S22S22P63S23P64d84S2 -
第10题:
若把某元素原子核外电子排布写成(n-1)d4ns2时,违背了()
- A、保里不相容原理
- B、能量最低原理
- C、洪特规则
- D、洪特规则特例
正确答案:D -
第11题:
问答题简述电子在原子核外排布的规则,并写出N、Cu的核外电子排布式。正确答案: (1)能量最低-多电子原子在基态时,核外电子总是尽可能分布到能量最低的轨道,这称为能量最低原理。
(2)保里不相容原理-在同一个原子中没有四个量子数完全对应相同的电子。
(3)洪特规则-电子分布到能量相同的等价轨道时,总是尽量先以自旋相同的方向单独占据能量相同的轨道。
洪特规则的特例-由光谱实验结果得到,等价轨道全充满、半充满或全空的状态是比较稳定的。解析: 暂无解析 -
第12题:
单选题关于电子的排布规律,下列说法正确的是()A在同一个原子中,不可能有运动状态完全相同的两个电子同在
B核外电子总是尽先占能量最高的轨道
C在同一电子亚层的各个轨道上,电子的排布将尽可能分占不同的轨道,而且自旋方向相同
D核外电子总是尽先占能量最低的轨道
正确答案: B解析: 暂无解析 -
第13题:
高中化学《核外电子的排布规律》
一、考题回顾
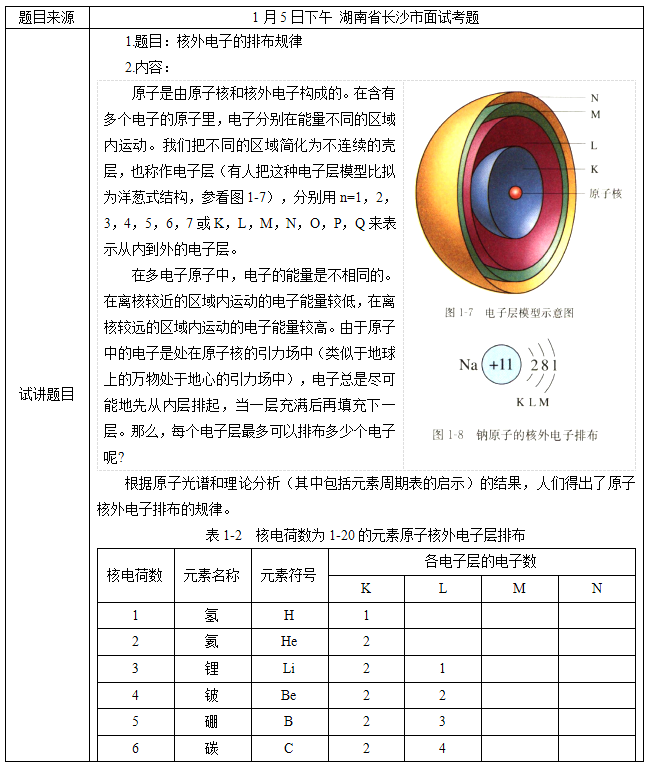
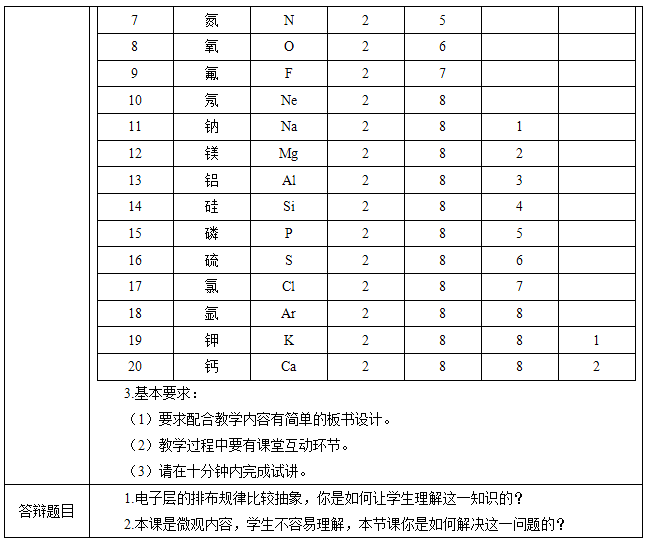
二、考题解析
【教学过程】
(一)提问导入
【提出问题】原子的结构是怎样的?
【学生回答】原子是由原子核和核外电子构成的。
【提出问题】展示短周期元素原子的核电荷数及其核外电子数,让学生观察其规律。
【学生回答】原子的核电荷数发生变化,核外电子的数目也在变化。
【教师引导】核外电子排布有何规律,本节课来进行探究。
(二)新课教学
【多媒体展现】原子的剖面示意图,提出问题:能看出原子的排列有何规律?
【学生回答】原子是分层排列的。
【提出问题】如何表示电子的这种分层排布。
【学生回答】在含有多个电子的原子里,电子分别在能量不同的区域内运动。把不同的区域简化为不连续的壳层,也称作电子层,分别用n=1,2,3,4,5,6,7或K,L,M,N,O,P,Q来表示从内到外的电子层。
【提出问题】电子在各层能量高低顺序是什么?与离核远近有什么联系?
【讨论交流】电子能量:K
【提出问题】核外电子既然是分层排布的,在排布时,电子是如何进入各电子层的呢?
【学生回答】电子总是尽可能地先从能量低的内层排起,当一层充满后,再排下一层,即是按照从能量低的电子层到能量高的电子层依次排列的。
【提出问题】结合前面已学过的碱金属元素,卤族元素的原子结构示意图,找出核外电子在每一层的排布有什么规律?
【学生回答】K层不超过2个,M层不超过8个,M层作为次外层电子数目也不超过8。
【教师总结】最外层电子数都不超过8个(K层不超过2个),次外层电子数不超过18个,倒数第三层电子数不超过32个。
【提出问题】每一电子层最多填充的电子数有什么规律?
【学生回答】每一电子层最多填充的电子数为2n2(n代表电子层数)个。
(三)拓展提高
画出卤族元素——碘元素的原子结构示意图。
(四)小结作业
小结:学生总结本节课的内容。
作业:元素的原子核外电子排布呈现周期性的变化,推断元素的性质有什么变化?
【板书设计】

【答辩题目解析】
1.电子层的排布规律比较抽象,你是如何让学生理解这一知识的?
2.本课是微观内容,学生不容易理解,本节课你是如何解决这一问题的?答案:解析:1.
首先结合课本上的模型图片和讲解给学生,按照离核的远近,电子层的能量不同,所能容纳的电子数也不同,其次继续讲解他的排布规律最多是2n2,让学生自己计算这个规律,最后结合动画图的形式,直观的播放给学生,让学生从直观到抽象,逐步的接受这节课的知识。
2.
本节课是学生走进微观世界的第一课,理解较有难度,在导入部分通过知识的前后联系提出悬疑式问题来引起学生的好奇心和求知欲,激发起他们的探究欲望,对于核外电子排布规律的知识可使用多媒体动画的方式进行直观呈现,帮助学生更好的理解原子中的电子排布,同时对于较复杂的问题可以组织学生展开小组讨论得出对应的结论。 -
第14题:
下列各组元素原子核外电子排布符合半充满规则的是()
- A、Mg
- B、Cr
- C、Si
- D、Co
正确答案:A -
第15题:
原子核外电子排布主要遵循的三个原理是什么?
正确答案:1.能量最低原理;2.泡利不相容原理;3.洪特规则 -
第16题:
通过元素周期表,可以知道元素的()。
- A、符号
- B、原子量
- C、电子数
- D、核外电子排布
正确答案:A,B,C -
第17题:
在原子核外电子排布中,通常用()来表明运动着的电子离核远近的不同。
- A、电子云
- B、运动速度
- C、能量大小
- D、电子层
正确答案:D -
第18题:
在多电子原子中,核外电子排布应遵循的三个原则是:()、()、()
正确答案:保利不相容原理;能量最低原理;洪特规则 -
第19题:
根据核外电子排布规则,可以肯定:()
- A、原子的价层电子数不超过8
- B、周期数等于基态原子的能级最高轨道的主量子数
- C、族数等于基态原子的价层电子数
- D、一个原子中,没有两个电子具有四个完全相同的量子数
- E、在多电子原子中,3d轨道的能级高于4s轨道的能级
正确答案:D -
第20题:
关于电子的排布规律,下列说法正确的是()
- A、在同一个原子中,不可能有运动状态完全相同的两个电子同在
- B、核外电子总是尽先占能量最高的轨道
- C、在同一电子亚层的各个轨道上,电子的排布将尽可能分占不同的轨道,而且自旋方向相同
- D、核外电子总是尽先占能量最低的轨道
正确答案:D -
第21题:
简述原子核外电子排布三原则。
正确答案: 泡利不相容原理、最低能量原理、洪德规则 -
第22题:
单选题关于原子核外电子排布说法错误的是()A在同一个原子中,不可能有运动状态完全相同的两个电子存在
B核外电子总是尽先占领能量最低的轨道
C在同一亚层各轨道上,电子排布尽可能分占不同的轨道,而且自旋方向相同
D电子运动与它的电子云伸展方向无关
正确答案: C解析: 暂无解析 -
第23题:
单选题今有3种原子,它们不相同的是( ).A质子数
B中子数
C核外电子数
D核外电子排布
正确答案: C解析:
这三种原子均是碳原子的同位素,他们质子数、核外电子数、核外电子排布均相同,中子数不同,质量数不同.
