将20℃时50克硝酸钾的饱和溶液蒸干,得到硝酸钾固体12g。硝酸钾在20℃时的溶解度为()g。A、31.6B、26C、40D、38
题目
将20℃时50克硝酸钾的饱和溶液蒸干,得到硝酸钾固体12g。硝酸钾在20℃时的溶解度为()g。
A、31.6
B、26
C、40
D、38
相似考题
更多“将20℃时50克硝酸钾的饱和溶液蒸干,得到硝酸钾固体12g。硝酸钾在20℃时的溶解度为()g。 ”相关问题
-
第1题:
某硝酸钾溶液在20℃时是饱和的,当其他条件不变,温度升到100℃时,该溶液不再饱和。()此题为判断题(对,错)。
参考答案:√
-
第2题:
在60℃时,硝酸钾的溶解度是110g。这句话的含义是________________________________
在60°C时,100g水中最多能溶解硝酸钾的质量为110g。 -
第3题:
一、考题回顾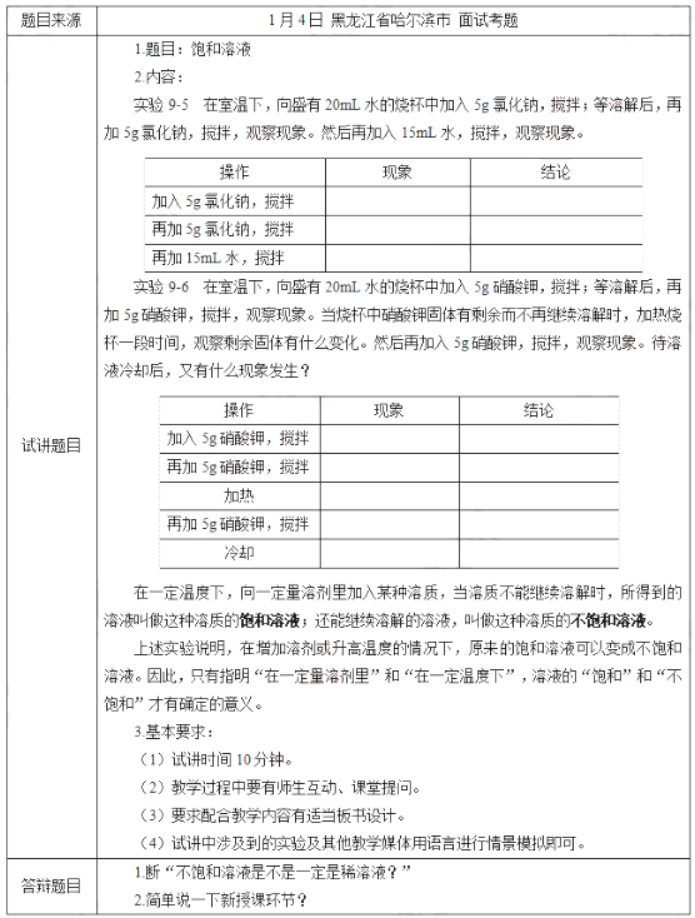
二、考题解析
【教学过程】
环节一:课堂导入
【提出问题】日常生活中在水中不断的加入糖会有什么现象产生?
【学生回答】在水中不断的加入糖,开始不断溶解,后来就不再溶解。
【教师引导】为什么不断加入糖之后,会出现不再溶解的现象?接下来就探究“饱和溶液”的内容。
环节二:新课教学
【教师引导】向盛有20mL水的烧杯中加入5g氯化钠,搅拌;等溶解后,再加5g氯化钠,搅拌,观察现象。然后再加入15mL水,搅拌,观察会产生什么现象?
【学生实验】学生按照设置好的活动小组,根据任务安排进行动手实验。
【学生回答】向盛有20mL水的烧杯中加入5g氯化钠,搅拌,氯化钠全部溶解。等溶解后,再加5g氯化钠,搅拌,氯化钠部分溶解。然后再加入15mL水,搅拌,未溶解的氯化钠继续溶解。
【教师引导】在室温下,向盛有20mL水的烧杯中加入5g硝酸钾,搅拌;等溶解后,再加5g硝酸钾,搅拌,观察现象。
【学生实验】学生按照设置好的活动小组,根据任务安排进行动手实验。
【学生回答】向盛有20mL水的烧杯中加入5g硝酸钾,搅拌,全部溶解。等溶解后,再加5g硝酸钾,搅拌,硝酸钾部分溶解。
【教师引导】当烧杯中硝酸钾固体有剩余而不再继续溶解时,加热烧杯一段时间,观察剩余固体有什么变化。然后再加入5g硝酸钾,搅拌,观察现象。待溶液冷却后,又有什么现象发生?
【学生实验】学生按照设置好的活动小组,根据任务安排进行动手实验。
【学生回答】加热烧杯后,剩余固体全部溶解。再加入5g硝酸钾,也全部溶解。待溶液冷却后,有晶体析出。
【教师总结】在一定温度下,向一定量溶剂里加入某种溶质,当溶质不能继续溶解时,所得到的溶液叫做这种溶质的饱和溶液;还能继续溶解的溶液,叫做这种溶质的不饱和溶液。
【教师提问】请学生根据对饱和溶液和不饱和溶液含义的理解,对上述实验中溶液的状态试着举例说明。
【学生回答】向盛有20mL水的烧杯中加入5g氯化钠,搅拌,氯化钠全部溶解。等溶解后,再加5g氯化钠,搅拌,氯化钠只有部分溶解,此时是饱和溶液。然后再加入15mL水,因为又能继续溶解氯化钠,所以此时为不饱和溶液。
【教师提问】通过以上实验操作,如何由不饱和溶液变成饱和溶液?
【学生回答】①加入溶质;②降温。
【教师引导】如何由饱和溶液变成不饱和溶液?
【学生回答】①增加溶剂;②升温。
【教师说明】只有指明“在一定量溶剂里”和“在一定温度下”,溶液的“饱和”和“不饱和”才有确定的意义。
环节三:巩固提高
1.在大箩卜上挖一个孔,向其中注入饱和食盐水,一段时间后,将食盐水倒出来,在相同温度下,发现在倒出的溶液中还可以溶解少量食盐。这说明( )。
A.倒出的溶液是饱和溶液 B.倒出的溶液是不饱和溶液
C.原溶液中溶剂多了 D.原溶液中溶质少了
【答案】AC。
环节四:小结作业
学生总结归纳本节课所学主要知识,表述学习心得。
作业:思考“某溶质的饱和溶液一定是浓溶液吗?”。
【板书设计】 答案:解析:
答案:解析: -
第4题:
在一定的温度下,从50g硝酸钾饱和溶液中取出5g溶液,剩下的溶液变为不饱和溶液。()此题为判断题(对,错)。
参考答案:错误
-
第5题:
在20℃时,将40g硝酸钾固体加入100g水中,充分搅拌后,仍有8.4g硝酸钾固体未溶解。请填写下列空白:
(1)所得溶液是20℃时硝酸钾的__________溶液(填“饱和”或“不饱和”);
(2)20℃时硝酸钾的溶解度为__________;
(3)所得溶液中硝酸钾的质量分数为_________。
①饱和 ②31.6g ③24%
