碘量法的误差主要来源是( )。A.碘容易挥发 B.pH的干扰 C. D.指示剂不灵敏
题目
碘量法的误差主要来源是( )。
A.碘容易挥发
B.pH的干扰
C.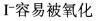
D.指示剂不灵敏
B.pH的干扰
C.
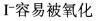
D.指示剂不灵敏
相似考题
参考答案和解析
答案:A
解析:

更多“碘量法的误差主要来源是( )。”相关问题
-
第1题:
使用碘量法滴定时,误差的主要来源是什么?如何减小误差?
参考答案:解:(1)误差来源主要是I2挥发和I-被O2氧化
(2)减小误差的措施:防止I2挥发的方法:加入过量的KI(比理论值大2~3倍);在室温中进行;使用碘瓶,快滴慢摇。
防止I-被O2氧化的方法:降低酸度,以降低I-被O2氧化的速率;防止阳光直射,除去Cu2+、NO2-等催化剂,避免I-加速氧化;使用碘量瓶,滴定前的反应完全后立即滴定,快滴慢摇。
-
第2题:
简述碘量法的误差来源主要有哪两个方面?如何避免?
正确答案: 一是I2容易挥发,二是I-在酸性溶液里容易被空气氧化。
⑴、防止I2挥发的方法加入过量的KI(一般比理论值大2-3倍)I2+I-=I-3;反应在室温(<250C)下进行;滴定时轻摇,最好用带塞的三角瓶(碘量瓶)
⑵、防止I-被空气氧化的方法避免阳光照射;析出I2后,一般应及时用Na2S2O3溶液滴定;滴定速度应适当快些。 -
第3题:
碘量法的误差来源有那些?
正确答案:一是碘具有挥发性易损失
二是I-在酸性溶液中易被来源于空气中的氧氧化而析出I2 -
第4题:
碘量法的主要误差来源是()和()。
正确答案:I2的挥发性;I-的易被氧化 -
第5题:
碘量法误差的来源?
正确答案: (1)碘具有挥发性,易损失,
(2)碘离子在酸性溶液中易被崐空气中的氧所氧化而析出碘。 -
第6题:
碘量法的误差来源有I2的挥发、I-被空气氧化。
正确答案:正确 -
第7题:
间接碘量法的主要误差来源()
- A、碘的挥发和碘离子的氧化
- B、碘的挥发
- C、碘离子的氧化
- D、Na2S2O3不稳定
正确答案:A -
第8题:
间接碘量法的主要误差来源为()、沉淀分子挥发和()
正确答案:溶液的酸度;碘离子氧化 -
第9题:
简述碘量法误差的主要来源。
正确答案: (1)碘的挥发
预防:过量加入KI——助溶,防止挥发;增大浓度,提高速度;溶液温度勿高,在室温下进行;碘量瓶中进行反应(磨口塞,封水);滴定中勿过分振摇;
(2)碘离子的氧化(酸性条件下)
预防:控制溶液酸度,酸度增大加快氧化;避免光照(暗处放置);碘单质完全析出后立即滴定;除去催化性杂质(NO3-,NO,Cu2+) -
第10题:
问答题简述碘量法的误差来源主要有哪两个方面?如何避免?正确答案: 一是I2容易挥发,二是I-在酸性溶液里容易被空气氧化。
⑴、防止I2挥发的方法加入过量的KI(一般比理论值大2-3倍)I2+I-=I-3;反应在室温(<250C)下进行;滴定时轻摇,最好用带塞的三角瓶(碘量瓶)
⑵、防止I-被空气氧化的方法避免阳光照射;析出I2后,一般应及时用Na2S2O3溶液滴定;滴定速度应适当快些。解析: 暂无解析 -
第11题:
填空题碘量法的误差来源时()和()正确答案: I-的氧化和I2的挥发解析: 暂无解析 -
第12题:
问答题碘量法的主要误差来源有哪些?为什么碘量法不适宜在高酸度或高碱度介质中进行?正确答案: 碘量法的主要误差来源有以下几个方面:
(1) 标准溶液的遇酸分解;
(2) 碘标准溶液的挥发和被滴定碘的挥发;
(3) 空气对KI的氧化作用:
(4) 滴定条件的不适当。
由于碘量法使用的标准溶液和它们间的反应必须在中性或弱酸性溶液中进行。因为在碱性溶液中,将会发生副反应:
S2O32-+4I2+10OH-=2SO42-+8I-+5H2O
而且在碱性溶液中还会发生歧化反应:
3I2+6OH-=IO3-+5I-+3H2O
如果在强碱性溶液中,溶液会发生分解:
S2O32-+2H+=SO2↑+S↓+H2O
同时,在酸性溶液中也容易被空气中的氧所氧化:
4I-+4H++O2=2I2+2H2O
基于以上原因,所以碘量法不适宜在高酸度或高碱度介质进行。解析: 暂无解析 -
第13题:
简述碘量法的误差来源及减小误差的方法。
正确答案: 碘量法的误差来源主要有两个:一是碘具有挥发性,易损失;二是I-在酸性条件下易被空气中的氧氧化而析出I2。
因此,为了避免碘的挥发,应避免阳光照射,并且滴定时应在较低温度下进行。用间接碘量法时,最好在碘量瓶中进行。为减少I-与空气的接触,并减少I2的挥发,滴定时不应过度摇动,开始滴定时应快滴慢摇,近终点时应慢滴快摇,以免淀粉吸附I2。 -
第14题:
简述碘量法误差来源及减小误差的方法。
正确答案: 碘量法误差来源于碘的挥发及I-在酸性溶液中易被空气中的O2氧化。
解决方法:针对于碘的挥发不应让溶液温度过高,一般室温下进行,振摇不宜过度剧烈,可加入过量的KI,在间接碘量法中,滴定反应在碘量瓶中进行。
针对于易被氧化,可用棕色试剂瓶贮存I-标准溶液,避免日光照射,设法消除Cu2+
、NO2-等的催化作用,滴定速度适当快些。 -
第15题:
碘量法的误差来源主要有哪两方面?
正确答案: 一是碘的挥发损失.
二是酸性碘化物溶液能被空气中的氧缓慢地氧化。 -
第16题:
碘量法的主要误差源是()。
正确答案:碘的挥发和碘离子的氧化 -
第17题:
碘量法误差来源有两个,一个()二是()。
正确答案:碘具有挥发性易损失;I-在酸性溶液中易被来源于空气中氧化而析出I2 -
第18题:
碘量法中的主要误差来源有哪些?配制、标定和保存I2及As2O3标准溶液时,应注意哪些事项?
正确答案: 主要误差来源有两个方面:一是I2易挥发,在强碱性溶液中会发生歧化反应;二是在酸性溶液中,I-易被空气中的O2氧化。配制、标定和保存I2及As2O3标准溶液时的注意事项:配制I2溶液时,先在托盘天平上称取一定量碘,加入过量KI,置于研钵中,加少量水研磨,使I2全部溶解,然后将溶液稀释,倾入棕色瓶于暗处保存。保存I2溶液时应避免与橡皮等有机物接触,也要防止I2溶液见光遇热,否则浓度将发生变化。
标定I2溶液的浓度时,可用已标定好的Na2S2O3标准溶液来标定,也可用As2O3来标定。As2O3难溶于水,但可溶于碱溶液中,与I2的反应是可逆的,在中性或微碱性溶液中,反应定量向右进行。因此标定时先酸化溶液,再加NaHCO3,调节pH≈8。 -
第19题:
碘量法中的主要误差来源是由于硫代硫酸钠标准溶液不稳定,容易与空气和水中的氧反应,使滴定结果偏高。
正确答案:错误 -
第20题:
间接碘量法的主要误差来源是Na2S2O3不稳定。
正确答案:错误 -
第21题:
填空题间接碘量法的主要误差来源为()、沉淀分子挥发和()正确答案: 溶液的酸度,碘离子氧化解析: 暂无解析 -
第22题:
单选题间接碘量法的主要误差来源()A碘的挥发和碘离子的氧化
B碘的挥发
C碘离子的氧化
DNa2S2O3不稳定
正确答案: A解析: 暂无解析 -
第23题:
判断题间接碘量法的主要误差来源是Na2S2O3不稳定。A对
B错
正确答案: 对解析: 暂无解析
