(1) X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为__________________________
题目
(1) X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为__________________________
相似考题
更多“(1) X的硫酸盐溶液与过量NaOH溶液反应的离子方程式为__________________________ ”相关问题
-
第1题:
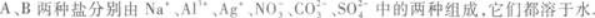
(1)往两种溶液中分别加入盐酸,A溶液不反应,B溶液产生无色无味气体.
(2)往两种溶液中分别加入过量NaOH溶液,A溶液先产生白色沉淀,然后沉淀消失,B溶液与NaOH不反应.
(3)往两种盐溶液中分别加入BaCl2溶液,都产生白色沉淀.再分别加入稀HNO3,A中沉淀不消失,B中沉淀消失.由此可知,A的化学式为____________,B的化学式为____________.答案:解析:Al2(SO4)3 Na2CO3 【解题指要】 解答此类题目,应熟知各种离子的鉴别反应及反应的特殊现象.另外,分析时应全面照顾,不要漏掉条件.
(1)加入盐酸,B溶液产生无色无味气体.在给出的6种离子中只

即B一定是碳酸盐.
(2)加入过量NaOH溶液,A溶液先产生白色沉淀,然后沉淀消失,显然这是Al3+的特征反应.其反应方程式为
即A中一定含有Al3+,是铝盐.
(3)向A、B溶液中分别加入BaCl2溶液,都有白色沉淀生成.再分别加入稀HNO3,A中沉淀

-
第2题:
当含有铜离子的溶液和含有氰根离子的溶液相混合时,将发生什么变化?若氰根离子过量时,有出现什么现象?为什么?写出相关方程式。
错误 -
第3题:
2、用相同浓度的H3PO4(pKa1 = 2.17,pKa2 = 7.20 ,pKa3 = 12.32)和NaOH溶液,配制pH = 7.00的缓冲溶液,关键是要假定分步反应时哪种溶液过量的问题。下列几种步骤的假定中正确的是
A.假定第一步H3PO4溶液过量
B.假定第一步NaOH溶液过量,第二步再假定NaH2PO4溶液过量
C.假定第一步、第二步都是NaOH溶液过量,第三步再假定NaH2PO4溶液过量
D.无法配制
假定第一步 NaOH 溶液过量,第二步再假定 NaH2PO4 溶液过量 -
第4题:
用相同浓度的H3PO4(pKa1 = 2.17,pKa2 = 7.20 ,pKa3 = 12.32)和NaOH溶液,配制pH = 7.00的缓冲溶液,关键是要假定分步反应时哪种溶液过量的问题。下列几种步骤的假定中正确的是
A.假定第一步H3PO4溶液过量
B.假定第一步NaOH溶液过量,第二步再假定NaH2PO4溶液过量
C.假定第一步、第二步都是NaOH溶液过量,第三步再假定NaH2PO4溶液过量
D.无法配制
假定第一步 NaOH 溶液过量,第二步再假定 NaH2PO4 溶液过量 -
第5题:
下列离子中,与过量NaOH溶液反应不生成沉淀的是
A.Be2+
B.Mg2+
C.Bi3+
D.Sr2+
B
