(2) 向滤液I中加入铁粉,发生反应的离子方程式为:_________________________、_______________________________________。
题目
(2) 向滤液I中加入铁粉,发生反应的离子方程式为:_________________________、_______________________________________。
相似考题
更多“(2) 向滤液I中加入铁粉,发生反应的离子方程式为:_________________________、_______________________________________。”相关问题
-
第1题:
醋酸钠固体跟盐酸反应,其离子反应方程式为__________。答案:解析:
-
第2题:
向AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,反应完成后过滤,下列情况不可能存在的是()A、滤纸上有Ag、Cu、Fe、Zn,滤液中有Zn2+、Fe2+
B、滤纸上有Ag、Cu,滤液中有Zn2+、Fe2+
C、滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Fe2+
D、滤纸上有Ag、Cu、Fe,滤液中有Cu2+、Zn2+、Fe2+答案:A,D解析: -
第3题:
稀硫酸滴在铜片上,所发生的反应的离子方程式是Cu+2H+=Cu2++H2↑。
正确答案:错误 -
第4题:
有一瓶两种阴离子混合的溶液,加入HCl有浑浊现象,且有刺激性气味产生,加入过量的HCl,再加入BaCl2溶液有白色沉淀产生,问阴离子溶液的组成,并写出反应方程式
正确答案:SO42-,S2O32-
S2O32-+2H+=S↓+SO2↑+H2O
Ba2++SO42-=BaSO4↓ -
第5题:
某一金属盐溶液,加入适量Na2CO3生成灰绿色沉淀,再加入H2O2并煮沸,此时溶液呈黄色,冷却并酸化此溶液,再加入H2O2溶液呈蓝色,此蓝色化合物在水中不稳定,在乙醚中较稳定,写出上述各反应的离子方程式
正确答案:加Na2CO3:CO32-+H2O===HCO3-+OH-
Cr3++3OH-=Cr(OH)3↓(灰绿色)
加H2O2煮沸:
2Cr(OH)3+3H2O2+4OH-===2CrO42-(黄色)+8H2O
酸化:
2CrO42-+2H+Cr2O72-+H2O
再加H2O2:
Cr2O72-+4H2O2+2H+====2CrO5(深绿色)+5H2O -
第6题:
向一含的四种离子(主要离子)的混合溶液中滴加AgNO3溶液,至不再有沉淀析出为止.过滤,当用稀硝酸处理沉淀时,砖红色沉淀溶解得橙色溶液,但仍有白色沉淀.滤液呈紫色,用硫酸酸化后,加入Na2SO3,则紫色逐渐消失.作"焰色反应"透过蓝色钴玻璃可以看到紫色火焰.指出上述溶液有何物质?并写有关反应方程式
正确答案: 混合液中含有:KClK2CrO4KMnO4
当加入AgNO3:Ag++Cl-=AgCl↓(白)
2Ag++CrO42-=Ag2CrO4↓(砖红)
加入稀HNO3:AgCl不溶
2Ag2CrO4+2H+=4Ag++Cr2O72-(橙红)+H2O
加入H2SO4酸化,再加入Na2SO3,
2MnO4-+5SO32-+6H+=2Mn2++5SO42-+3H2O -
第7题:
向某溶液中加入过量盐酸,生成白色沉淀,过滤后向滤液中加入过量氨水使溶液呈碱性,又有白色沉淀生成,在过滤后又向溶液中加入Na2CO3溶液,再次生成白色沉淀。原溶液中含有的离子是()()()
正确答案:Ag+;Al3+;Ba2+ -
第8题:
向Fe3+离子的溶液中加入硫氰化钾或硫氰化铵溶液时,然后再加入少许铁粉, 有何现象并说明之?
正确答案:向Fe3+的溶液中加入SCN-时,形成[Fe(SCN)n]3-n(n=1-6)而溶液呈血红色。若加入少许铁粉,使Fe3+还原成Fe2+,破坏了[Fe(SCN)n]3-n,因此,血红色又消失。 -
第9题:
离子反应方程式是指用参加反应的()表示化学反应的方程式。
正确答案:离子 -
第10题:
用实际参加反应的离子的符号来表示化学反应的方程式,叫做离子方程式。
正确答案:正确 -
第11题:
填空题往物质的量浓度相同的氯化铜、三氯化铁和氯化铝的混合溶液中,加入过量铁粉,充分反应后进行过滤,滤纸上得到的反应产物是____,滤液中浓度最大的金属离子是____.正确答案: Cu,Fe2+解析:
铁粉还原Cu2+生成Cu,铁粉还原Fe3+生成Fe2+,同时铁粉在反应中也变为Fe2+,因此滤液中浓度最大的金属离子是Fe2+. -
第12题:
单选题HClO的酸性比HCl弱,可逆反应方程式为:,到达平衡后,要使HClO的浓度显著增大,可加入( )ACaCO3(s)
BHCI(g)
CNaOH(s)
DH2O(I)
正确答案: D解析:
B项,要使HClO的浓度显著增大,即使平衡向右移动,在题目给出的CaCO3、HCl、NaOH、H2O中,HCl使平衡向左移动;D项,加入H2O,可使平衡向右移动,生成的HClO较多,但同时加入H2O也使溶液体积增大,所以HClO的浓度不一定增大,即使增大,也不是“显著”增大;C项,加入NaOH,因消耗了HCl和HClO而使平衡向右移动,但反应最终得到的是NaCl和NaClO,所以不能使HClO浓度增大;A项,加入CaCO3,因CaCO3可与强酸HCl反应,而不与弱酸HClO反应,所以因消耗HCl而使平衡向右移动,最终使HClO的浓度显著增大. -
第13题:
向某溶液中加入过量盐酸生成白色沉淀,过滤后向滤液中加入过量的氨水(使溶液呈碱性).又有白色沉淀生成:再过滤后向滤液中加入碳酸钠溶液,又生成白色沉淀。则原溶液中含有的离子可能是()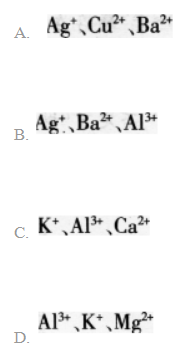 答案:B解析:
答案:B解析:
-
第14题:
往BaCl2和CaCl2的水溶液中分别依次加入:(1)碳酸铵;(2)醋酸;(3)铬酸钾,各有何现象发生?写出反应方程式。
正确答案: BaCl2+(NH4)2CO3=BaCO3↓+NH4Cl
BaCl2+2CH3COOH=Ba(CH3COO)2↓+2HCl
BaCl2+K2CrO4=BaCrO4↓+2KCl
CaCl2+(NH4)2CO3=CaCO3↓+2NH4Cl
CaCl2+2CH3COOH=Ca(CH3COO)2↓+ 2HCl
CaCl2+K2CrO4=CaCrO4•2H2O↓+2KCl -
第15题:
写出下列反应方程式并注明产物颜色:向K2Cr2O7溶液中加入Ag+离子有()色沉淀生成,其反应式为()
正确答案: 砖红色;Cr2O72-+4Ag++H2O==2H++2Ag2CrO4↓ -
第16题:
写出下列反应方程式,并注明产物颜色:向K2Cr2O7溶液中加入Ba2+离子生成()色沉淀,其反应式为()
正确答案:黄色;Cr2O72-+2Ba2++H2O==2H++2BaCrO4↓ -
第17题:
某一金属盐溶液,加入适量Na2CO3生成灰绿色沉淀,再加入H2O2并煮沸,此时溶液呈黄色,冷却并酸化此黄色溶液,再加入H2O2溶液呈深蓝色,此蓝色化合物在水中不稳定,在乙醚中较稳定,写出上述各反应的离子方程式
正确答案: 加Na2CO3:
CO32-+H2O==HCO3-+OH-
Cr3++3OH-=Cr(OH)3↓(灰绿)
加H2O
2Cr(OH)3+3H2O2+4OH-=2CrO42-(黄)+8H2O
酸化:
2CrO42-+2H+=Cr2O72-+H2O
再加H2O2
Cr2O72-+4H2O2+2H+=2CrO5(蓝)+5H2O -
第18题:
下列化学方程式或离子方程式正确的是()。
- A、常温下,将铁片置于浓硝酸中:Fe+6HNO3=Fe(NO3)3+3NO2↑+3H2O
- B、向氯化铵的稀溶液中加入少量NaOH:NH4++OH-=NH3↑+H2O
- C、向(NH4)2SO4溶液中加入适量Ba(OH)2:Ba2++SO42-=BaSO4↓
- D、向浓硝酸中加入铜片:Cu+4H++2NO3-=Cu2++2NO2↑+2H2O
正确答案:D -
第19题:
完成并配平反应方程式:H2O2+I-+H+→
正确答案: H2O2+2I-+2H+ === I2+2H2O。 -
第20题:
在Na2S2O3的溶液中加入(),则产生黄色沉淀和刺激性气体,其离子反应方程式为(),这是鉴定S2O32-的常用方法。
正确答案:稀HCl;S2O32↑+2H+===S↓+SO2↑+H2O -
第21题:
把含有少量Cu(OH)2的铁粉加入硫酸中,反应完成后,铁粉有剩余,过滤后,滤渣中有()。
- A、Fe和Cu、
- B、Fe、
- C、Cu、
- D、Fe和Cu(OH)2
正确答案:A -
第22题:
+3价铁盐跟铁粉在溶液中发生反应能生成亚铁盐,现将生锈的铁粉(足量)放入稀盐酸中,先后观察到哪些现象?写出反应的化学方程式。
正确答案: 先看到溶液变成黄色,然后铁粉表面有气泡生成,最后看到溶液逐渐变成浅绿色:Fe2O3+6HCl===2FeCl3+3H2O
Fe+2HCl===FeCl2+H2↑Fe+2FeCl3====3FeCl2 -
第23题:
单选题在含有NH4+、Cu2+、Na+的溶液中,加入过量铁粉充分反应后,溶液中不能大量存在的离子是( ).ANH4+
BNa+
CFe2+
DCu2+
正确答案: A解析:
Fe和Cu2+会发生置换反应,生成Fe2+和Cu.
