对乙酰氨基酚片剂溶出度测定:取标示量为0.3g的本品6片,依法在1000mL溶剂中测定溶出度。经30分钟时,取溶液5mL滤过,精密吸取续滤液1mL,加0.04%氢氧化钠溶液稀释至50mL,摇匀,在257nm波长处测得每片的吸收度分别为0.345,0.348,0.351,0.359,0.356和0.333,按其百分吸收系数为715计算出各片的溶出量。限度为标示量的80%。其溶出度符合规定。
题目
对乙酰氨基酚片剂溶出度测定:取标示量为0.3g的本品6片,依法在1000mL溶剂中测定溶出度。经30分钟时,取溶液5mL滤过,精密吸取续滤液1mL,加0.04%氢氧化钠溶液稀释至50mL,摇匀,在257nm波长处测得每片的吸收度分别为0.345,0.348,0.351,0.359,0.356和0.333,按其百分吸收系数为715计算出各片的溶出量。限度为标示量的80%。其溶出度符合规定。
相似考题
更多“对乙酰氨基酚片剂溶出度测定:取标示量为0.3g的本品6片,依法在”相关问题
-
第1题:
对乙酰氨基酚难溶于水,今将其制成口服片剂(规格为0.3克),试验发现有裂片和溶出度不合格的问题。试分析原因,并根据片剂成型理论和Noyes一Whitney方程讨论应采取的措施。
正确答案:产生裂片和溶出度不合格的原因可能是:对乙酰氨基酚的可压性差由于规格较大(0.3g)使可加入的稀释剂量很少或没有稀释剂选用的辅料的可压性不理想选用的黏合剂黏性不足或用量不够制成的颗粒太干或细粉太多都会导致裂片;对乙酰氨基酚难溶于水由于可加入的辅料量少选用的辅料亲水性不好(如常用的润滑剂硬脂酸镁为疏水性的)或崩解剂的崩解性能不理想且药物的粒径较大都会导致溶出度不合格。 可采取以下措施解决: ①药物经粉碎减小粒径增大药物的溶出面积;②在处方中加入可压性好、亲水性好的辅料如乳糖;③选用亲水性的润滑剂;④加入优良的崩解剂;⑤加入表面活性剂以改善片剂的润湿性;⑥选用黏合性能好又不影响片剂崩解性能的黏合剂如聚维酮;⑦控制颗粒含水量适中。
产生裂片和溶出度不合格的原因可能是:对乙酰氨基酚的可压性差,由于规格较大(0.3g),使可加入的稀释剂量很少或没有稀释剂,选用的辅料的可压性不理想,选用的黏合剂黏性不足或用量不够,制成的颗粒太干或细粉太多,都会导致裂片;对乙酰氨基酚难溶于水,由于可加入的辅料量少,选用的辅料亲水性不好(如常用的润滑剂硬脂酸镁为疏水性的)或崩解剂的崩解性能不理想,且药物的粒径较大,都会导致溶出度不合格。可采取以下措施解决:①药物经粉碎减小粒径增大药物的溶出面积;②在处方中加入可压性好、亲水性好的辅料如乳糖;③选用亲水性的润滑剂;④加入优良的崩解剂;⑤加入表面活性剂以改善片剂的润湿性;⑥选用黏合性能好又不影响片剂崩解性能的黏合剂如聚维酮;⑦控制颗粒含水量适中。 -
第2题:
复方对乙酰氨基酚片中对乙酰氨基酚的含量测定法
正确答案:B
-
第3题:
对乙酰氨基酚片(标示量为0.3g/片)的含量测定: 取本品20片,精密称定为7.2200g,研细,精密称取0.0506,置250ml量瓶中,加0.4%氢氧化钠溶液50ml与水50ml,振摇15分钟,加水至刻度,摇匀,滤过,精密量取续滤液5ml,置100ml量瓶中,加0.4%氢氧化钠溶液 10ml,加水至刻度,摇匀,照紫外-可见分光光度法(附录ⅣA),在257nm的波长处测定吸光度为0.590,已知 C8H9NO2的吸收系数(E1%1cm)为715。药典规定:本品含对乙酰氨基酚(C8H9NO2)应为标示量的95.0~105.0%。请计算本品的含量,并判断本品是否符合药典的规定。
答案:本品的含量为0.2947g/片,符合药典规定。
解析:吸收系数(E1%1cm)为715,其物理意义为溶液的浓度为1%(g/mL),液层厚度为1cm时的吸光度。
已知对照品浓度为1g/100ml的溶液吸光度为715,故样品中含C8H9NO2为0.590*20*250/715/100=0.0413g,每一片含量为0.0413*7.2200/0.0506/20=0.2947g,本品含量为标示量的0.2947g/0.3g*100%=98.23%。故符合药典规定。
-
第4题:
中国药典规定片剂溶出度测定结果判断标准中,规定的限度(Q)应为标示量的
A.0.99
B.0.8
C.0.999
D.0.9
E.0.7
正确答案:E
-
第5题:
中国药典对片剂进行溶出度检查,限度(Q)应为标示量的
A、95%
B、60%
C、75%
D、90%
E、70%
参考答案:E
-
第6题:
根据下列实验,判断正确的是精密称取对乙酰氨基酚42mg,置250ml量瓶中,加0.4%氢氧化钠溶液50ml,溶解后,加水至刻度,摇匀,精密量取5ml,置100ml量瓶中,加0.4%氢氧化钠溶液10ml,加水至刻度,摇匀,采用紫外一可见分光光度法,在257nm的波长处测定吸光度为0.605,按对乙酰氨基酚(C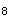 H
H NO
NO )的吸收系数(
)的吸收系数( )为715计算,即得A.对乙酰氨基酚的含量是100.7%
)为715计算,即得A.对乙酰氨基酚的含量是100.7%
B.本实验用的是紫外分光光度法中的吸光度法
C.对乙酰氨基酚的含量是98.9%
D.为稀释倍数;W为供试品的取样量(g)。
E.对乙酰氨基酚的含量是100.3%答案:A解析:吸收系数法,按各品种项下的方法配制供试品溶液,在规定的波长处测定其吸光度,以该品种在规定条件下的吸收系数计算含量。按吸收系数法计算含量: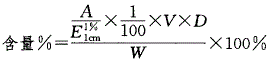 式中,A为供试品溶液的吸光度;
式中,A为供试品溶液的吸光度;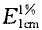 为百分吸光系数;V为供试品溶液原始体积(ml);
为百分吸光系数;V为供试品溶液原始体积(ml); -
第7题:
溶出度测定的结果判断中,除另有规定外,Q值应为标示量的()
- A、60%
- B、70%
- C、80%
- D、90%
正确答案:B -
第8题:
中国药典(2000年版)规定片剂溶出度测定结果的判断标准中,规定的限度(Q)一般为标示量的()
- A、50%
- B、90%
- C、80%
- D、70%
- E、30%
正确答案:D -
第9题:
烟酸片(标示量0.3g/片)的含量测定:取本品10片,精密称定总重量为3.5840g研细,取细粉0.3729g,加新沸的水50ml,置水浴上加热,使其溶解,放冷至室温,加酚酞指示剂3滴,用NaOH(0.1005mol/L)滴定,消耗25.20ml,标示量为()%。(已知1ml0.1mol/LNaOH相当于12.31mg烟酸)
正确答案:99.9 -
第10题:
填空题醋酸氢化可的松注射液含量测定方法如下:取本品摇匀,精密量取2mL,置100mL量瓶中,加无水乙醇稀释至刻度,摇匀,精密量取2mL,置另一100mL量瓶中,加无水乙醇稀释至刻度,摇匀,照分光光度法在241nm波长测定吸收度A=0.389。已知E1%1cm=395,标示量=25mg/mL,本品的标示量为()%。正确答案: 98.5解析: 暂无解析 -
第11题:
填空题VB 12注射液(标示量为0.1mg/ml)含量测定:精密量取本品7.5ml,置25ml量瓶中,加蒸馏水稀释至刻度摇匀,置1cm石英池中蒸馏水为空白在361±1nm处测定吸收度A=0.593,按VB 12的 =207计算,其标示量为()%。正确答案: 95.5解析: 暂无解析 -
第12题:
单选题中国药典(2000年版)规定片剂溶出度测定结果的判断标准中,规定的限度(Q)一般为标示量的()A50%
B90%
C80%
D70%
E30%
正确答案: D解析: 暂无解析 -
第13题:
《中国药典》(2005年版)收载的对乙酰氨基酚制剂中需检查溶出度的有( )
 正确答案:ABC
正确答案:ABC
-
第14题:
紫外分光光度法可测定的药物有( )。
A.对乙酰氨基酚
B.对乙酰氨基酚片
C.对乙酰氨基酚注射液
D.盐酸肾上腺素
E.对乙酰氨基酚栓剂
正确答案:ABCDE
-
第15题:
关于片剂的常规检查叙述错误的是
A、重量差异是片剂的常规检查
B、对于小剂量的药物,需要进行含量均匀度检查
C、崩解时限是片剂的常规检查
D、片重>0.3g时,重量差异限度为10%
E、难溶性的药物,需要进行溶出度测定
参考答案:D
-
第16题:
复方对乙酰氨基酚片中对乙酰氨基酚含量测定法采用
正确答案:A
-
第17题:
属于中国药典在制剂通则中规定的内容为
A.泡腾片的崩解度检查方法
B.栓剂和阴道用片的融变时限标准和检查方法
C.对乙酰氨基酚(扑热息痛)含量测定方法
D.片剂溶出度试验方法
E.控释制剂和缓释制剂的释放度试验方法
正确答案:ABDE
-
第18题:
中国药典对片剂进行溶出度检查,限度(Q)应为标示量的A.95%
B.60%
C.75%
D.90%
E.70%答案:E解析:药典规定。 -
第19题:
己烯雌酚片的含量测定方法如下:取本品20片,精密称定,总重量为2.8050g,研细后,精密称取片粉0.2338g,置50mL量瓶中,加无水乙醇约30mL,置水浴中加热,振摇使溶解,加无水乙醇稀释至刻度,摇匀,滤过,弃初滤液,精密量取续滤液5mL,置50mL量瓶中,加无水乙醇稀释至刻度,摇匀。照分光光度法在241nm波长测定吸收度A=0.609。已知E1%1cm=600,标示量=3mg/片,己烯雌酚的标示量为()%。
正确答案:101.5 -
第20题:
(三)案例摘要:乙酰水杨酸268g,对乙酰氨基酚136g,咖啡因33.4g,淀粉266g,淀粉浆(15%~17%)85g,滑石粉25g(5%),轻质液体石蜡2.5g,酒石酸2.7g,制成1000片。 关于片剂的质量检查,不正确的是()
- A、肠溶衣在人工胃液中不崩解
- B、凡检查溶出度、含量均匀度的片剂不进行崩解时限检查
- C、口服片剂不进行微生物限度检查
- D、分散片、咀嚼片可不作为崩解时限检查
- E、缓释片应进行溶出度检查
正确答案:C,E -
第21题:
单选题关于片剂中药物溶出度,下列哪种说法是正确的?( )A崩解合格的药品一定溶出度合格
B片剂在规定时间内的溶出度应在90%以上
C缓控释制剂至少取样5个时间点
D缓控释制剂最后取样点的累计释放率为标示量的75%以上
E以上均不正确
正确答案: A解析:
A项,对于难溶性药物,崩解度合格不一定能保证药物快速而完全溶解出来;B项,普通片剂应在45分钟内溶出标示量的70%以上;CD两项,对缓控释制剂至少取样3个时间点,即在0.5~2小时内累计释放约30%(考虑突释)、释药50%的时间点、最后取样点的累计释放率为标示量的75%以上(考虑释放是否完全)。 -
第22题:
多选题(三)案例摘要:乙酰水杨酸268g,对乙酰氨基酚136g,咖啡因33.4g,淀粉266g,淀粉浆(15%~17%)85g,滑石粉25g(5%),轻质液体石蜡2.5g,酒石酸2.7g,制成1000片。 关于片剂的质量检查,不正确的是()A肠溶衣在人工胃液中不崩解
B凡检查溶出度、含量均匀度的片剂不进行崩解时限检查
C口服片剂不进行微生物限度检查
D分散片、咀嚼片可不作为崩解时限检查
E缓释片应进行溶出度检查
正确答案: C,A解析: 暂无解析 -
第23题:
判断题对乙酰氨基酚片剂溶出度测定:取标示量为0.3g的本品6片,依法在1000mL溶剂中测定溶出度。经30分钟时,取溶液5mL滤过,精密吸取续滤液1mL,加0.04%氢氧化钠溶液稀释至50mL,摇匀,在257nm波长处测得每片的吸收度分别为0.345,0.348,0.351,0.359,0.356和0.333,按其百分吸收系数为715计算出各片的溶出量。限度为标示量的80%。其溶出度符合规定。A对
B错
正确答案: 对解析: 暂无解析
