9、欲使Ag2CO3(Ksp=8.1×10-12)全部转化为Ag2CrO4(Ksp=1.1×10-12),需要c (CrO42-)/ c (CO32-)> 。(保留2位有效数字)
题目
9、欲使Ag2CO3(Ksp=8.1×10-12)全部转化为Ag2CrO4(Ksp=1.1×10-12),需要c (CrO42-)/ c (CO32-)> 。(保留2位有效数字)
相似考题
更多“9、欲使Ag2CO3(Ksp=8.1×10-12)全部转化为Ag2CrO4(Ksp=1.1×10-12),需要c (CrO42-)/ c (CO32-)> 。(保留2位有效数字)”相关问题
-
第1题:
欲使沉淀溶解,Ksp必需()离子浓度的乘积。A、等于
B、大于
C、小于
D、无确定关系
参考答案:B
-
第2题:
25℃时,AgCl的溶解度为0.192×10-3g,其溶度积常数Ksp=()。(AgCl的摩尔质量为143.4)
- A、1.8×10-6
- B、1.8×10-8
- C、1.8×10-10
- D、1.8×10-12
正确答案:C -
第3题:
在含有Cl-和CrO42-(均为10-3mol·L-1)溶液中逐滴加入AgNO3溶液,哪种离子先沉淀?两者能否分离? (Ksp,AgCl=1.56×10-10KspAg2CrO4=2.0×10-12)
正确答案: (1)沉淀AgCl时,需
[Ag+]=1.56×10-10/10-3=1.56×10-6
沉淀Ag2CrO4时,需
[Ag+]=(2.0×10-12/10-3)1/2=4.5×10-5
因为1.56×10-6<4.5×10-6所以AgCl先沉淀
(2)因为[Cl-]2/[CrO42-]=Ksp,AgCl2/Ksp,Ag2CrO4=1.22×10-8
当[Cl-]=(1.22×10-8×[CrO42-])1/2=3.48×10-6时,
Ag2CrO4才开始沉淀,此时已有
(10-3-3.48×10-6)/10-3×100%=99.7%沉淀
可以分离 -
第4题:
利用生成配合物使难溶电解质溶解时,下面哪种情况最有利于沉淀溶解()。
- A、lgKs愈大,Ksp愈大
- B、lgKs愈小,Ksp愈大
- C、lgKs愈大,Ksp愈小
- D、lgKs愈小,Ksp愈小
正确答案:A -
第5题:
Ag2CrO4的Ksp=2.0×10-12,AgCl的Ksp=1.6×10-10,则Ag2CrO4比AgCl更难溶解于水。
正确答案:错误 -
第6题:
25℃时,Ag2CrO4的Ksp为1.1³10-12则Ag2CrO4在水中的溶解度是()克/升。(Ag2CrO4的分子量为为331.8)
- A、3.3×10-2
- B、2.16×10-2
- C、5.4×10-2
- D、1.3×10-2
正确答案:B -
第7题:
已知Ksp(Ag2CO3=8.1×10-12,则Ag2CO3的溶解度S为多少mol˙L-1?()
- A、1.42×10-4
- B、3.42×10-4
- C、2.85×10-6
- D、2.12×10-6
正确答案:A -
第8题:
同温度下,将下列物质溶于水成饱和溶液,溶解度最大的是()
- A、AgCl(Ksp=1.8×10-18)
- B、Ag2Cr2O4(Ksp=1.1×10-12)
- C、Mg(OH)2(Ksp=1.8×10-10)
- D、Fe3(PO4)2(Ksp=1.3×10-22)
正确答案:C -
第9题:
25℃时Ag2CrO4的KSP=1.1310-12,试求Ag2CrO4在水中的溶解度(克/升)。(Ag2CrO4的分子量:331.8)
正确答案: 在水中的溶解度为2.163克/升。 -
第10题:
Ag+、Pb2+、Ba2+混合溶液中,各离子浓度均为0.10mol/L,往溶液中滴加K2Cr2O7试剂,最先生成的沉淀是(),最后生成的沉淀是()。 设Ni2+、Cd2+两溶液离子浓度相同,若分别通入H2S至饱和,形成()沉淀时介质的酸度可以较大。(Ksp,PbCrO4=1.77×10-14,Ksp,BaCrO4=1.17×10-10,Ksp,Ag2CrO4=9.0×10-12,Ksp,NiS=3×10-21,Ksp,CdS=3.6×10-29)。
正确答案:PbCrO4;Ag2CrO4;CdS -
第11题:
因为Ag2CrO4的溶度积(KSPθ=2.0×10-12)小于AgCl的溶度积(KSPθ=1.6×10-10),所以,Ag2CrO4必定比AgCl更难溶于水。
正确答案:错误 -
第12题:
填空题Ag2CrO4的KSP=2.0×10-20,不考虑任何副反应,则溶解度()。正确答案: S=(2.0×10-20/22)1/3 =1.7×10-7(mol/L)解析: 暂无解析 -
第13题:
已知25℃时AgCl与Ag2CO3的KSP分别为1.77×10-10和8.45×10-12,我们可以得出在室温下( )。A 只要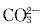 的浓度足够,AgCl(s)可直接转化可为Ag2CO3(s)
的浓度足够,AgCl(s)可直接转化可为Ag2CO3(s)
B AgCl(s)不可能直接转化可为Ag2CO3(s)
C 只要Cl-的浓度足够,Ag2CO3(s)也不可直接转化可为AgCl(s)
D 因无各物质的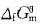 值,故这里不能判断上述反应的方向答案:B解析:
值,故这里不能判断上述反应的方向答案:B解析: ①
①
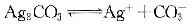 ②
②
 ③
③
对于反应③的平衡常数可由①②求得,其KSP=(1.77×10-10)2/8.45×10-12
△G=-RTlnKSP>0,所以,反应③不会自发进行 -
第14题:
已知ksp,AgCl=1.8×10-10,ksp,Ag2CrO4=2.0×10-12,在Cl-和CrO42+浓度皆为0.10mol/L的溶液中,逐滴加入AgNO3溶液,情况为()。
- A、Ag2CrO4先沉淀
- B、只有Ag2CrO4沉淀
- C、AgCl先沉淀
- D、同时沉淀
正确答案:C -
第15题:
沉淀转化的方向是由Ksp大的转化为Ksp小的。
正确答案:错误 -
第16题:
298K时,Mg(OH)2在水中溶解度(mol·L-1)[已知Mg(OH)2的Ksp为5.61×10-12]是()。
- A、1.77×10-4
- B、1.12×10-4
- C、2.36×10-6
- D、1.12×10-6
正确答案:B -
第17题:
Ag2CrO4饱和溶液的Ksp=()。
- A、[Ag+]·[CrO4-]
- B、[Ag+]2·[CrO-]4
- C、[Ag+]2·[CrO42-]
- D、[Ag+]·[CrO42-]
正确答案:C -
第18题:
氯化银的Ksp=1.8×10-10,Ag2CrO4的Ksp=2.0×10-12,而两个银盐的溶解度S(单位:mol/l)的关系是SAgCl()SAg2CrO4。
正确答案:小于 -
第19题:
已知Kspθ(Ag2CrO4)=1.1×10-12,在0.10mol.L-1Ag+溶液中,要产生Ag2CrO4沉淀,CrO42-的浓度至少应大于()。
- A、1.1×10-10mol.L-1
- B、2.25×10-11mol.L-1
- C、0.10mol.L-1
- D、1×10-11mol.L-1
正确答案:A -
第20题:
已知AgCl和Ag2CrO4的KθSP分别为1.8×10-10,1.1×10-12。若某混合液中,[Cl-]=[CrO42-]=10-5mol.L-1,当加入Ag+达10-4mol.L
时,则会发生() - A、 AgCl先沉淀
- B、只有AgCl沉淀
- C、只有Ag2CrO4沉淀
- D、二者都沉淀
正确答案:B -
第21题:
Ag2CrO4的KSP=2.0×10-20,不考虑任何副反应,则溶解度()。
正确答案:S=(2.0×10-20/22)1/3 =1.7×10-7(mol/L) -
第22题:
Mg(OH)2与MnCO3的KspΘ分别为5.61×10-12和2.2×10-11,在它们的饱和溶液中[Mn2+]比[Mg2+]()。
正确答案:小 -
第23题:
欲使Ag2CO3转化为Ag2C2O4(KspΘ=5.3×10-12),必须使()
- A、[C2O42-]≤0.63[CO32-]
- B、[C2O42-]≥1.6[CO32-]
- C、[C2O42-]<1.6[CO32-]
- D、[C2O42-]<0.63[CO32-]
正确答案:D -
第24题:
问答题25℃时Ag2CrO4的KSP=1.1310-12,试求Ag2CrO4在水中的溶解度(克/升)。(Ag2CrO4的分子量:331.8)正确答案: 在水中的溶解度为2.163克/升。解析: 暂无解析
