已知NH3·H2O的pKb=4.74,则0.10 mol·L-1NH3·H2O溶液的pH为11.13。()
题目
已知NH3·H2O的pKb=4.74,则0.10 mol·L-1NH3·H2O溶液的pH为11.13。()
相似考题
参考答案和解析
更多“已知NH3·H2O的pKb=4.74,则0.10 mol·L-1NH3·H2O溶液的pH为11.13。()”相关问题
-
第1题:
浓度为0.1mol/L的某弱酸弱碱盐NH4A溶液pH=7.00,则HA的pKa为( )。
(已知:NH3·H2O的Kb=1.8×10-5)
求计算过程
答案:
NH4A在质子论当作两性物质 [H+]=约=[Ka(NH4+) *Ka(HA)]^1/2 [H+]^2 =Ka(NH4+)* Ka(HA) 而Ka(NH4+)=Kw/Kb(NH3) 因此 [H+]^2 =Kw/ Kb(NH3)* Ka(HA) (10^-7)^2=10^-14 /Kb(NH3)* Ka(HA) 即:Ka(HA)=Kb(NH3)=1.8*10^-5。
-
第2题:
在含有0.1mol/L NH3·H2O和0.1mol/L NH4Cl的溶液中,已知KbNH3·H2O=1.8×10-5,则H+的离子浓度为( )mol/L。A.134×10~-3
B.556×10~-10
C.946×10~-12
D.180中10~-5答案:B解析:碱性缓冲溶液中 -
第3题:
在0.1mol•L-1的NH3•H2O溶液中,加入一些NH4C1固体,则()
- A、NH3的Kb增大
- B、NH3的Kb减少
- C、溶液pH增大
- D、溶液pH减少
正确答案:D -
第4题:
NH4+的Ka=1×10-9.26,则0.10mol/LNH3水溶液的pH为()。
- A、9.26
- B、11.13
- C、4.74
- D、2.87
正确答案:B -
第5题:
测得0.1mol/L的NH3²H2O溶液的pH=12.0,此溶液的H+浓度为()mol/L。
- A、1.0³10-13
- B、1.0³10-12
- C、1.2³10-12
- D、12
正确答案:B -
第6题:
将50mL0.10mol/LNH3•H2O(已知Kb=1.75×10-5)溶液和20mL0.10mol/LHCl混合后,稀释至100mL,溶液的()。
正确答案:9.42 -
第7题:
如果NH3•H2O的电离常数为1.8*10-5,0.1mol•L-1NH3•H2O溶液中的OH 浓度是多少(mol•L-1)?()
- A、1.8*10-6
- B、1.3*10-3
- C、4.2*10-3
- D、5.0*10-2
- E、1.8*10-4
正确答案:C -
第8题:
将0.400mol/L的NH3·H2O与0.200mol/LHCl等体积混合,在混合后的溶液中加入少量强酸,则溶液的pH将()。
- A、显著降低
- B、显著增加
- C、保持相对稳定
- D、不变
正确答案:C -
第9题:
NH3的pKb=4.74,则NH3--NH4Cl缓冲液pH缓冲范围是()。
正确答案:8.26~10.26 -
第10题:
欲配制pH=9.0的缓冲溶液1.0L,应在500mL0.20mol/LNH3•H2O(pKb=4.75)的溶液 中加入固体NH4Cl(M=53.5g/mol)()g。
正确答案:9.5 -
第11题:
已知HAc的pKa=4.74,则0.1mol/LNaAc溶液的pH=()。
正确答案:8.87 -
第12题:
单选题将0.400mol/L的NH3·H2O与0.200mol/LHCl等体积混合,在混合后的溶液中加入少量强酸,则溶液的pH将()。A显著降低
B显著增加
C保持相对稳定
D不变
正确答案: B解析: 暂无解析 -
第13题:
已知Kθb(NH3·H2O)=1.8×10-5,0.1mol·L-1的NH3·H2O溶液的pH为( )。A、 2.87
B、 11.13
C、 2.37
D、 11.63答案:B解析:根据电离常数求氢氧根离子OH-的溶度有:
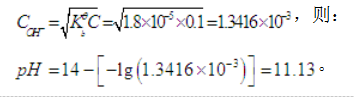
-
第14题:
下列水溶液pH值为3.02的是( )。A.0.010mol·l-1HAc(Ka=1.76×10-5)
B.0.0010mol·l-1NaOH
C.0.050mol·l-1HAc
D.0.1mol·l-1NH3·H2O答案:C解析:{图} -
第15题:
NH3·H2O的pKb=4.75,在20.0mL0.10mol·L-1NH3·H2O溶液中,加入20.0mL0.050mol·L-1HCl,则溶液中的pH为()。
- A、4.75
- B、7
- C、9.25
- D、9.55
正确答案:C -
第16题:
欲配制pH=5的缓冲溶液,应选用下列()共轭酸碱对。
- A、NH2OH2+—NH2OH(NH2OH的pKb=3.38)
- B、HAc—Ac-(HAc的pKa=4.74)
- C、NH4+—NH3•H2O(NH3•H2O的pKb=4.74)
- D、HCOOH—HCOO-(HCOOH的pKa=3.74)
正确答案:B -
第17题:
0.10mol/lHAc溶液(KHAc=1.8×10-5)与0.10mol/lNH3·H2O溶液(KNH3·H2O=1.8×10-5)pH值相同。()
正确答案:错误 -
第18题:
向120mL浓度为0.10mol·L-1的NH3·H2O中加入30mL浓度为0.10mol·L-1的HCl,则混合溶液的PH=()。(已知NH3·H2O的PKθb=4.75)
- A、4.27
- B、9.73
- C、8.77
- D、5.23
正确答案:C -
第19题:
浓度为5.6×10-3 mol·L-1的 NH3·H2O溶液的PH值与浓度为()mol·L-1的NaOH水溶液的PH值相等。(已知NH3·H2O的Kθb=1.8×10-5)
正确答案:3.17×10-4 -
第20题:
用0.2mol/ LHCl溶液滴定0.10mol/L NH3(pKb=4.74)和甲胺(pKb=3.38)的混合溶液时,在滴定曲线上,出现()个滴定突跃。
正确答案:1 -
第21题:
用0.1mol/L的NAOH滴定0.1mol/LHCl与0.1mol/LNH4Cl(NH3•H2O的pKB=4.75)的混合液,化学计量点的pH值为()
- A、4.2
- B、5.3
- C、7.0
- D、8.4
正确答案:B -
第22题:
已知NH3的pKb=4.74,则NH4+>的Ka值为()
正确答案:5.5×10-10 -
第23题:
单选题欲配制pH=9的缓冲溶液,应选用()ANH2OH(羟氨)(pKb=8.04)
BNH3·H2O(pKb=4.74)
CCH3COOH(pKa=4.74)
DHCOOH(pKa=3.74)
正确答案: D解析: 暂无解析 -
第24题:
单选题已知AgBr的=12.30,[Ag(NH3)2]+的=7.40,则AgBr在1.001molL-1NH3溶液中的溶解度(molL-1)为()。A10-4.90
B10-6.15
C0.10-9.85
D10-2.45
正确答案: C解析: 暂无解析
