原子中核外电子排布为1S22S22P63S23P4的元索,位于元素周期的第几周期( )。A、一B、二C、三D、四E、五
题目
原子中核外电子排布为1S22S22P63S23P4的元索,位于元素周期的第几周期( )。
A、一
B、二
C、三
D、四
E、五
相似考题
参考答案和解析
更多“原子中核外电子排布为1S22S22P63S23P4的元索,位于元素周期的第几周期( )。A、一B、二C、三D、四E、 ”相关问题
-
第1题:
30号元素基态原子核外电子排布式为(),该元素属于()周期,()族,()区。参考答案:
-
第2题:
某原子失去2个核外电子后的核外电子排布与Ar原子相同。该原子的元素符号为(),原子序数为()。参考答案: Ca;20。
-
第3题:
氧元素在元素周期表中在第几周期:()
- A、第一周期
- B、第二周期
- C、第三周期
- D、第四周期
正确答案:B -
第4题:
原子中核外电子排布为1S22S22P63S23P4的元索,位于元素周期的第几周期()。
- A、一
- B、二
- C、三
- D、四
- E、五
正确答案:C -
第5题:
原子核外电子排布主要遵循的三个原理是什么?
正确答案:1.能量最低原理;2.泡利不相容原理;3.洪特规则 -
第6题:
元素的性质随着元素原子序数的递增而周期性变化,是由于()引起的。
- A、原子量的递增
- B、原子的核外电子的递增
- C、原子的核外电子排布的周期性变化
- D、原子的质子数发生周期性变化
正确答案:C -
第7题:
已知某副族元素A的原子,电子最后排入3d,最高氧化数为+4;元素B的原子,电子最后排入4p,最高氧化数为+5。回答下列问题: ⑴写出A、B元素原子的核外电子排布式。 ⑵根据核外电子排布式,指出它们在周期表中的位置(周期、族)。
正确答案:⑴A:1s22s22p63s23p63d24s2;B:1s22s22p63s23p63d104s24p3。
⑵A:第四周期ⅣB族;B:第四周期ⅤA族。 -
第8题:
原子序数为17的元素,其原子核外电子排布式为();未成对电子数为1。
正确答案:1s22s22p63s23p5 -
第9题:
写出下列原子或离子的核外电子排布. <1>.Cl-17,Cl- <2>.Fe-26,Fe3+ <3>.Hg-80. 判断上述各元素分别属于第几周期,第几族(主.付)。
正确答案:(1).Cl-17,[Ne]3s23p5,第三周期,ⅦA;Cl-[Ne]3s23p6
(2).Fe-26,[Ar]3d64s2,第四周期,ⅧB;Fe3+[Ar]3d5
(3).Hg-80,[Xe]4f145d106s2,第六周期,ⅡB. -
第10题:
问答题原子序数是10的元素在元素周期表中属第几周期?第几族?是金属元素还是非金属元素?正确答案: 第二周期;第O族;非金属元素。解析: 暂无解析 -
第11题:
单选题关于元素周期律,下列各种说法中,不正确的是()A元素性质随着核外电子周期性的排布而呈周期性的变化
B同一周期的元素的第一电离能随着原子序数的递增,由小到大
C同一周期的元素的原子半径随着原子序数的递增,由大到小
D同一周期的元素的原子电负性随着原子序数的递增,由小到大
E同一周期的元素的主要化合价随着原子序数的递增,由小到大
正确答案: B解析: 暂无解析 -
第12题:
单选题原子中核外电子排布为1S22S22P63S23P4的元索,位于元素周期的第几周期()。A一
B二
C三
D四
E五
正确答案: A解析: 核外电子数为16,该元素是硫,位于元素周期表的第三行,即第三周期。 -
第13题:
请举例说明原子核外电子排布的三个基本原则。正确答案:核外电子排布所遵循的三个规则是:能量最低原理、泡利不相容原理和洪特规则。
1、最低能量原理:
电子可看作是一种物质,也具有同样的性质,即它在一般情况下总想处于一种较为安全(或稳定)的一种状态(基态),也就是能量最低时的状态。当有外加作用时,电子也是可以吸收能量到能量较高的状态(激发态),但是它总有要回到基态的趋势。
2、泡利不相容原理:
在同一个原子中没有也不可能有运动状态完全相同的两个电子存在。
3、洪特规则:
有两方面的含义:一是电子在原子核外排布时,将尽可能分占不同的轨道,且自旋平行;洪特规则的第二个含义是对于同一个电子亚层,当电子排布处于∶全满(s2、p6、d10、f14)半满(s1、p3、d5、f7)。
-
第14题:
下列各种表述中,两个微粒属于同种元素的原子的是( )。
A.3D能级有一个空轨道的基态原子和核外电子排布为1s22s22p63s23p2的原子
B.2p能级有一个未成对电子的基态原子和价电子排布为2s22p5的原子
C.M层全充满而N层4s2的原子和核外电子排布为1s22s22p63s23p63d24s2的原子
D.最外层电子数是核外电子总数的1/5的原子和价电子排布为4s24p3的原子答案:A解析:A项,3p能级有一个空轨道的基态原子的核外电子排布为1s22s22p63s23p2,A项描述的是同种元素的原子;B项,2p能级有一个未成对电子的基态原子的核外价电子排布有两种情况:2s22p1、2s22p5,B项描述的不一定是同种元素的原子:C项.M层全充满而N层为4s:的原子的核外电子排布为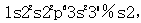 ,c项描述的不是同种元素的原子;D项.最外层电子数是核外电子总数的1/5的原子是Br,其核外电子排布为 )
,c项描述的不是同种元素的原子;D项.最外层电子数是核外电子总数的1/5的原子是Br,其核外电子排布为 )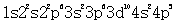 .D项描述的不是同一种元素的原子;故本题选A。
.D项描述的不是同一种元素的原子;故本题选A。 -
第15题:
某元素的原子序数为24它属于第几周期()
- A、第二
- B、第三
- C、第四
- D、第五
正确答案:C -
第16题:
当n=4时,该电子层电子的最大容量为()个;某元素原子在n=4的电子层上只有2个电子,在次外层l=2的轨道中有10个电子,该元素符号是(),位于周期表中第四周期,第()族,其核外电子排布式为()。
正确答案: 32;Zn;ⅡB;1s22s22p63s23p63d104s2 -
第17题:
通过元素周期表,可以知道元素的()。
- A、符号
- B、原子量
- C、电子数
- D、核外电子排布
正确答案:A,B,C -
第18题:
原子序数是10的元素在元素周期表中属第几周期?第几族?是金属元素还是非金属元素?
正确答案:第二周期;第O族;非金属元素。 -
第19题:
在多电子原子中,核外电子排布应遵循的三个原则是:()、()、()
正确答案:保利不相容原理;能量最低原理;洪特规则 -
第20题:
简述原子核外电子排布三原则。
正确答案: 泡利不相容原理、最低能量原理、洪德规则 -
第21题:
某一元素的原子序数为24,试问: (1)核外电子总数是多少? (2)它的电子排布式? (3)价电子层结构; (4)元素所处的周期、族、区?
正确答案: (1)核外电子总数是24
(2)它的电子排布式:1s22s22p63s23p63d54s1
(3)价电子层结构:3d54s1
(4)元素所处的四周期、ⅥB族、d区 -
第22题:
单选题氧元素在元素周期表中在第几周期:()A第一周期
B第二周期
C第三周期
D第四周期
正确答案: A解析: 暂无解析 -
第23题:
单选题某元素的原子序数为24它属于第几周期()A第二
B第三
C第四
D第五
正确答案: C解析: 暂无解析 -
第24题:
单选题原子中核外电子排布为1S22S22P63S23P4的元素,位于元素周期的第几周期()A一
B二
C三
D四
E五
正确答案: C解析: 核外电子数为16,该元素是硫,位于元素周期表的第三行,即第三周期
