如果将 7.16×10-4 mol的 XO(OH)溶液还原到较低价态,需要用 674.5mL 的 0.066 mol.dm-3 的 Na₂ SO₃溶液,那么 X元素的最终氧化态为A.-2B.-1C.0D.+1
题目
如果将 7.16×10-4 mol的 XO(OH)溶液还原到较低价态,需要用 674.5mL 的 0.066 mol.dm-3 的 Na₂ SO₃溶液,那么 X元素的最终氧化态为
A.-2
B.-1
C.0
D.+1
相似考题
参考答案和解析
更多“如果将 7.16×10-4 mol的 XO(OH)溶液还原到较低价态,需要用 674.5mL 的 0.066 mol.dm-3 的 Na₂ SO₃溶液,那么 X元素的最终氧化态为”相关问题
-
第1题:
0.02mol/lAgNO3溶液与同浓度的Na2SO4溶液等体积混合后通过计算是否有沉淀出现(KspAg2SO4=1.4*10-5)()。A.KspAg2SO4=4*10-4有Ag2SO4沉淀出现
B.Qsp=4*10-4有Ag2SO4沉淀出现
C.Qsp=1*10-4有Ag2SO4沉淀出现
D.Qsp=1*10-6没有Ag2SO4沉淀出现
参考答案:D
-
第2题:
Mg(OH)2在( )项中的溶解度最大。A.纯水
B.001mol/kg的MgC.l2溶液
C.001mol/kg的B.A.(OH)2溶液
D.001mol/kg的NA.OH溶液答案:A解析:根据同离子效应,在难溶电解质中,加入与其具有相同离子的强电解质时,将抑制弱电解质的电离 -
第3题:
室温下,下列溶液中的c(OH-)最小的是(??)A.pH=0的溶液
B.0.05 mol·L-1H2SO4溶液
C.0.5 mol·L-1?HCl溶液
D.0.05mol·L-1Ba(OH)2溶液答案:A解析: -
第4题:
已知所含元素化合价发生变化的反应是氧化还原反应,其中被还原的元素化合价降低,被氧化的元素化合价升高。海洋中有丰富的资源,如下图所示利用海水可获得许多化工产品。下列有关说法正确的是 ( ) A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的试剂顺序为:Na2CO3溶液、NaOH溶液、BaCl2溶液,过滤后加盐酸
A.第①步中除去粗盐中的SO42-、Ca2+、Mg2+等杂质,加入的试剂顺序为:Na2CO3溶液、NaOH溶液、BaCl2溶液,过滤后加盐酸
B.第②步中加入的试剂为CaCl2溶液
C.第③步中发生分解反应
D.在第④步中溴元素被还原答案:C解析: -
第5题:
从有关电对的电极电位判断氧化还原反应进行方向的正确方法是崐()。
- A、某电对的还原态可以还原电位比它低的另一电对的氧化态
- B、作为一种氧化剂,它可以氧化电位比它高的还原态
- C、某电对的氧化态可以氧化电位较它低的另一电对的还原态
- D、电对的电位越低,其氧化态的氧化能力越强
正确答案:C -
第6题:
硫代硫酸钠的制备方法为()
- A、将硫粉溶于沸滕的Na2SO4溶液中
- B、将硫粉溶于沸滕的Na2SO3碱性溶液中
- C、用硫酸酸化过的高锰酸钾去氧化Na2SO3
- D、硫化钠与Na2SO3反应
正确答案:B -
第7题:
铁盐检查时,需加入过硫酸铵固体适量的目的在于()
- A、将高价态铁离子(Fe3+)还原为低价态铁离子(Fe2+)
- B、加速Fe3+和SCN的反应速度
- C、增加颜色深度
- D、将低价态铁离子(Fe2+)氧化为高价态铁离子(Fe3+),同时防止硫氰酸铁在光线作用下,发生还原或分解反应而褪色
正确答案:D -
第8题:
NA为阿伏加德罗常数,下列关于0.2mol/LK2SO4溶液的正确说法是()
- A、500mL溶液中所含K+、SO42-总数为0.3NA
- B、500mL溶液中含有0.1NA个K+离子
- C、1L溶液中K+离子浓度是0.2mol/L
- D、2L溶液中SO42-离子浓度是0.4mol/L
正确答案:A -
第9题:
CuSO4溶液和Na2S溶液混合后的产物是()。
- A、Cu(OH)2↓+H2S↑+Na2SO4
- B、CuS↓+Na2SO4
- C、Cu↓+S↓+Na2SO4
- D、以上答案都不对
正确答案:B -
第10题:
两种分子酸HX溶液和HY溶液有相同的pH,则这两种酸的浓度(mol.dm-3)相同。
正确答案:错误 -
第11题:
二苯胺磺酸钠是氧化还原指示剂,其氧化态是紫色,还原态是无色。在指示终点过程中消耗滴定剂溶液,因此往往要()。
正确答案:定量加入 -
第12题:
20cm3Fe(OH)3溶液中加入5×10-3mol•cm-3Na2SO4溶液12.5cm3使其聚沉,则Na2SO4对Fe(OH)3溶液的聚沉值为()(mol•dm-3)。
- A、1.92
- B、3.125
- C、3.84
- D、6.25
正确答案:A -
第13题:
电解Na2SO4水溶液时,阳极上放电的离子是( )。A、 H+
B、 OH-
C、 Na+
D、 SO2-4答案:B解析:Na2SO4水溶液的电解实际上是电解水,阳极:
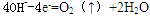
阴极:

Na+、SO42-均不参与放电。 -
第14题:
室温下,下列溶液中的C(OH-)最小的是( )A.pH=0的溶液
B.5 mol/L HCl溶液
C.05 mol/L H2SO4溶液
D.05 mol/L Ba(OH)2溶液答案:A解析:室温下,即c(H+)·c(OH-)=1×10-14(mol/L)2.由此,c(H+)和c(OH-)只要知道其中一个即可求得另一个. A选项为pH=0的溶液,即c(H+)=1 mol/L,所以c(OH-)=1×10-14 mol/L.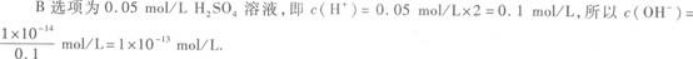
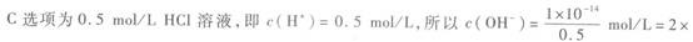
D选项为0.05 mol/L Ba(OH)2溶液,c(OH-)=0.05 mol/L×2=0.1 mol/L.
所以,c(OH-)最小的是1×10-14 mol/L,即A选项. -
第15题:
将0.1 mol/L的NaOH溶液20 mL与0.2 mol/L的CH3COOH溶液10 mL混合.混合后的溶液中,有关离子浓度间的关系正确的是( )A.C(Na+)>c(OH-)>c(H+)>c(CH3COO-)
B.C(Na+)>c(OH-)>c(CH3COO-)>c(H+)
C.C(Na+)>c(CH3COO-)>c(H+)>c(OH-)
D.C(Na+)>c(CH3COO-)>c(OH-)>c(H+)答案:D解析:【解题指要】 溶液中含有NaOH和CH3COOH的物质的量分别为
等物质的量的NaOH与CH3COOH恰好完全反应:
所以混合后的溶液可以看做是CH3COONa溶液,在此溶液中的离子有
若不考虑水解,则有c(Na+)=c(CH3COO-);c(H+)=c(OH-).但事实是CH3COO-会发生水解:
由于水解反应消耗了CH3COO-且生成了OH-,所以c(Na+)>c(CH3COO-);C(OH-)>c(H+).由于水解程度一般都很低,所以c(CH3COO-)>c(OH-).
即:c(Na+)>c(CH3COO-)>c(OH-)>c(H+). -
第16题:
检查铁盐时,需加入过硫酸铵固体适量的目的在于A.增加颜色深度
B.将低价态铁离子(Fe )氧化为高价态铁离子(Fe
)氧化为高价态铁离子(Fe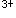 ),同时防止硫氰酸铁在光线作用下,发生还原或分解反应而褪色
),同时防止硫氰酸铁在光线作用下,发生还原或分解反应而褪色
C.将高价态铁离子(Fe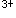 )还原为低价态铁离子(Fe
)还原为低价态铁离子(Fe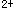 )
)
D.消除干扰
E.加速Fe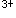 和SCN的反应速度答案:B解析:
和SCN的反应速度答案:B解析: -
第17题:
NA为阿伏加德罗常数,下列对0.3mol/L的22SO4溶液的说法中,正确的是()
- A、1L溶液中含0.3NA个钾离子
- B、1L溶液中含0.9NA个离子(K+、SO42-)
- C、2L溶液中钾离子浓度是1.2mol/L
- D、2L溶液中含0.6NA个离子(K+、SO42-)
正确答案:B -
第18题:
元素在化合物中的氧化态代表了它在氧化还原反应中所处的状态,氧化态越高,氧化能力越强
正确答案:错误 -
第19题:
0.10 mol.dm-3 HAc溶液中c(H+)=1.3*10-3mol.dm-3,故0.050 mol.dm-3 HAc溶液中c(H+)=0.65*10-3 mol.dm-3。
正确答案:错误 -
第20题:
从有关电对的电极电位判断氧化还原反应进行方向的正确方法是()。
- A、某电对的还原态可以还原电位比它低的另一电对的氧化态
- B、电对的电极电位越低,是氧化态的氧化能力越强
- C、某电对的氧化态可以氧化电极电位较它低的另一电对的还原态
- D、电对的电极电位越高,其还原态的还原能力越强
- E、作为一种氧化剂,它可以氧化电极电位比它高的还原剂
正确答案:C -
第21题:
所谓歧化反应,就是()
- A、某一元素自身发生的反应
- B、某一化合物内元素发生的氧化还原反应
- C、某一元素的自氧化还原反应
- D、同一元素的同一氧化态氧化还原成不同氧化态的反应
正确答案:D -
第22题:
检查铁盐时,需加入过硫酸铵固体适量的目的在于()
- A、消除干扰
- B、加速Fe3+和SCN的反应速度
- C、增加颜色深度
- D、将低价态铁离子(FE2+.氧化为高价态铁离子(FE3+.,同时防止硫氰酸铁在光线作用下,发生还原或分解反应而褪色
- E、将高价态铁离子(FE3+.还原为低价态铁离子(FE2+.
正确答案:D -
第23题:
KMnO4溶液作为氧化剂,在不同介质中可被还原至不同价态,在酸性介质中还原时,其基本*单位为()。
正确答案:1/5KMnO4 -
第24题:
填空题二苯胺磺酸钠是氧化还原指示剂,其氧化态是紫色,还原态是无色。在指示终点过程中消耗滴定剂溶液,因此往往要()。正确答案: 定量加入解析: 暂无解析
