把NaAc晶体加到0.1mol/L HAc溶液中,将会有下列中哪种变化? A.溶液pH值升髙 B.溶液pH值下降 C. Ka增加 D. Ka减小
题目
B.溶液pH值下降
C. Ka增加
D. Ka减小
相似考题
更多“把NaAc晶体加到0.1mol/L HAc溶液中,将会有下列中哪种变化? A.溶液pH值升髙 B.溶液pH值下降 C. Ka增加 D. Ka减小”相关问题
-
第1题:
某弱酸HAc的Ka=1(×)10-5,则其0.1mol/L溶液的PH值为:()?
A.1.0
B.2.0
C.3.0
D.3.5
E.5.0
答案:C
解析:因为是弱酸,所以HAc电离能力很弱,HAc浓度近似等于0.1mol/L,由Ka=【H+】*【Ac-】/【HAc】,【H+】和【Ac-】近似相等,可得【H+】=10-3,PH=-lg(氢离子浓度)所以PH值=3 -
第2题:
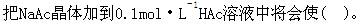 A.溶液的pH值降低
A.溶液的pH值降低
B.Ka,HAc增加
C.溶液的pH值升高
D.Ka,HAc减小答案:C解析:
-
第3题:
将0.1mol/L的HAc与0.1mol/L的NaAc混合溶液中加水稀释至原的体积的2倍,其H+浓度和pH值变化为( )。A.原来的1/2倍和增大
B.原来的1/2倍和减小
C.减小和增大
D.不变和不变答案:D解析:HAc与NaAc组成缓冲溶液,根据缓冲溶液pH值的计算公式,因此HAc与NaAc浓度降低相同倍数,pH值不变。 -
第4题:
在HAc-NaAc的混合液中,HAc和NaAc的浓度都为0.1mol/L,HAc的Ka=1.8×10-5。此缓冲溶液的pH值为()。
A4.74
B7.56
C8.86
D9.26
A
略 -
第5题:
求0.1mol/LHAc溶液的PH值(Ka=1.8×10-5)。
正确答案: [H+]=LmolCKa/1034.11.0108.1)(35−−×=××=⋅酸pH=-lg[H+]=-lg(1.34×10-3)=3-lg1.34=2.87
0.1mol/LHAc溶液的pH值为2.87。 -
第6题:
1L溶液中HAc的溶度为1.0mol/L,NaAc的浓度为0.1mol/L,则该溶液的PH值为()HAc的pKa=4.74。
- A、2.74
- B、3.74
- C、4.74
- D、5.74
正确答案:B -
第7题:
向1.0L0.10mol·L-1HAc溶液中加入1.0mL0.010mol·L-1HCl溶液,下列叙述正确的是()。
- A、HAc解离度减小
- B、溶液的pH为3.02
- C、KaΘ(HAc)减小
- D、溶液的pH为2.30
正确答案:A -
第8题:
把醋酸钠晶体加到1升0.1mol•L-1的醋酸溶液中将会产生:()
- A、K°平衡值增加
- B、K°平衡值减小
- C、pH值增加
- D、[Na+]浓度增加
- E、[Na+]浓度不变
正确答案:C -
第9题:
把NaAc晶体加到0.1mol/LHAc溶液中,将会有下列中哪种变化?()
- A、溶液pH值升高
- B、溶液pH值下降
- C、K增加
- D、K减小
正确答案:A -
第10题:
在0.1mol/L的HAc溶液中加入少量的固体NaAc时,HAc的电离度将(),溶液的pH将()。
正确答案:减小;增大 -
第11题:
已知Kaθ(HAc)=1.75×10-5,用0.025mol.L-1HAc溶液和等体积0.050mol.L-1NaAc溶液配制的缓冲溶液,其pH=(),在该溶液中加入很少量HCl溶液,其pH值将()。
正确答案:5.06;基本不变 -
第12题:
单选题把NaAc晶体加到0.1mol/LHAc溶液中,将会有下列中哪种变化?()A溶液pH值升高
B溶液pH值下降
CK增加
DK减小
正确答案: B解析: 暂无解析 -
第13题:
为使HAc溶液的电离度和溶液的pH都增加,往HAc溶液中加的物质应是下列中哪一种?A. NaAc 晶体
B. NaOH 晶体
C. HCl(g)
D. NaCl 晶体答案:B解析:提示:在HAc溶液中存在: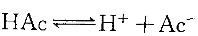 。为使电离度增加,必须使平衡向右移动;为使pH值增加,必须使H+离子浓度下降。
。为使电离度增加,必须使平衡向右移动;为使pH值增加,必须使H+离子浓度下降。 -
第14题:
常温下,往1.0L0.10mol/LHAc溶液中加入一些NaAc晶体并使之溶解,可能发生的变化是( )。A.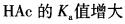
B.
C.溶液的pH值增大
D.溶液的pH值减小答案:C解析: -
第15题:
把NaAc晶体加到0.1mol/L HAc溶液中,将会有下列中哪种变化?A.溶液pH值升髙
B.溶液pH值下降
C. Ka增加
D. Ka减小答案:A解析:提示:Ka只与温度有关。HAc溶液中加入NaAc使HAc的电离平衡向左移动,
-
第16题:
0.1mol/l的HCl溶液和0.1mol/l的HAc(Ka=1.8×10-5),溶液等体积混合后,pH值为()。
- A、1.0
- B、2.0
- C、1.3
- D、1.5
正确答案:C -
第17题:
0.1mol/LHAc溶液的PH值(Ka=1.8×10-5)。
正确答案: 根据弱酸[H+]的计算公式:
[H+]=Ka?C酸=1.8×10-5×0.1=1.34×10-3
PH=-lg[H+]=-lg1.34×10-3=3-lg1.34=2.87 -
第18题:
在0.06mol˙kg-1的HAc溶液中,加入NaAc晶体,使其浓度达0.2mol˙kg-1后,若KaΘ(HAc)=1.8pH×105,则溶液的pH值应多少?()
- A、5.27
- B、44
- C、5.94
- D、7.30
正确答案:C -
第19题:
往lL0.10mol˙L-1HAc溶液中加入一些NaAc晶体并使之溶解,会发生的情况是怎样的?()
- A、HAc的值增大
- B、HAc的值减小
- C、溶液的pH增大
- D、溶液的pH减小
正确答案:B,C -
第20题:
往1升0.01MHAc溶液中,加入一些NaAc晶体,会使溶液的pH值()。
- A、减小
- B、增大
- C、不变
- D、等于2
正确答案:B -
第21题:
把NaAc晶体加到0.1mol/LHAc溶液中,将会有下列中哪种变化?()
- A、溶液pH值升高
- B、溶液pH值下降
- C、Ka增加
- D、Ka减小
正确答案:A -
第22题:
含0.100mol·L-1HAc(Ka=1.8×10-5)-0.0020mol·L-1NaAc溶液的pH值()。
正确答案:3.17 -
第23题:
单选题把NaAc晶体加到0.1mol·L-1溶液中将会使()。A溶液的pH值降低
B增加
C溶液的pH值升高
D减小
正确答案: A解析: 暂无解析 -
第24题:
单选题在HAc-NaAc的混合液中,HAc和NaAc的浓度都为0.1mol/L,HAc的Ka=1.8×10-5。此缓冲溶液的pH值为()。A4.74
B7.56
C8.86
D9.26
正确答案: B解析: 暂无解析
