某元素原子基态的电子构型为[Ar]3d84s2,它在元素周期表中的位置是A.s区B.p区C.d区D.f区
题目
某元素原子基态的电子构型为[Ar]3d84s2,它在元素周期表中的位置是
A.s区
B.p区
C.d区
D.f区
相似考题
更多“某元素原子基态的电子构型为[Ar]3d84s2,它在元素周期表中的位置是”相关问题
-
第1题:
某原子序数为15的元素,其基态原子的核外电子分布中,未成对电子数是( )。A、0
B、1
C、2
D、3答案:D解析:正确书写核外电子分布式,可先根据三个分布规则和近似能级顺序将电子依次填入相应轨道,再按电子层顺序整理一下分布式,按n由小到大自左向右排列各原子轨道,相同电子层的轨道排在一起。原子序数为15的元素基态原子的核外电子分布为:
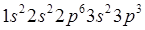
未成对电子数是3。 -
第2题:
在元素周期表中,价层电子构型为ns2np3的元素有(),(),(),(),(),称为()元素;价层电子构型为(n1)d10ns2np6的元素有(),(),(),这类元索属于()。
正确答案:N;P;As;Sb;Bi;氮族(VA族);Kr;Xe;Rn;稀有气体(或0族) -
第3题:
某元素的价电子为4s24p4,问:它的最外层、次外层的电子数;它的可能氧化态,它在周期表中的位置(周期、族、区),它的基态原子的未成对电子数,它的氢化物的立体结构。
正确答案: 最外层6个电子,次外层18个电子(3s23p63d10):其可能的氧化态是-2、+4、+6;它位于第四周期、VIA族、p区;其基态原子的未成对电子数为2;氢化物的立体结构是V型。 -
第4题:
某元素基态原子最外层为5s2,最高氧化态为+4,它位于周期表哪个区?是第几周期第几族元素?写出它的+4氧化态离子的电子构型。若用A代替它的元素符号,写出相应氧化物的化学式。
正确答案: 它位于d区,第五周期IVB族。+4氧化态离子的电子构型为[Kr],即1s22s22p63s23p63d104s24p6;其相应氧化物为AO2。 -
第5题:
已知某副族元素A的原子,电子最后排入3d,最高氧化数为+4;元素B的原子,电子最后排入4p,最高氧化数为+5。回答下列问题: ⑴写出A、B元素原子的核外电子排布式。 ⑵根据核外电子排布式,指出它们在周期表中的位置(周期、族)。
正确答案:⑴A:1s22s22p63s23p63d24s2;B:1s22s22p63s23p63d104s24p3。
⑵A:第四周期ⅣB族;B:第四周期ⅤA族。 -
第6题:
某元素的二价阳离子核外有24个电子,该元素原子的外层电子构型是()。
正确答案:3d64S2 -
第7题:
某元素的原子序数为20,其外层电子构型是(),位于周期表S区、II主族。
正确答案:4S2 -
第8题:
某元素基态原子外层电子构型为n=4, l=0的轨道上有两个电子,n=3,l=2的轨道上有7个电子,该元素的电子结构式(),属于()周期()族的元素。
正确答案:1s22s22p63s63p63d74s7;四;Ⅷ -
第9题:
不查周期表,分别写出下列元素在周期表中的位置(周期、族、区),元素符号及名称。 ⑴Z=47; ⑵基态原子中有3d6电子; ⑶基态原子中有两个未成对的3d电子; ⑷基态原子的电子构型为[Kr]4d45s1; ⑸基态原子的外层电子组态为3d14s2。
正确答案: (1)银,Ag,第五周期,第IB族;
(2)铁,Fe,第四周期,第VIII族;
(3)钛,Ti,第四周期,第IVB族或镍,Ni,第四周期,第VIII族;
(4)铌,Nb,第五周期,第VB族;
(5)钪,Sc,第四周期,第IIIB族。 -
第10题:
元素周期表是元素周期律的具体表现形式,是我们学习化学的工具。元素在周期表中的位置,反映了元素的原子结构和元素的性质。我们可以根据元素在周期表中的位置推测其原子结构和性质,也可以根据元素的原子结构推测它在周期表中的位置。请回答下列问题:(1)有人说“氦的最外层电子数为2,应该把它放在第ⅡA族”,你认为这样编排元素周期表有何利弊?(2)结合化学教学实践,论述三序结合的原则在化学教材编写中“原子结构和元素周期表”理论部分的应用。
正确答案: (1)利:符合同族元素最外层电子数相等的规律等。弊:与同族其他元素性质相差悬殊等。(2)依据三序结合的原则,理论前部分为卤族元素,采用了由个别到一般,由个性到共性的归纳方式,符合高一学生的认知和心理发展过程和知识体系;理论后部分为氧族元素、氮族元素,采用了一般到个别,共性到个性的演绎方式,符合高一后半学期学生的心理发展,已经具有了一定的抽象逻辑思维能力。发挥理论的指导作用,培养学生的能力,有利于个体发展。 -
第11题:
请问下列所问是什么元素? (1)某元素+2价离子和Ar的电子构型相同; (2)某元素的+3价离子和F-的电子构型相同; (3)某元素的+2价离子的3d电子数为7个
正确答案:(1)Ca
(2)Al
(3)Co -
第12题:
问答题元素周期表是元素周期律的具体表现形式,是我们学习化学的工具。元素在周期表中的位置,反映了元素的原子结构和元素的性质。我们可以根据元素在周期表中的位置推测其原子结构和性质,也可以根据元素的原子结构推测它在周期表中的位置。请回答下列问题:(1)有人说“氦的最外层电子数为2,应该把它放在第ⅡA族”,你认为这样编排元素周期表有何利弊?(2)结合化学教学实践,论述三序结合的原则在化学教材编写中“原子结构和元素周期表”理论部分的应用。正确答案: (1)利:符合同族元素最外层电子数相等的规律等。弊:与同族其他元素性质相差悬殊等。(2)依据三序结合的原则,理论前部分为卤族元素,采用了由个别到一般,由个性到共性的归纳方式,符合高一学生的认知和心理发展过程和知识体系;理论后部分为氧族元素、氮族元素,采用了一般到个别,共性到个性的演绎方式,符合高一后半学期学生的心理发展,已经具有了一定的抽象逻辑思维能力。发挥理论的指导作用,培养学生的能力,有利于个体发展。解析: 暂无解析 -
第13题:
47号元素Ag的基态价层电子结构为4d105S1,它在周期表中的位置是:
A. ds 区 B. s 区 C. d 区 D. P 区答案:A解析:提示:Ag为IB元素,为ds区。 -
第14题:
已知某元素+2价离子的核外电子排布式为:[Ar]3d5,该元素在周期表中处于()周期、()族、()区,元素符号是()。
正确答案:第四;ⅦB;d;Mn -
第15题:
某元素的基态价层电子构型为5d66s2,请给出比该元素的原子序数小4的元素的基态原子电子组态。
正确答案: 按构造原理,该元素的基态电子组态为[Xe]4f145d24s2。 -
第16题:
若某基态原子的外围电子排布为4d15s2,则下列说法正确的是()
- A、该元素基态原子中共有3个电子
- B、该元素原子核外有5个电子层
- C、该元素原子最外层共有3个电子
- D、该元素原子M能层共有8个电子
正确答案:B -
第17题:
某元素的原子序数为26,其外层电子构型是(),位于周期表d区、Ⅷ族。
正确答案:3d64S2 -
第18题:
某元素原子主量子数n为4的电子层上有7个电子,该元素原子外层电子构型是(),未成对电子数为(),原子核外电子分布式为(),该元素原子序数是(),它位于第()周期,第()族,最高氧化数()。
正确答案:4s24p5;1;1s22s22p63s23p63d104s24p5;35;四;ⅦA;+7 -
第19题:
原子中电子排布为[Ar]3d24s2的元素,其最高氧化价为(),它在周期表中的位置是()族。
正确答案:+4;ⅣB -
第20题:
某元素的原子序数为26,其外层电子构型是(),位于周期表()区、()族。
正确答案:3d64S2;d;Ⅷ -
第21题:
某高中学生学习了元素周期律后,能够根据某元素的原子结构推测它在元素周期表中的位置及性质,这种方法称为()。
- A、归纳法
- B、类比法
- C、演绎法
- D、分类法
正确答案:C -
第22题:
(2007)47号元素Ag的基态价层电子结构为4d105s1,它在周期表中的位置是:()
- A、ds区
- B、s区
- C、d区
- D、p区
正确答案:A -
第23题:
单选题某元素的价电子构型为ns2np4,此元素在周期表中的位置是()。AIIA族
BVIA族
CVIB族
DIVA族
正确答案: A解析: 暂无解析 -
第24题:
单选题47号元素Ag的基态价层电子结构为4d105s1,它在周期表中的位置是( )。Ads区
Bs区
Cd区
Dp区
正确答案: D解析:
Ag是47号元素,可推知属于IB族,由电子填充情况查表可知,ds区:包括ⅠB、ⅡB族元素,外层电子构型为(n-1)d10ns1和(n-1)d10ns2。其中第5周期最高主量子数n=5。因此在ds区。
