某原电池符号为:,向AgN03溶液中通入H2S气体,使Ag+生成Ag2S沉淀,这时原电池的电动势将( )。A.增大 B.减小C.不变D.不能确定
题目
 ,向AgN03溶液中通入H2S气体,使Ag+生成Ag2S沉淀,这时原电池的电动势将( )。
,向AgN03溶液中通入H2S气体,使Ag+生成Ag2S沉淀,这时原电池的电动势将( )。
B.减小
C.不变
D.不能确定
相似考题
更多“某原电池符号为:,向AgN03溶液中通入H2S气体,使Ag+生成Ag2S沉淀,这时原电池的电动势将( )。 ”相关问题
-
第1题:
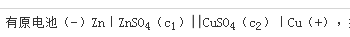
如向铜半电池中通入硫化氢,则原电池电动势变化趋势是( )。A、 变大
B、 变小
C、 不变
D、 无法判断答案:B解析:
-
第2题:
在铜锌原电池的铜电极一端的电解质溶液中加入氨水后,其电动势将( )。
A.减小 B.增大 C.不变 D.无法判断答案:A解析:提示:加入氨水后,由于铜离子形成铜氨配离子,铜电对(作正极〉的电极电势下降,电动势减少。 -
第3题:
将H2S气体通入Hg2(NO3)2溶液中,得到的沉淀物质是()
- A、Hg2S
- B、Hg
- C、HgS+ Hg
- D、HgS
正确答案:C -
第4题:
在标准条件下将氧化还原反应Fe2++Ag+Fe3++Ag装配成原电池,原电池符号为()
- A、(-)Fe2+|Fe3+‖Ag+½Ag(+)
- B、(-)Ag|Ag+‖Fe3+½Fe2+(+)
- C、(-)Pt|Fe2+,Fe3+‖Ag+½Ag(+)
- D、(-)Ag|Ag+‖Fe2+,Fe3+½Pt(+)
正确答案:C -
第5题:
已知φθAg+/Ag=0.80V,φθZn2+/Zn=-0.76V。将两电对组成原电池,该原电池的标准电动势为()
- A、2.36V
- B、0.04V
- C、0.84V
- D、1.56V
正确答案:D -
第6题:
金属M与过量Cl2一起加热,生成液态化合物A,反之若金属M过量则生成固态化合物B.B的盐酸水溶液可将Hg2+还原成Hg+或进一步还原成汞.也可将Fe3+还体原成Fe2+并且当向B的酸性溶液中通入H2S气体时,生成暗棕色沉淀C,C不溶于Na2S或(NH4)2S溶液,若往A的盐酸溶液中通入H2S,生成黄色沉淀D,D溶于(NH4)2
正确答案:MSn、A:SnCl4、B:SnCl2
DSnS2、E://(NH4)2SnS3
Sn+2Cl2(过量)=SnCl4
Sn(过量)+Cl2=SnCl2
4Cl-+SnCl2+2Hg2++2HCl=Hg2Cl2+H2SnCl6
2Cl-+SnCl2+Hg2++2HCl=2Hg+H2SnCl6
2Cl-+2Fe3++SnCl2=2Fe2++SnCl4
SnCl2+H2S=2HCl+SnS↓
SnCl4+2H2S=SnS2+4HCl
SnS2+(NH4)2S=(NH4)2SnS3 -
第7题:
某无色晶体,易溶于水.在水溶液中通入H2S气体有黑色沉淀生成,沉淀与H2O2作用转变为白色,该物质是()
- A、SnCl2
- B、SnCl4
- C、PbCl2
- D、Pb(NO3)2
正确答案:D -
第8题:
向原电池(一)Ag,AgCl│Cl-‖Ag+│Ag(+)的负极中加入NaCl,则原电池电动势的变化是:()
- A、变大
- B、变小
- C、不变
- D、不能确定
正确答案:A -
第9题:
(2013)向原电池(一)Ag,AgCl│Cl-‖Ag+│Ag(+)的负极中加入NaCl,则原电池电动势的变化是:()
- A、变大
- B、变小
- C、不变
- D、不能确定
正确答案:A -
第10题:
单选题(2013)向原电池(一)Ag,AgCl│Cl-‖Ag+│Ag(+)的负极中加入NaCl,则原电池电动势的变化是:()A变大
B变小
C不变
D不能确定
正确答案: D解析: 暂无解析 -
第11题:
单选题在铜锌原电池的铜电极一端的电解质溶液中加入氨水后,其电动势将()。A减小
B增大
C不变
D无法判断
正确答案: D解析: 暂无解析 -
第12题:
单选题向原电池(-)Ag,AgCl|Cl-‖Ag+|Ag(+)的负极中加入NaCl,则原电池电动势的变化是( )。[2013年真题]A变大
B变小
C不变
D不能确定
正确答案: D解析:
原电池发生氧化还原反应,负极为:Ag-e-+Cl-=AgCl,正极为:Ag++e-=Ag。根据电极电势的能斯特方程式,有φ=φϴ+0.059lg[1/c(Cl-)]。由于负极中加入NaCl,Cl-浓度增加,则负极电极电势减小,正极电极电势不变,所以原电池的电动势E=φ正-φ负增大。 -
第13题:
向原电池(-)Ag,AgCl Cl- Ag+ Ag(+)的负极中加入NaCl,则原电池电动势的变化是:A.变大
B.变小
C.不变
D.不能确定答案:A解析:提示 负极氧化反应:Ag+Cl- =AgCl+e
正极还原反应:Ag++e=Ag
电池反应为:Ag++Cl-=AgCl
原电池负极能斯特方程式为: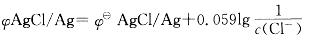
由于负极中加入NaCl,Cl-浓度增加,则负极电极电势减小,正极电极电势不变,
则电池的电动势增大。 -
第14题:
把氧化还原反应Zn+2Ag+Zn2++2Ag组成原电池,欲使该原电池的电动势增大,可采取的措施是()
- A、降低Zn2+浓度
- B、降低Ag+浓度
- C、增加Zn2+浓度
- D、加大Ag电极的表面积
正确答案:A -
第15题:
Ag+在适量的氨水中生成()。
- A、无色溶液
- B、无色无味气体
- C、白色沉淀
- D、褐色沉淀
正确答案:D -
第16题:
在0.001mol·L-1ZnCl2溶液中通入H2S气体达到饱和,如果以盐酸调整酸度,使ZnS生成沉淀,溶液的氢离子浓度应控制在什么范围?(Ksp(ZnS)=1.2×10-23,KH2S=K1×K2=1.0×10-22)
正确答案:H2S的饱和溶液[H2S]=0.1mol·L-1
ZnS开始沉淀的S2-的最低浓度为:
[S2-]=Ksp(ZnS)/[Zn2+]=1.2×10-23/10-3=1.2×10-2mol·L-1
将[S2-]代入KH2S=[H+][S2-]/[H2S],求[H+]
[H+]=0.029mol·L-1
使Zn2+完全沉淀的S2-浓度为[S2-]=1.2×10-23/10-5=1.2×10-18mol·L-1
[H+]=0.0029mol·L-1 -
第17题:
在ZnSO4溶液中通入H2S气体只出现少量的白色沉淀,但若在通入H2S之前,加入适量固体NaAc则可形成大量的沉淀,为什么?
正确答案: 由于 Zn2++ H2S ━━ ZnS + 2H+溶液酸度增大,使ZnS沉淀生成受到抑制,
若通H2S之前,先加适量固体NaAc,则溶液呈碱性,再通入H2S时生成的H+被OH-中和,溶液的酸度减小, 则有利于ZnS的生成. -
第18题:
在铜锌原电池的铜电极一端的电解质溶液中加入氨水后,其电动势将()。
- A、减小
- B、增大
- C、不变
- D、无法判断
正确答案:A -
第19题:
向原电池(-)Zn|Zn2+(1mol·L-1)||Cu2+(1mol·L-1)|Cu(+)的正极溶液中通入H2S气体,则原电池的电动势()
- A、增加
- B、减小
- C、不变
- D、无法判断
正确答案:B -
第20题:
在铜锌原电池中,往CuSO4溶液中加入氨水,电池电动势将有何变化?()
- A、变大
- B、不变
- C、变小
- D、无法确定
正确答案:C -
第21题:
在铜锌原电池中,往CuSO溶液中加入氨水,电池电动势将有何变化?()
- A、变大
- B、不变
- C、变小
- D、无法确定
正确答案:C -
第22题:
单选题往含有FeSO4、Fe2(SO4)3、CuSO4的混合溶液中通入H2S气体后,有沉淀生成,该沉淀是( ).AFeS和CuS
BFe2S3和CuS
CCuS
DCuS和S
正确答案: C解析:
Fe3+具有氧化性,会将S2-氧化为单质S,H2S可与Cu2+反应生成CuS的沉淀,FeS溶于酸. -
第23题:
单选题在铜锌原电池中,往CuSO4溶液中加入氨水,电池电动势将有何变化?()A变大
B不变
C变小
D无法确定
正确答案: A解析: 暂无解析
