常温、常压下,将1 mol蔗糖溶解在水中制成1 L溶液。此溶解过程中体系的ΔH-TΔS和熵的变化情况是( )A.ΔH-TΔS>0,ΔSB.ΔH-TΔS0 C.ΔH-TΔS>0,ΔS>0 D.ΔH-TΔS
题目
B.ΔH-TΔS<0,ΔS>0
C.ΔH-TΔS>0,ΔS>0
D.ΔH-TΔS<0,ΔS<0
相似考题
更多“常温、常压下,将1 mol蔗糖溶解在水中制成1 L溶液。此溶解过程中体系的ΔH-TΔS和熵的变化情况是( )”相关问题
-
第1题:
设 AgCl 在水中、在0. 01mol/L NaCl 溶液中、在0. 01mol/L MgCl2 溶液中、在0. 01mol/L AgNO3溶液中的溶解度分别为S0、S1、S2、S3。下列式子中正确的是?
A. S0>S3>S2>S1 B. S0>S1=S3>S2
C. S0>S1>S2>S3 D. S0>S1=S2=S3答案:B解析:提示:AgCl在NaCl、MgCl2、AgNO3溶液中均存在同离子效应,使溶解度下降,而0. 01mol/L的MgCl2溶液中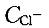 为0. 02mol/L,故溶解度下降更多。
为0. 02mol/L,故溶解度下降更多。 -
第2题:
常温、常压下,将1 mol蔗糖溶解在水中制成1 L溶液。此溶解过程中体系的ΔH-TΔS和熵的变化情况是( )A.ΔH-TΔS>0,ΔS<0
B.ΔH-TΔS<0,ΔS>0 ? ? ? ?
C.ΔH-TΔS>0,ΔS>0
D.ΔH-TΔS<0,ΔS<0?答案:A解析:由焓判据和熵判据组成的复合判据适合于所有过程,该条件下,蔗糖溶于水能够自发进行,故ΔH-TΔS<0;蔗糖分子由规则的晶体状态变为能自由移动的“无序”状态,为熵增加的过程。 -
第3题:
AgCl在水中,0.01mol/L CaCl2 溶液中,0.01mol/L NaCl溶液,0.05mol/L AgNO3 溶液中的溶解度分别为S0、S1、S2、S3,那么下列哪种排列是正确的( )。
A. S0>S1>S2>S3 B. S0>S2>S1>S3 C. S0>S1>S2=S3 D. S0>S2>S3>S1答案:B解析:提示:据同离子效应,同离子浓度越大,溶解度越低。 -
第4题:
在含有AgCl(S)的饱和溶液中加入0.1mol·L-1的AgNO3,AgCl的溶解度将(),这是由于()的结果
正确答案:降低(或减小);同离子效应 -
第5题:
PbI2在水中的溶解度为1.2×10-3mol·L-1,其Kθsp=()若将PbI2溶于0.01 mol·L-1KI溶液,其溶解度为()mol·L-1。
正确答案:6.9×10-9;S=6.9×10-5 -
第6题:
PbI2在水中的溶解度为1.2×10-3mol.L-1,其KθSP=(),PbI2溶于0.01mol.L-1KI溶液,其溶解度为()mol.L-1。
正确答案:6.9×10-9;6.9×10-5 -
第7题:
已知Ag2CrO4固体在水中的溶解度为1.20×10-3mol·L-1,则Ag2CrO4在0.01 mol·L-1的K2CrO4溶液中的溶解度为()mol·L-1。
正确答案:8.31×10-4 -
第8题:
25℃时,NaCl在水中的溶解度为6mol·L-1。若在1L水中加入5mol的NaCl,则溶解过程为()。
- A、ΔS>0,ΔG<0
- B、△S>0,△G>0
- C、ΔS<0,ΔG>0
- D、ΔS<0,ΔG<0
正确答案:A -
第9题:
PbSO4和KspӨ为1.8×10-8,在纯水中其溶解度为()mol·L-1;在浓度为1.0×10-2mol·L-1的Na2SO4溶液中达到饱和时其溶解度为()mol·L-1。
正确答案:1.3×10-4;2.68 -
第10题:
计算AgCl在1升0.1mol·L-1NH3·H2O中的溶解度为()。100克AgCl()(能/不能)全部溶解在1升1mol·L-1的氨水中。
正确答案:4.1×10-3mol·L-1;不能 -
第11题:
AgCl在0.01mol.L-1HCl溶液中溶解度比在纯水中小,当Cl-≥0.5mol/L时,AgCl反而比在水中容易溶解,其中的原因为()。
- A、同离子效应
- B、配位效应
- C、酸效应
- D、盐效应
正确答案:A,B -
第12题:
单选题25℃时,NaCl在水中的溶解度为6mol·L-1。若在1L水中加入5mol的NaCl,则溶解过程为()。AΔS>0,ΔG<0
B△S>0,△G>0
CΔS<0,ΔG>0
DΔS<0,ΔG<0
正确答案: A解析: 自发、熵增过程。 -
第13题:
常温常压下,下列气体在水中溶解度最大的是( )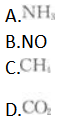 答案:A解析:
答案:A解析: -
第14题:
在298K时,NaCl在水中的溶解度为26g。如将1molNaCl溶解在1L水中,此溶解过程中体系的△H-TAS和熵如何变化( )。A.△H-T△S>0,△S<0
B.△H-T△S<0,△S>0
C.△H-T△S>0,△S>0
D.△H-T△S<0,△S<0答案:B解析:NaCl(S)溶解于水中是自发进行的过程,故△H-TAS<0;NaCl(S)=NaCl(aq),体系的混乱度增大,△S>0。 -
第15题:
有四个学生分别用下面的操作方法配制0.1mol/LCuSO4溶液,其中不正确的是()。
- A、量取25g胆矾溶解在1L水中
- B、称取16gCuSO4溶解在1L水中
- C、称取25g胆矾溶解在10ml水中,加入90mL水中,再加入90mL水
- D、量取500Ml0.2mol/LCuSO4溶液,加水至1L
正确答案:A,B,C -
第16题:
AgCl在1.0mol·L-1NaCl溶液中的溶解度要小于在纯水中的溶解度。
正确答案:正确 -
第17题:
用NaAc•3H2O晶体,2.0mol/LNaOH来配制PH为5.0的HAc-NaAc缓冲溶液1升,其正确的配制是()
- A、将49克NaAc•3H2O放入少量水中溶解,再加入50ml2.0mol/LHAc溶液,用水稀释1升
- B、将98克NaAc•3H2O放入少量水中溶解,再加入50ml2.0mol/LHAc溶液,用水稀释1升
- C、将25克NaAc•3H2O放入少量水中溶解,再加入100ml2.0mol/LHAc溶液,用水稀释1升
- D、将49克NaAc•3H2O放入少量水中溶解,再加入100ml2.0mol/LHAc溶液,用水稀释1升
正确答案:C -
第18题:
AgBr(s)在水中的溶解度为7.2×10-7mol·L-1,其Kθsp(),AgBr(s)在0.1 mol·L-1KBr溶液中的溶解度S=()mol·L-1。
正确答案:5.18×10-13;5.18×10-12 -
第19题:
Mn(OH)2的KspΘ为1.9×10-13,在纯水中其溶解度为()mol·L-1;0.050molMn(OH)2(s)刚好在浓度为()mol·L-1,体积为0.5L的NH4Cl溶液中溶解。
正确答案:3.6×10-5;2.8 -
第20题:
Ag2CrO4在纯水中的溶解度S=5.0×10-5mol/L,则其溶度积(),KspAg2CrO4在0.01 mol/L AgNO3溶液中的溶解度()。
正确答案:4s3=4×(5.0×10-5)3=5×10-13;Ksp/C2(Ag+)=5×10-13/0.01=5×10-9mol/L -
第21题:
AgCl在1mol.L-1NaCl溶液中,由于盐效应的影响,使其溶解度比在水中要略大一些。
正确答案:错误 -
第22题:
PbSO4的KspΘ为2.53×10-8,在纯水中其溶解度为()mol·L-1;在浓度为1.0×10-2mol·L-1的Na2SO4溶液中达到饱和时其溶解度为()mol·L-1。
正确答案:1.59×10-4;2.53×10-6 -
第23题:
判断题AgCl在1.0mol·L-1NaCl溶液中的溶解度要小于在纯水中的溶解度。A对
B错
正确答案: 错解析: 暂无解析
