已知反应:X+Y=M+N为放热反应,对该反应的下列说法正确的是(?? ) ? ?A.该反应为放热反应,因此不必加热即可反应 B.X能量一定高于M C.X和Y的总能量一定高于M和N的总能量 D.Y能量一定高于N
题目
已知反应:X+Y=M+N为放热反应,对该反应的下列说法正确的是(?? ) ? ?
A.该反应为放热反应,因此不必加热即可反应
B.X能量一定高于M
C.X和Y的总能量一定高于M和N的总能量
D.Y能量一定高于N
B.X能量一定高于M
C.X和Y的总能量一定高于M和N的总能量
D.Y能量一定高于N
相似考题
参考答案和解析
答案:C
解析:
A.反应的放热、吸热与反应条件(如加热)无关,某些放热反应也需要加热才能反应,如氢气和氧气的反应,故A错误;
B.反应物的总能量大于生成物的总能量,X的能量与Y的能量关系无法确定,故B错误;
C.该反应为放热反应,所以反应物的总能量大于生成物的总能量,即X和Y的总能量一定高于M和N的总能量,故C正确;
D.反应物的总能量大于生成物的总能量,Y的能量不一定高于N,故D错误.
故选C.
B.反应物的总能量大于生成物的总能量,X的能量与Y的能量关系无法确定,故B错误;
C.该反应为放热反应,所以反应物的总能量大于生成物的总能量,即X和Y的总能量一定高于M和N的总能量,故C正确;
D.反应物的总能量大于生成物的总能量,Y的能量不一定高于N,故D错误.
故选C.
更多“已知反应:X+Y=M+N为放热反应,对该反应的下列说法正确的是(?? ) ? ?”相关问题
-
第1题:
下列有关直链烷烃异构化反应,说法错误的是()。A、需借助催化剂金属和酸性功能
B、是辛烷值增加的反应
C、反应速度最快
D、是放热反应
参考答案:C
-
第2题:
 衡时,A的转化率与温度、压强的关系如图1-5所示.由图形可得出的正确结论是( )A.正反应吸热,m+n>p
衡时,A的转化率与温度、压强的关系如图1-5所示.由图形可得出的正确结论是( )A.正反应吸热,m+n>p
B.正反应吸热,m+nC.正反应放热,m+n>p
D.正反应放热,m+n答案:C解析:(1)首先把A的转化率与温度、压强三者问的关系转化为其中两者间的关系.其方法是: ①固定压强,即从三条曲线中任选一条.如选取1 ×106 Pa这条曲线,如图1-13所示,这条曲线表示在压强一定的条件下,A的转化率与温度之间的关系.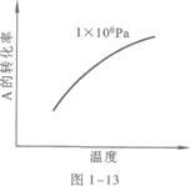

温度升高,A的转化率增大,说明平衡向右移动了.
根据平衡移动原理可知,温度升高,平衡向吸热方向移动.所以,正反应方向就是吸热方向,
即正反应为吸热反应.由此可否定C、D两个选项.
②固定温度.作一条与纵轴平行的垂线分别与三条曲线交于a、b、c点,如图1-14所示,这
三个点表明了在温度恒定时,A的转化率与压强之间的关系:压强增大,A的转化率也增大,说明平衡向右移动了.
同样,根据平衡移动原理可知,压强增大,平衡应向气体物质的量减小的方向移动,所以,正反应方向就是气体物质的量减小的方向,即m+n>p.由此可知A选项正确.
(2)解此题时应明确,反应方程式中气态物质前的系数之比就是它们的物质的量之比,也是它们的体积比(相同状况下).所以,讨论化学平衡问题,应注意各种物质的状态.第3题:
下列说法正确的是( )。
A.在化学反应中物质发生化学变化的同时.不一定发生能量变化
B.△H>0表示放热反应,△H<0表示吸热反应
C.放热反应,使体系的温度降低;吸热反应,使体系的温度升高
D.生成物释放的总能量大于反应物吸收的总能量时,该反应的△H<0答案:D解析:化学反应过程中既有物质变化又有能量变化,A项错误;△H>0,表示的是吸热反应,△H <0表示的是放热反应,B项错误;放热反应中,因为有热量的放出,所以使体系的温度升高;吸热反应中,因为要吸收热量,所以使体系的温度降低,C项错误;在化学反应中,生成物释放的总能量大于反应物吸收的总能量时,反应为放热反应,该反应的△H <0。D项正确。第4题:
下列有关SO2气体转化反应特点的叙述不正确的是()。
- A、体积缩小
- B、体积增大
- C、放热反应
- D、可逆反应
正确答案:B第5题:
关于烷烃和五元环烷烃的异构化说法正确的是()
- A、都是放热反应
- B、都是吸热反应
- C、烷烃为放热反应,环烷烃为吸热反应
- D、烷烃为吸热反应,环烷烃为放热反应
正确答案:A第6题:
如果一个反应是放热反应,而反应的熵变小于零,则该反应在()是可以自发的,()下就不是自发的。
正确答案:低温;高温第7题:
在容器不变的密闭容器中,在一定条件下发生反应:2A(g)=B(g)+C(S),且达到化学平衡,当升高温度时其容器内气体的密度增大,则下列判断正确的是()
- A、若正反应是吸热反应,则A为非气态
- B、若正反应是放热反应,则A为气态
- C、若在平衡体系中加入少量C该平衡向逆反应方向移动
- D、压强对该平衡的移动无影响
正确答案:A,B第8题:
在A+B=C+D平衡体系中,增温则平衡常数K变小,则下列选项正确的是()。
- A、正反应是放热反应,逆反应是吸热反应
- B、正逆反应都是吸热反应
- C、正逆反应都是放热反应
- D、正反应是吸热反应,逆反应是放热反应
正确答案:A第9题:
下列对生成MTBE的反应正确的是()。
- A、放热反应
- B、吸热反应
- C、加成反应
- D、不可逆反应
正确答案:A第10题:
PCl5的分解反应:PCl5(g)=PCl3(g)+Cl2(g),2000C达到平衡时有48.5%分解,3000C达到平衡时有97%分解。则下列说法正确的是()
- A、此反应为放热反应
- B、反应是吸热反应
- C、升高温度,平衡逆向移动
- D、压力改变对平衡无影响
正确答案:B第11题:
单选题对CO变换反应,下列说法正确的是()A高温和高水碳比有利于平衡右移
B变换反应是可逆放热反应
C变换过程采用但反应器
D压力对平衡和反应速度都无影响
正确答案: B解析: 暂无解析第12题:
单选题下列说法正确的是( )。A需要加热的化学反应都是吸热反应
B中和反应都是放热反应
C原电池是将电能转化为化学能的一种装置
D水力发电是将化学能转化为电能的过程
正确答案: B解析:
A项错误,加热,一般只是改变化学反应的速度,并不能说需要加热的化学反应都是吸热反应。B项正确,中和反应的实质是氢离子与氢氧根的结合,氢离子与氢氧根的能量和大于水的能量,故中和反应都放热。C项错误,原电池是将化学能转化为电能的一种装置。D项错误,水力发电是将机械能转化为电能的过程。第13题:
 A.该反应的正反应是吸热反应
A.该反应的正反应是吸热反应
B.该反应的逆反应是放热反应
C.该反应的正反应是放热反应
D.温度对该反应没有影响答案:C解析:对于放热,温度升高,平衡常数降低。第14题:
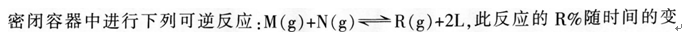 化符合图1,其中R%为R在平衡混合物中的体积分数,T,P分别为温度和压强,下列判断正确的是( )。
化符合图1,其中R%为R在平衡混合物中的体积分数,T,P分别为温度和压强,下列判断正确的是( )。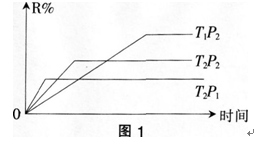 A、正反应为吸热反应、L为气体
A、正反应为吸热反应、L为气体
B、正反应为吸热反应、L为固体
C、正反应为放热反应、L为气体
D、正反应为放热反应、L为固体或液体答案:C解析:第15题:
合成氨指由氮和氢在高温高压和催化剂存在下直接合成的氨,下列关于合成氨工艺的反应类型,说法正确的是( )。A.吸热反应
B.放热反应
C.吸放热平衡反应
D.自平衡反应答案:A解析:本题考查的是危险化工工艺及安全技术。合成氨工艺的反应为吸热反应。第16题:
关于对烃化反应说法正确的有()。
- A、烃化反应的苯进料是大量超过化学计量的。
- B、烃化反应是放热反应。
- C、烃化反应是气相可逆反应。
- D、高的苯烯比可以使乙烯转化率提高,二乙苯和三乙苯浓度降低。
正确答案:A,B,C,D第17题:
对放热反应若提高反应温度则会()反应速度。
正确答案:加快第18题:
吹氧氧化脱炭是放热反应,加矿氧化也是实现碳氧间的反应,故也是放热反应。
正确答案:错误第19题:
在平衡体系中,增温则平衡常数K变小,则下列选项正确的是()。
- A、正反应是放热反应,逆反应是吸热反应
- B、正逆反应都是吸热反应
- C、正逆反应都是放热反应
- D、正反应是吸热反应,逆反应是放热反应
正确答案:A第20题:
钴钼加氢为()反应。
- A、吸热反应
- B、既不吸热也不放热反应
- C、放热反应
- D、物理
正确答案:C第21题:
含成氨生产中,碳与水蒸汽的化学反应是()。
- A、吸热反应;
- B、放热反应;
- C、先吸热反应后放热反应;
- D、先放热反应后吸热反应;
正确答案:B第22题:
下列说法正确的是()
- A、需要加热的化学反应都是吸热反应
- B、中和反应都是放热反应
- C、原电池是将电能转化为化学能的一种装置
- D、水力发电是将化学能转化为电能的过程
正确答案:B第23题:
单选题已知反应:mA+nB=pC+qD,当体系总压力增大一倍时,该反应的反应速率增大到原来的四倍,则(m+n)等于( )。A1
B2
C4
D0
正确答案: C解析:
反应的速率方程为v=k[c(A)]m[c(B)]n,当体系总压力增大一倍时,c(A)1=2c(A)0,c(B)1=2c(B)0,此时v1=k[c(A)1]m[c(B)1]n=k[2c(A)0]m[2c(B)0]n=2(m+n)k[c(A)0]m[c(B)0]n=2(m+n)kv0=4v0,即2(m+n)=4,所以(m+n)等于2。
