中和10ML0.1mol/L氨水需要0.05mol/L盐酸()mL,在理论终点时溶液显()性。
题目
相似考题
更多“中和10ML0.1mol/L氨水需要0.05mol/L盐酸()mL,在理论终点时溶液显()性。”相关问题
-
第1题:
中和10ML0.1mol/L氨水需要0.05mol/L盐酸20mL,在理论终点时溶液显( )性
正确答案:酸
-
第2题:
强心苷温和酸水解的条件是A.0.02~0.05mol/L盐酸长时间加热
B.0.01mol/L盐酸,在含水醇中短时间加热
C.3%~5%盐酸,长时间加热
D.0.02~0.05mol/L盐酸,在含水醇中短时间加热
E.0.02~0.05mol/L盐酸,在含水醇中短时间加热答案:D解析:答案只能是D,其他均为干扰答案。 -
第3题:
强心苷温和酸水解的条件是A.0.02~0.05moL/L盐酸长时间加热
B.0.01mol/L盐酸,在含水醇中短时间加热
C.3%~5%盐酸,长时间加热
D.0.02~0.05mol/L盐酸,在含水醇中短时间加热
E.0.02~0.05moI/L盐酸,在含水醇中长时间加热答案:D解析:强心苷温和酸水解的条件是0.02~0.05mol/L盐酸,在含水醇中短时间加热,所以答案为D。 -
第4题:
现有6m3废NaOH溶液,其浓度为0.1mol/L,打算用0.05mol/L的HCl溶液进行中和,需要多少m3的HCl溶液?
正确答案: 设需要xm3的HCl溶液
根据NaOH和HCl反应时,其摩尔比为1:1。则
6×103×0.1=x×103×0.05
X=12 -
第5题:
浓度为0.1000mol/L的NaOH溶液滴定相同浓度的HAc溶液,理论终点时溶液显()。
正确答案:碱性 -
第6题:
以浓度为0.1000mol/L的氢氧化钠溶液滴定20mL浓度为0.100011101/L的盐酸,理论终点后,氢氧化钠过量O.02mL,此时溶液的pH值为()。
- A、(A11.00
- B、B.3.3
- C、C.8.0
- D、D.9.7
正确答案:D -
第7题:
将100mL0.1mol·L-1HAc溶液加到100mL0.1mol·L-1NaOH溶液中,因恰能中和完全,所以混合溶液应显中性。
正确答案:错误 -
第8题:
强心苷温和酸水解的条件是()
- A、0.02~0.05moL/L盐酸长时间加热
- B、0.01mol/L盐酸,在含水醇中短时间加热
- C、3%~5%盐酸,长时间加热
- D、0.02~0.05mol/L盐酸,在含水醇中短时间加热
- E、0.02~0.05moI/L盐酸,在含水醇中长时间加热
正确答案:D -
第9题:
对于氢氧化钠、氨水等废液可以进行如下处理:用6mol/L盐酸水溶液中和,再用大量水冲洗。
正确答案:正确 -
第10题:
中和下列溶液,需要多少毫升0.2150mol/LNaOH溶液? (1)22.53mL 0.1250mol/L H2SO4溶液; (2)20.52mL 0.2040mol/L HCl溶液。
正确答案: (1)22.53×0.1250×2=0.2150V ;V= 26.20(mL)
(2)20.52×0.2040=0.2150V;V=19.47(mL) -
第11题:
单选题0.05mol/L的次氯酸钠溶液配制,取1ml次氯酸试剂原液,用碘量法标定其浓度,然后用()稀释成0.05mol/L的溶液。A水
B吸收液
C1+1盐酸溶液
D2mol/L氢氧化钠溶液
正确答案: D解析: 暂无解析 -
第12题:
判断题将100mL0.1mol·L-1HAc溶液加到100mL0.1mol·L-1NaOH溶液中,因恰能中和完全,所以混合溶液应显中性。A对
B错
正确答案: 对解析: 暂无解析 -
第13题:
将6 mL 0.2 mol/L盐酸与10 mL 0.1 mol/L氨水混合,完全反应后,溶液中各种离子浓度的相对大小是.答案:解析: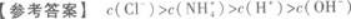 【解题指要】(1)首先要强调,将两种溶液混合时必须考虑这一过程中是否发生化学反应.如本题是将盐酸与氨水混合,会发生化学反应:
【解题指要】(1)首先要强调,将两种溶液混合时必须考虑这一过程中是否发生化学反应.如本题是将盐酸与氨水混合,会发生化学反应:

根据HCl和NH3的数量的不同.可能有三种情况:
①恰好完全反应,此时就变成NH4Cl溶液;
②HCl有剩余,此时就是NH4Cl和HCl的混合溶液;
③NH3有剩余,此时就是NH4Cl与NH3的混合溶液.
(2)盐酸中HCl的物质的量为:0.2 mol/L×0.006 L=0.001 2 mol.
氨水中NH3的物质的量为:0.1 mol/L×0.01 L=0.001 mol.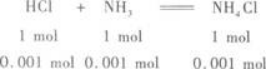
所以,反应后生成NH4Cl 0.001 mol,剩余的HCl为0.001 2 mol-0.001 mol=0.000 2 mol.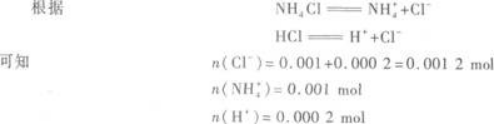
以上物质的量的大小顺序就是离子浓度的大小顺序.
另外,一般情况下,溶液均指水溶液,所以溶液中还有水电离出来的H+和OH-两种离子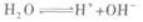
此题中酸有剩余,所以c(H+)一定大于c(OH-).
-
第14题:
强心苷温和酸水解的条件是A:0.02~0.05mol/L盐酸长时间加热
B:0.0lmol/L盐酸,在含水醇中短时间加热
C:3%~5%盐酸,长时间加热
D:0.02~0.05mol/L盐酸,在含水醇中短时间加热
E:0.02~0.05mol/L盐酸,在含水醇中长时间加热答案:D解析: -
第15题:
强心苷温和酸水解的条件是A:0.02~0.05mol/L盐酸长时间加热
B:0.0lmol/L盐酸,在含水醇中短时间加热
C:3%~5%盐酸,长时间加热
D:0.02~0.05mol/L盐酸,在含水醇中短时间加热答案:D解析: -
第16题:
10mL0.1mol/LHAc溶液与10mL0.1mol/LNaOH溶液混合,pH值等于7。()
正确答案:正确 -
第17题:
用0.1000moL/L盐酸溶液滴定0.1000mol/L氨水等量点时,溶液的PH值为()
- A、等于7.0
- B、小于7.0
- C、大于7.0
正确答案:B -
第18题:
用标准的盐酸溶液来滴定待测NaOH溶液,已知盐酸溶液物质的量浓度为0.02mol/L,用量为20mL,待测NaOH溶液的用量为40mL,则NaOH溶液物质的量浓度为()。
- A、0.01mol/L
- B、0.02mol/L
- C、0.03mol/L
- D、0.05mol/L
正确答案:A -
第19题:
25℃时CaCO3的溶解度在()最小。()
- A、0.05mol·L-1的AgN03溶液
- B、0.05mol·L-1的CaCl2溶液
- C、0.01mol·L-1的NaCl溶液
- D、纯水
正确答案:B -
第20题:
0.05mol/L的次氯酸钠溶液配制,取1ml次氯酸试剂原液,用碘量法标定其浓度,然后用()稀释成0.05mol/L的溶液。
- A、水
- B、吸收液
- C、1+1盐酸溶液
- D、2mol/L氢氧化钠溶液
正确答案:D -
第21题:
中和10ML0.1mol/L氨水需要0.05mol/L盐酸()mL,在理论终点时溶液显()性。
正确答案:20;酸 -
第22题:
填空题0.1mol·L-1的RClx溶液10mL,当加入0.05mol·L-1的AgNO3溶液60mL时,恰好完全反应,x值等于____.正确答案: 3解析:
由原子个数守恒.银离子和氯离子最终以氯化银形式沉淀.银离子的物质的量等于氯离子的物质的量. -
第23题:
单选题向200mL0.1mol/L Na2SO4溶液中加入100mL0.25mol/L的Ba(OH)2溶液后,还需加入多少盐酸才能恰好完全中和( ).A10mL lmol/L盐酸
B5mL lmol/L盐酸
C50mL lmol/L盐酸
D25mL 0.5mol/L盐酸
正确答案: A解析:
Ba(OH)2溶液加入后对氢氧根离子没有消耗,所以溶液中的氢氧根离子的物质的量为为0.05mol,所以需要0.05mol的氢离子来中和. -
第24题:
判断题对于氢氧化钠、氨水等废液可以进行如下处理:用6mol/L盐酸水溶液中和,再用大量水冲洗。A对
B错
正确答案: 对解析: 暂无解析
