下列分子中,键角最大的是: A. NH3 B. H2S C. BeCl2 D. CCl4
题目
下列分子中,键角最大的是:
A. NH3
B. H2S
C. BeCl2
D. CCl4
B. H2S
C. BeCl2
D. CCl4
相似考题
更多“下列分子中,键角最大的是: A. NH3 B. H2S C. BeCl2 D. CCl4”相关问题
-
第1题:
下列分子中,偶极矩不等于零的是:
A. BeCl2 B. NH3 C. BF3 D. CO2答案:B解析:提示:偶极矩等于零的是非极性分子,偶极矩不等于零的为极性分子。 -
第2题:
下列分子中,键角最大的是( )。A.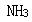
B.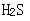
C.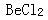
D. 答案:C解析:
答案:C解析:
-
第3题:
下列分子中,键角最大的是:A. NH3
B. H 2S
C. BeCl 2
D. CCl 4答案:C解析:BeCl 2中说采取sp杂化,为直线型分子,键角180°。
答案:C -
第4题:
在下列各种化合物中,分子间有氢键的是( )。
A. CH3Br B. NH3 C. CH4 D. CH3Cl答案:B解析:提示:分子中含有N—H、O—H、F—H键的化合物,含有氢键。 -
第5题:
下列分子中,键角最大的是( )。
A. NH3 B. H2S C. BeCl2 D. CCl4答案:C解析:提示:BeCl2分子空间构型为直线形,键角180°,CCl4分子空间构型为正四面体, NH3分子空间构型为三角锥形,H2S为V字形,键角均小于180°。 -
第6题:
下列各组物质中,键有极性,分子也有极性的是:()
- A、CO2和SO3
- B、CCl4与Cl2
- C、H2O和SO2
- D、HgCl2与NH3
正确答案:C -
第7题:
指出下列分子的杂化方式和几何构型:CCl4、H2S、CO2、BCl3、HgCl2
正确答案: CCl4:sp3杂化正四面体
H2S:不等性sp3杂化V字形
CO2:sp杂化直线形
BCl3:sp2杂化平面三角形
HgCl2:sp杂化直线形 -
第8题:
根据键的极性和分子的几何构型,判断下列分子哪些是极性分子?哪些是非极性分子? Br2,HF,H2S(V形),CS2(直线形),CHCl2(四面体),CCl4(正四面体)
正确答案: 极性分子:HF、H2S、CHCl3
非极性分子:Br2、CS2、CCl4 -
第9题:
下列分子中,键角最大的是()。
- A、NH3
- B、H2S
- C、BeCl2
- D、CCl4
正确答案:C -
第10题:
试判断下列分子是极性分子是有();是非极性分子的有()。 BeH2,H2S,HCl,CCl4,CHCl3
正确答案:H2S,HCl,CHCl3;BeH2,CCl4 -
第11题:
根据键的极性和分子几何构型,推断下列分子哪些是极性分子?哪些是非极性分子? Ne Br2 HF NO H2S(V字型)CS2(直线型)CHCl3(四面体)CCl4(正四面体)BF3(平面三角形)NH3(三角锥形)
正确答案: 极性分子:HFNOH2S(V字型)CHCl3(四面体)NH3(三角锥形)
非极性分子:NeBr2CS2(直线型)CCl4(正四面体)BF3(平面三角形) -
第12题:
单选题下列分子中,键角最大的是( )。ANH3
BH2S
CBeCl2
DCCl4
正确答案: A解析:
A项,NH3为不等性sp3杂化,N—H键间的夹角要比理论值小一些,不是109°28′,而是107°;B项,H2S为sp3杂化,键角92.1°;C项,BeCl2为sp杂化,键角180°;D项,CCl4为sp3杂化,键角109°28′。 -
第13题:
下列物质中,分子的空间构型为“V”字形的是:
A. CO2 B. BF3 C. BaCl2 D. H2S答案:D解析:提示:C02直线型,H2S中S采取不等性sp3杂化,为“V”字形。 -
第14题:
NH3,分子中H—N—H的键角为( )。 答案:B解析:NH3分子中H—N—H的键角为107°18′。
答案:B解析:NH3分子中H—N—H的键角为107°18′。 -
第15题:
用杂化轨道理论推测下列分子空间构型,其中为三角锥形的是( )。
A. NH3 B. H2O C. BF3 D. BeCl2答案:A解析:提示:BF3中心原子B以Sp2杂化,呈平面三角形;NH3的中心原子N为Sp3不等性杂化,分子构型为三角锥形,H2O为V字形;BeCl2为直线形。 -
第16题:
下列各物质分子间只存在色散力的是()。
A. SiH4 B. NH3 C. H2O D. HCl答案:A解析:提示:SiH4为非极性分子,非极性分子之间只存在色散力,而NH3、 H2O、 HCl 三种分子都为极性分子,极性分子之间不仅存在色散力,还存在诱导力和取向力。 -
第17题:
下列分子NH3、BCl3、CO2、H2S、SiCl4中,属于极性分子的是()。
正确答案:NH3和H2S -
第18题:
判断下列各组分子之间存在什么形式的分子间作用力。 ⑴H2S气体分子 ⑵Ne与水 ⑶CH3Br气体分子 ⑷NH3气体分子 ⑸Br2与CS2
正确答案:⑴色散力、诱导力、取向力;
⑵色散力、诱导力;
⑶色散力、诱导力、取向力;
⑷色散力、诱导力、取向力、氢键;
⑸色散力。 -
第19题:
请解释下列有关键长和键角的问题:NH3﹑PH3﹑AsH3分子中的键角依次为107°﹑93.08°﹑91.8°,逐渐减小。
正确答案:从N到As,电负性逐渐减小,孤电子对离核越来越远,对成键电子排斥作用越来越弱,故键角逐渐减小。 -
第20题:
(2007)下列分子中,键角最大的是:()
- A、NH3
- B、H2S
- C、BeCl2
- D、CCl4
正确答案:C -
第21题:
H2S分子以不等性sp3杂化轨道成键,所以它的键角是:()
- A、109.5°
- B、小于109.5°
- C、大于109.5°
正确答案:B -
第22题:
CCl4分子中,C-Cl键是()性共价键;但由于分子的(),所以CCl4分子是()。
正确答案:极性;对称性结构;非极性分子 -
第23题:
单选题下列分子中 , 含有键角最大的是()A甲烷
B乙烯
C乙炔
D苯
E以上都不对
正确答案: C解析: 暂无解析
