(15分)(注意:在试题卷上作答无效)已知周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化合价氧化物的水化物是强酸。回答下列问题:(1)W与Q可以形成一种高温结构陶瓷材料。W的氯化物分子呈正四面体结构,W的氧化物的晶体类型是 ;(2)Q的具有相同化合价且可以相互转变的氧化物是 ;(3)R和Y形成的二元化合物中,R呈现最高化合价的化合物的化学式是 ;(4)这5个元素的氢化物分子中,①立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式) ,其原因是;②电子总数相同的氢化物的化学式和立体结构分别是;
题目
(15分)(注意:在试题卷上作答无效)
已知周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化合价氧化物的水化物是强酸。回答下列问题:
(1)W与Q可以形成一种高温结构陶瓷材料。W的氯化物分子呈正四面体结构,W的氧化物的晶体类型是 ;
(2)Q的具有相同化合价且可以相互转变的氧化物是 ;
(3)R和Y形成的二元化合物中,R呈现最高化合价的化合物的化学式是 ;
(4)这5个元素的氢化物分子中,①立体结构类型相同的氢化物的沸点从高到低排列次序是(填化学式) ,其原因是
;
②电子总数相同的氢化物的化学式和立体结构分别是
;
(5)W和Q所形成的结构陶瓷材料的一种合成方法如下:W的氯化物与Q的氢化物加热反应,生成化合物W(QH2)4和HCL气体;W(QH2)4在高温下分解生成Q的氢化物和该陶瓷材料。上述相关反应的化学方程式(各物质用化学式表示)是 。
相似考题
更多“(15分)(注意:在试题卷上作答无效) 已知周期表中,元素Q、R、W、Y与元素X相邻。Y的最高化合价氧化 ”相关问题
-
第1题:
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是( )。
A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X)
B.Y分别与Z、W形成的化合物中化学键类型相同
C.X的最高价氧化物对应水化物的酸性比W的弱
D.Y的简单气态氢化物的热稳定性比W强答案:D解析:由X、Y、Z、W的原子序数依次增大,x原子的最外层电子数是其内层电子数的2倍,可知X是C元素;Y是地壳中含量最高的元素,因此Y是0元素;Z2+和Y2-一具有相同的电子层结构,因此Z是Mg元素;W和X位于同主族,因此W是Si元素。A项,原子半径顺序应该是r(Z)>r(W)>r(X)>r(Y),A项错误;B项,Y与Z形成的化合物是M90,化学键是离子键,Y与W形成的化合物是Si02,化学键是共价键,B项错误;C项,同主族元素从上到下最高价氧化物对应的氧化物的酸性依次减弱.C项错误:D项,同周期元素对应的气态氢化物的稳定性从左到右依次增强,同主族的元素气态氢化物的稳定性从上到下依次减弱.故Y的简单气态氢化物的热稳定性比W的强.故D正确。 -
第2题:
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与X同主族。下列说法正确的是( )。A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X)
B.Y分别与Z、W形成的化合物中化学键类型相同
C.X的最高价氧化物对应水化物的酸性比W的弱
D.Y的气态简单氢化物的热稳定性比W的强答案:D解析:【知识点】元素周期表
【解析】由题意可知,X为碳,Y为氧,Z为镁,W为硅,则原子半径镁大于硅,A项错误;氧化镁为离子键,二氧化硅为共价键,B项错误;碳酸的酸性大于硅酸,C项错误;水的热稳定性大于硅烷.D项正确。故本题选D。 -
第3题:
短周期主族的非金属元素X、Y、Z在周期表中的位置如图所示,下列有关说法一定正确的是( )。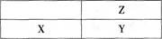 A、气态氢化物的稳定性:Z>Y>X
A、气态氢化物的稳定性:Z>Y>X
B、第一电离能:Z>Y>X
C、含氧酸的酸性:Z>Y>X
D、元素的最高化合价:Z=Y>X答案:A解析:同周期元素,从左到右,非金属性逐渐增强;同主族元素,从上到下,非金属性逐渐减弱。非金属性越强,气态氢化物越稳定,A项正确。若X是P,Y是S,Z是O,则第一电离能Z>X>Y,B项错误。若X是S,Y是Cl,Z是F,F没有含氧酸,F没有正化合价,C、D项错误。故本题选A。 -
第4题:
图4为元素周期表的一部分,其中X、Y、Z、W为短周期元素,W元素的核电荷数为X元素的2倍。下列说法正确的是( )。
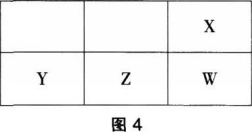 A.X、Z、W元素的原子半径依次递增
A.X、Z、W元素的原子半径依次递增
B.X元素常见氢化物的沸点高于W元素常见氢化物的沸点
C.YX2晶体熔化、液态WX3气化均需克服分子间作用力
D.Y、Z、W元素在自然界中均不能以游离态存在答案:B解析:因为X、Y、Z、W为短周期元素,X与W位于同主族,且W元素的核电荷数为X元素的2倍.则设X元素最外层电子数为x,则2+8+x=2(2+x),解得x=6,所以X为0,W为S,Z为P,Y为Si。P的原子半径大于S,A项错误。X元素常见氢化物为H2O,W元素常见氢化物为H2S,H2O含有氢键,故H2O的沸点高于H2S,B项正确。SiO2是原子晶体,其熔化需克服的是共价键,C项错误。S能以游离态存在于自然界中,D项错误。故本题选B。 -
第5题:
短周期主族元素X、Y、Z、W的原子序数依次增大。X原子的最外层电子数是其内层电子数的2倍,Y是地壳中含量最高的元素,Z2+与Y2-具有相同的电子层结构,W与x同主族。下列说法正确的是( )。A.原子半径大小顺序:r(W)>r(Z)>r(Y)>r(X)
B.Y分别与Z、W形成的化合物中化学键类型相同
C.X的最高价氧化物对应水化物的酸性比W的弱
D.Y的气态简单氢化物的热稳定性比W的强答案:D解析:由题意可知:X为C,Y为0,Z为Mg,w为Si,则原子半径r(Si)>r(Mg)>r(c)>r(O),A项错误;M90为离子键,Si02为共价键,B项错误;碳酸的酸性大于硅酸,C项错误;水的热稳定性大于硅烷.D项正确。故选D。 @##
