用二氧化锰与浓盐酸混合加热制氯气,此反应中若有2 mol氯化氢参与反应,则电子转移的物质的量为(??)A.0.5 mol B.1 mol C.2 mol D.4 mol
题目
B.1 mol
C.2 mol
D.4 mol
相似考题
参考答案和解析
更多“用二氧化锰与浓盐酸混合加热制氯气,此反应中若有2 mol氯化氢参与反应,则电子转移的物质的量为(??)”相关问题
-
第1题:
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是( )。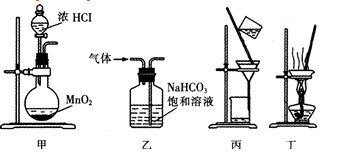 A.用装置甲制取氯气
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl2 ?4H2O答案:C解析:用二氧化锰与浓盐酸反应制取氯气,需要加热,A项错误;气体除杂应深入浅出,B项错误;过滤可以分离二氧化锰和氯化锰溶液,C项正确;氯化锰易发生水解反应,D项错误。故选C。 -
第2题:
下列装置应用于实验室制氯气并回收氯化锰的实验,能达到实验目的的是( )。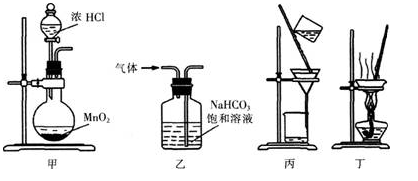 A.用装置甲制取氯气
A.用装置甲制取氯气
B.用装置乙除去氯气中的少量氯化氢
C.用装置丙分离二氧化锰和氯化锰溶液
D.用装置丁蒸干氯化锰溶液制MnCl答案:C解析:【知识点】化学实验
【解析】二氧化锰和浓盐酸反应制取氯气,需要加热,A项错误;气体除杂应深入浅出,B项错误;过滤可以分离二氧化锰和氯化锰溶液,C项正确;氯化锰易发生水解反应,D项错误。故本题选C。 -
第3题:
0.62gNa2O恰好与20mL某浓度的盐酸完全反应,此盐酸的物质的量浓度为()(Na2O的相对分子质量为62)。
- A、1.0mol/L
- B、0.2mol/L
- C、0.4mol/L
- D、0.5mol/L
正确答案:A -
第4题:
500mL盐酸溶液中,含有纯盐酸的质量为36.5g,则此盐酸的物质的量浓度为()。
- A、0.5mol/L
- B、2mol/L
- C、3mol/L
- D、1.5mol/L
正确答案:B -
第5题:
agKClO3和bg二氧化锰混合加热,完全反应后,可得到cgKCl,则反应中得到氧气的质量为()
- A、(a+b-c)g
- B、b-cg
- C、(a+b+c)g
- D、a-cg
正确答案:D -
第6题:
在实验室,常用浓盐酸与()反应,来制备氯气。
- A、Fe2O3
- B、KMnO4
- C、Mg
- D、MnO2
正确答案:D -
第7题:
用市售浓盐酸配制的1+5HCl溶液,相当于物质的量浓度为()。
- A、3mol/L
- B、4mol/L
- C、2mol/L
正确答案:A -
第8题:
下列反应可制得纯净一氯乙烷的是()。
- A、乙烯通入浓盐酸中
- B、乙烯与氯化氢加成反应
- C、乙烷与氯气在光照下反应
- D、乙烷通入氯水中
正确答案:B -
第9题:
单选题K35ClO3晶体和含有H37Cl的浓盐酸反应生成氯气,已知反应方程式为KClO3+6HCl(浓)=KCl+3Cl2↑+3H2O,此反应生成氯气的摩尔质量为( ).A74g·mol-1
B73.3g·mol-1
C72g·mol-1
D70.6g·mol-1
正确答案: A解析:
由双线桥分析可知,生成的3个Cl2中共有6个Cl原子,其中5个来自于HCl中的37Cl,有1个来自KClO3中的35Cl,故氯气的相对分子质量为(35+5×37)÷6×2=73.3,则氯气的摩尔质量为73.3g·mol. -
第10题:
填空题甲烷与氯气可以发生____反应;乙烯与氯气可以发生____反应;苯与浓硝酸、浓硫酸混合,在60℃条件下,可以发生____反应,在该反应中浓硫酸是____.正确答案: 取代,加成,取代(硝化),催化剂解析:
甲烷与氯气发生取代反应生成一氯甲烷和HCl,乙烯与氯气发生加成反应生成二氯乙烷;将苯滴入浓硝酸和浓硫酸混合液中,并在60℃条件下反应生成硝基苯和水;由于硫酸反应前后物质的量不变,所以浓硫酸为催化剂. -
第11题:
单选题已知:①1molH2分子中化学键断裂时需要吸收436kJ的能量 ②1molCl2分子中化学键断裂时需要吸收243kJ的能量 ③由H原子和Cl原子形成1molHCl分子时释放431kJ的能量。 下列叙述正确的是()。A氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)2HCl(g)
B氢气和氯气反应生成2mol氯化氢气体,反应的ΔH=+183kJ·mol-l
C氢气和氯气反应生成2mol氯化氢气体,反应的ΔH=-183kJ·mol-l
D氢气和氯气反应生成1mol氯化氢气体,反应的AH=+183kJ·mol-l
正确答案: B解析: 暂无解析 -
第12题:
单选题下列各组物质在一定条件下反应,可以制得比较纯净的1,2-二氯乙烷的是:A乙烯通入浓盐酸中
B乙烷与氯气混合
C乙烯与氯气混合
D乙烯与卤化氢气体混合
正确答案: A解析: -
第13题:
在恒容密闭容器中,将CO和H2S混合加热,发生下列反应并达到平衡:
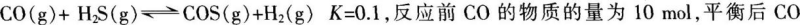
物质的量为8 mol。下列说法正确的是( )。《》()A.升高温度,H2S浓度增加,表明正反应是吸热反应
B.通入CO后,正反应速率逐渐增大
C.反应前H2S物质的量为7 mol
D.C0的平衡转化率为80%答案:C解析:升高温度,H2S的浓度增加,说明反应向逆反应方向进行,则逆反应是吸热反应,正反应是放热反应,A项错误。通入CO后,正反应速率先增大后逐渐减小至平衡,B项错误。反应平衡后消耗了2molCO,同

-
第14题:
工业上制备无水AlCl3常用的方法是()。
- A、加热使AlCl3·H2O脱水
- B、Al2O3与浓盐酸作用
- C、熔融的铝与氯气反应
- D、硫酸铝水溶液与氯化钡溶液反应
正确答案:C -
第15题:
加热就能生成少量氯气的一组物质是()。
- A、氯化钠和硫酸
- B、氯化钠和二氧化锰
- C、盐酸和溴
- D、盐酸和高锰酸钾
正确答案:D -
第16题:
在实验室中MnO2(s)仅与浓HCl加热才能反应制取氯气,这是因为浓HCl仅使E(MnO2/Mn2+)增大。
正确答案:错误 -
第17题:
关于盐酸的物理化学性质,下面哪一个说法是不正确的()。
- A、盐酸是没有颜色的液体
- B、浓盐酸有白雾是因为从浓盐酸中挥发出来的氯化氢气体与空气中水蒸气接触形成的
- C、盐酸跟很多金属单质反应会产生氢气
- D、浓盐酸中含有质量分数为80%以上的氯化氢
正确答案:D -
第18题:
在二氧化锰和浓盐酸的反应中()是还原剂,在锌和盐酸的反应中()是氧化剂。
正确答案:浓盐酸,盐酸 -
第19题:
在200毫升稀盐酸溶液中,含有0.73克氯化氢,则溶液的物质的量浓度为()。
- A、0.01mol/L
- B、0.1mol/L
- C、0.01L/mol
- D、0.1L/mol
正确答案:B -
第20题:
(2013)下列各组物质在一定条件下反应,可以制得比较纯净的1,2-二氯乙烷的是:()
- A、乙烯通入浓盐酸中
- B、乙烷与氯气混合
- C、乙烯与氯气混合
- D、乙烯与卤化氢气体混合
正确答案:C -
第21题:
单选题在铜和浓H2SO4的反应中,如果电子转移0.4mol,则被还原的硫酸的物质的量是( ).A0.4mol
B0.2mol
C2mol
D4mol
正确答案: A解析:
在该反应中,浓硫酸中正六价的硫转移到二氧化硫中,每生成1mol二氧化硫转移2mol电子.因此转移0.4mol电子时,还原硫酸的物质的量为0.2mol. -
第22题:
单选题在实验室中用二氧化锰和盐酸制取氯气的反应中,得到22.4升(标准状况下)氯气时,被氧化的氯化氢的物质的量是( ).A2摩尔
B3摩尔
C4摩尔
D1摩尔
正确答案: B解析:
22.4升(标准状况下)氯气的物质的量为1mol,制取氯气的化学反应方程式为MnO2+4HCl=Cl2+MnCl2+2H2O,被氧化的HCl与生成的氯气之比为2∶1,故每有1mol氯气生成就有2mol氯化氢被氧化. -
第23题:
单选题下列各组物质在一定条件下反应,可以制得较纯净的1,2-二氯乙烷的是( )。[2013年真题]A乙烯通入浓盐酸中
B乙烷与氯气混合
C乙烯与氯气混合
D乙烯与卤化氢气体混合
正确答案: D解析:
乙烯与氯化氢加成反应得到一氯乙烷,乙烷与氯气取代产物有多种,乙烯与卤化氢气体混合,卤素原子不同,生成不同的卤代乙烷。
