73g质量分数为20%的盐酸与足量大理石反应,生成二氧化碳的质量是多少?这些二氧化碳的体积(标准状况)是多少?(在标准状况下,二氧化碳的密度为1.977g/L。)
题目
73g质量分数为20%的盐酸与足量大理石反应,生成二氧化碳的质量是多少?这些二氧化碳的体积(标准状况)是多少?(在标准状况下,二氧化碳的密度为1.977g/L。)
相似考题
参考答案和解析
更多“73g质量分数为20%的盐酸与足量大理石反应,生成二氧化碳的质量是多少?这些二氧化碳的体积(标准状况)是多少?(在标准状况下,二氧化碳的密度为1.977g/L。)”相关问题
-
第1题:
锌与盐酸(HCl)反应生成氢气和氯化锌。实验室里用6.5g锌与足量盐酸反应,可
制得氢气和氯化锌的质量各是多少?
解:设制得H2的质量为x,ZnCl2 的质量为y。 Zn+2HCl=ZnCl2+H2↑ 65 136 2 6.5 g y x x=6.5g×2/65=0.2g y=136×6.5g/65=13.6g 答:可制得H2的质量约为0.2 g,ZnCl2的质量约为13.6 g。 -
第2题:
镁、锌、铁三种金属各30g,分别与足量盐酸反应,生成氢气的质量各是多少?如果反应后各生成氢气30g,则需要这三种金属的质量各是多少?
生成氢气的质量:Mg: 2.5g, Zn: 0.92g, Fe: 1.07g 需要金属的质量:Mg: 360g, Zn: 975g, Fe: 840g -
第3题:
体积水(密度为1 g/cm)吸收了560体积(标准状况下)氨气,所得氨水的密度为0.90 g/cm,求此溶液中溶质的质量分数.用此氨水10 mL与含7.74 g H,PO4的溶液混合,恰好完全反应,求此反应生成盐的分子式.答案:解析:
【解题指要】
(1)解此题首先应把体积单位具体化.设其为“L”,变为“1 L水溶解560 L(标准状况下)NH3”,这样便于计算.
(2)因NH3与H3PO4反应,可能有三种产物:NH4H2PO4、(NH4)2HPO4和(NH4)3PO4,所以应知道n(NH3)与n(H3PO4)的比值,才能知道生成盐的分子式. -
第4题:
一定质量的某铝屑和铁屑的混合物与足量稀硫酸反应后放出氢气8.96L(标准状况),同质量的此混合物与足量的氢氧化钠溶液反应,放出氢气6.72L(标准状况),求混合物中铝和铁的质量.答案:解析:题目中涉及的化学反应如下: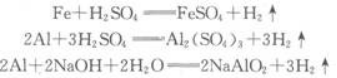

答:原混合物中铝的质量为5.4g,铁的质量为5.6g. -
第5题:
空气中二氧化碳浓度为0.10%,该浓度在标准状况下的质量浓度是A.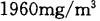
B.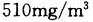
C.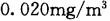
D.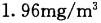
E.百分浓度未注明是否在标准状况无法计算答案:A解析: -
第6题:
空气中二氧化碳浓度为0.10%,该浓度在标准状况下的质量浓度是()
- A、1960mg/m3
- B、510mg/m3
- C、0.020mg/m3
- D、1.96mg/m3
- E、百分浓度未注明是否在标准状况无法计算
正确答案:A -
第7题:
在标准状况下,2.2g 二氧化碳气体的体积和 l .6g氧气的体积相等。
正确答案:正确 -
第8题:
在标准状况下,2.2g二氧化碳气体的体积和1.6g氧气的体积相等。
正确答案:正确 -
第9题:
在标准状况下,2.2克二氧化碳气体的体积和1.6克氧气的体积相等。
正确答案:正确 -
第10题:
填空题在标准状况下,8g某气体的分子数与22g二氧化碳的分子数相等.则该气体的密度为____.正确答案: 0.714g/L解析:
因为“8g某气体的分子数与22g二氧化碳的分子数相等”,所以8g气体与22g二氧化碳的物质的量相同,均为0.5mol,在标准状况下,气体体积均为11.2L,所以该气体的密度为8g/11.2L=0.714g/L. -
第11题:
问答题A、B两种气态烃,标准状况下A的密度为1.25g/L,将总质量为4.4g的A、B混合气体4.48L(标准状况下)通入足量的溴的四氯化碳溶液中,充分反应后,溴的四氯化碳溶液的质量增加了2.8g.试求A、B是什么气体?正确答案: A:乙烯;B:甲烷解析:
由于标准状况下烃A的密度为1.25g/L,可知A的相对分子质量M=1.25g/L×22.4L=28g/mol,所以A为乙烯;混合气体体积4.48L,即0.2mol,通入足量的溴的四氯化碳溶液中,乙烯被吸收,因为溴的四氯化碳溶液的质量增加了2.8g,可知原气体中含有0.1mol乙烯,另含有0.1mol B气体,质量为1.6g,即B的相对分子质量为16g/mol,即B为甲烷. -
第12题:
单选题下列物质所含分子数最多的是( ).A标准状况下,3mol二氧化碳
B标准状况下,49g氢气
C标准状况下,22.4L二氧化碳(标态)
D4℃时,11.2L水
正确答案: B解析:
标准状况下,3mol二氧化碳所含的分子数为3NA;49g氢气所含分子数为24.5NA,22.4L二氧化碳所含分子数为1NA,4℃时11.2L水所含分子数为622.2NA. -
第13题:
足量盐酸与250g碳酸钙反应,生成二氧化碳的质量是多少?
解:设可以生成二氧化碳的质量为x。 CaCO3+2HCl=CaCl2+H2O+CO2↑ 100 44 250g x 100/44=250g/x x=110g 答:可以生成二氧化碳110g 。 -
第14题:
某工厂利用废铁屑与废硫酸反应制取硫酸亚铁。现有废硫酸9.8t(H2SO4的质量分数为20%),与足量的废铁屑反应,可生产FeSO4的质量是多少?
解:设可生产FeSO4的质量为x。 答:可生产3.04t FeSO4 -
第15题:
某气态烃中各元素的质量分数为C:85.72%,H:14.28%。在标准状况下的密度是2.5g/L,该烃能使酸性高锰酸钾溶液或溴水褪色。求该烃的分子式和名称。答案:解析:
-
第16题:
.6g Na2CO3·10H2O与质量分数为36.5%(密度1.19g/cm3)的盐酸完全反应,消耗这种盐酸溶液多少毫升?在标准状况下,反应答案:解析:
-
第17题:
空气中二氧化碳浓度为0.10%,该浓度在标准状况下的质量浓度为()。
- A、1.96mg/m3
- B、1960mg/m3
- C、0.020mg/m3
- D、510mg/m3
- E、百分浓度未注明是否在标准状况无法计算
正确答案:B -
第18题:
在标准状况下,与12gH2的体积相等的N2的()。
- A、质量为12g
- B、物质的量为6mol
- C、体积为22.4L/mol
- D、物质的量为12mol
正确答案:B -
第19题:
在标准状况下,相同质量的下列气体中体积最大的是()
- A、氧气
- B、氮气
- C、二氧化碳
- D、二氧化硫
正确答案:B -
第20题:
已知在标准状况下1体积的水可吸收560体积的氨气,此氨水的密度为0.90g·mL-1,求此氨溶液的质量分数和物质的量浓度是()、()。
正确答案:0.298;15.8mol·L-1 -
第21题:
填空题燃烧2.2克某气态烃,生成0.15mol二氧化碳和3.6克水.在标准状况下,该气态烃对氢气的相对密度是22,则该气态烃的分子式为____.正确答案: C3H8解析:
设该气态烃的分子式为CxHy,3.6克的水就是0.2mol的H2O,其中有0.4mol的H;0.15mol的二氧化碳中有0.15mol的C,该气态烃的相对分子质量为22×2=44,则烃的物质的量为2.2/44=0.05mol,所以CxHy中C:H=3:8,则该气态烃为丙烷C3H8. -
第22题:
填空题在标准状况下,与6.4g氧气体积相等的二氧化碳的物质的量为____,质量为____,它们的体积为____.正确答案: 0.2mol,8.8g,4.48L解析:
标准状况下6.4g氧气的物质的量为0.2mol,,因此与之体积相等的二氧化碳的物质的量为0.2mol,质量为8.8g,体积为4.48L. -
第23题:
单选题在标准状况下,有一氧化碳和二氧化碳的混合气体5.6L,如果一氧化碳的质量是5.6g,则二氧化碳的质量是( ).A5.6g
B44g
C2.2g
D1g
正确答案: A解析:
由题意知混合气体总的物质的量0.25mol,一氧化碳的物质的量为0.2mol,所以二氧化碳的物质的量0.05mol,代入即得二氧化碳的质量.
