白色固体粉末氯酸钾(KClO3),在二氧化锰(MnO2)作催化剂并加热的条件下能较快地分解成氯化钾和氧气,试写出该反应的化学方程式。
题目
白色固体粉末氯酸钾(KClO3),在二氧化锰(MnO2)作催化剂并加热的条件下能
较快地分解成氯化钾和氧气,试写出该反应的化学方程式。
相似考题
更多“白色固体粉末氯酸钾(KClO3),在二氧化锰(MnO2)作催化剂并加热的条件下能较快地分解成氯化钾和氧气,试写出该反应的化学方程式。”相关问题
-
第1题:
下列有关催化剂的叙述正确的是( )
A.二氧化锰是所有反应的催化剂
B.加入二氧化锰能使双氧化分解放出的氧气总量增加
C.催化剂能增大化学反应的速率,而本身质量和化学性质在反应前后都不变
D.要使双氧水分解放出氧气,必须要加入二氧化锰,否则反应就不能发生
正确答案:C
C -
第2题:
写出镁、铜、氧气、盐酸两两间能发生反应的化学方程式,并注明反应类型。
2Mg+O2 点燃 2MgO (化合反应) Mg+2HCl=MgCl2+H2↑(置换反应) 2Cu+O2 加热 2CuO (化合反应) -
第3题:
请教:2009年自治州恩施州初中毕业生学业考试化学试题第3大题第1小题如何解答?【题目描述】
第 1 题在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产生气体为止,收集到一定质量的氧气。某化学兴趣小组欲求得所制氧气的质量,他们将加热后剩余物冷却到一定温度后,通过多次加水测定剩余物质量的办法即可求出。加水的质量与剩余固体的质量见下表:(MnO2是不溶于水的固体粉末)
试求:(1)表中m值为_____________ 。编号
1 2 3 4 加水的质量(g) 10 10 10 10 剩余固体的质量(g) 7.25 4.05 m 3 (2)所制得氧气的质量。
【参考答案分析】:
3 (由1和2可知加入10g水最多溶解3.2g KCl,而第三、第四次加水后溶解KCl为4.05g-3g﹤3.2g,则第三次加水后KCl完全溶解,剩余的固体全部是不溶于水的MnO2,则m=3,原混合物中KClO3为15.25g-3g=12.25g 。 ) (1分)
解:(2) 设可制得氧气的质量为x
2KClO32KCl + 3O2↑
245 96
15.25g-3g x (2分)

答:可制得氧气4.8克。 (2分)
-
第4题:
在催化剂中,能够使化学反应加快速度的称为正催化剂,使化学反应速度减慢的称为负催化剂,下列属于负催化剂的是( )。
A.为防止食用油脂酸化而加入的没食子酸正丙脂
B.在分解氯酸钾制备氧气实验时加入的二氧化锰
C.在用锌和稀硫酸反应制备氧气时加入的硫酸铜
D.在大雪后为促使积雪融化而在马路上撒下的盐答案:A解析:A项,没食子酸正丙脂的作用是减慢食用油脂酸化的速度,属于负催化剂,符合题意,当选。
B项,二氧化锰能加快氯化钾的分解速度,属于正催化剂,不符合题意,排除。
C项,硫酸铜能加快锌和稀硫酸的反应,属于正催化剂,不符合题意,排除。
D项,盐能加快积雪的融化速度,属于正催化剂,不符合题意,排除。
故本题答案为A选项。 -
第5题:
阅读下列三段材料,按要求完成任务。
材料一《义务教育化学课程标准(2011年版)》关于制取氧气的内容标准:初步学习氧气的实验室制取方法。
材料二教科书的知识结构体系
绪言化学使世界变得更加绚丽多彩
第一单元走进化学世界
第二单元我们周围的空气
课题1空气
课题2氧气
课题3制取氧气
实验活动l氧气的实验室制取与性质
第三单元物质构成的奥秘
第四单元自然界的水
第五单元化学方程式
第六单元碳和碳的氧化物
第七单元燃料及其利用
第八单元金属和金属材料
第九单元溶液
第十单元酸和碱
第十一单元盐化肥
第十二单元化学与生活
材料三某版本教科书“制取氧气”所呈现的部分内容:
课题3制取氧气
在实验室里.常采用加热高锰酸钾、分解过氧化氢或加热氯酸钾的方法制取氧气。
【实验2—5】
把少量高锰酸钾装入试管中,并在试管口放一团棉花,用带有导管的塞子塞紧试管。
(1)加热试管,用排水法收集一瓶氧气(如图2—14)。
(2)把带有火星的木条伸入集气瓶中,观察有什么现象发生。
高锰酸钾是一种暗紫色的固体,它受热时,分解出氧气,同时还有锰酸钾和二氧化锰生成:
除用加热高锰酸钾的方法制取氧气外.在实验室里还常常用分解过氧化氢的方法制取氧气。过氧化氢溶液在常温下可以分解放出氧气.但是在利用过氧化氢分解制取氧气时,通常还要放入少量二氧化锰.这是为什么呢?
【探究】
分解过氧化氢制氧气的反应中二氧化锰的作用
1.实验
(1)在试管中加入5 ml 5%过氧化氢溶液,把带火星的木条伸入试管,观察现象。
(2)向上述试管中加入少量二氧化锰,把带火星的木条伸入试管。观察现象(如图2一15)。
(3)待上述试管中没有现象发生时,重新加入过氧化氢溶液,并把带火星的木条伸入试管,观察现象。待试管中又没有现象发生时,再重复上述操作.观察现象。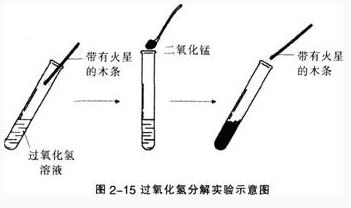
2.分析与讨论
(1)在实验(1)和(2)中木条是否复燃?发生这种现象的原因可能是什么?
(2)在实验(3)的重复实验中,反应后二氧化锰有无变化?
(3)综合分析实验(1)一(3)中所观察到的现象,你认为二氧化锰在过氧化氢分解的反应中起了什么作用?
在实验(1)中,带火星的木条不能复燃,是因为过氧化氢溶液在常温下分解缓慢.放出的氧气很少。在实验(2)中,木条复燃,是因为过氧化氢溶液中加入少量二氧化锰,使分解加速。这一反应可以表示如下:
在实验(3)中,实验重复多次,每次只消耗了过氧化氢,二氧化锰好像永远用不完。如果在实验前用精密的天平称量二氧化锰的质量,实验后把二氧化锰洗净、干燥.再称量,你会发现它的质量没有发生变化。把它再加到过氧化氢溶液中.还可以加速过氧化氢分解。这种在化学反应里能改变其他物质的化学反应速率.而本身的质量和化学性质在反应前后都没有发生变化
的物质叫作催化剂(又叫触媒)。催化剂在化学反应中所起的作用叫作催化作用。硫酸铜溶液等对过氧化氢的分解也具有催化作用。
催化剂在化工生产中具有重要而广泛的应用,生产化肥、农药、多种化工原料等都要使用催化剂。
在实验室里还可以通过加热混有二氧化锰的氯酸钾固体制取氧气.除生成氧气外,同时还有一种叫氯化钾的物质生成。二氧化锰在这一反应中也是催化剂。这个反应可表示如下:
【讨论】
分析上述三个制取氧气的反应,它们有什么共同特征?与化舍反应有什么不同?
要求:
(1)试对本课内容进行学情分析。
(2)确定本课的三维教学目标。
(3)确定本课的教学重点和难点。
(4)试对本课内容进行教学价值分析。
(5)设计本课教学内容的教学过程图。答案:解析:【知识点】化学教学设计能力——制取氧气
(1)通过前面的学习,学生对氧气的性质和用途有了较为深入的认识,对氧气产生了浓厚的探究欲望.他们渴望能亲手制得一瓶纯净的氧气。通过操控化学反应制备得到一种物质,对学生而言是一件神奇的事情。
学生对物质制备的认识仅限于从小学自然课、生活经验等途径获得的零星的、感性的体验.还不能形成系统的、理性的思考。同时,学生的化学知识、实验技能、探究能力也都处在初级阶段,对如何分析和处理实验中遇到的问题会感到束手无策。因此,氧气的实验室制法,在帮助学生顺利获得氧气的同时,要注意制备物质的思路的总结和落实。
(2)知识与技能:①知道实验室用过氧化氢、氯酸钾、高锰酸钾制取氧气的原理,能写出文字表达式:②能识别固体药品制备气体和液体药品制备气体的整套实验装置;③了解催化剂,能解释证明催化作用的对比实验;④在制备氧气的过程中,进行装置气密性检验、药品的取用、物质的加热、排水取气等基本实验操作的训练,能检验氧气的生成。
过程与方法:①通过制备氧气的过程,初步学习通过化学实验制备物质的一般思路方法;②通过催化剂作用的有关实验,进一步理解对比和变量控制的方法在化学实验中的应用。
情感态度与价值观:①通过实验活动获得氧气,感受实验成功的快乐,感受个人对自然改变的力量:②通过化学变化获得氧气,建立物质间可以转化的观念,加深化学对人类伟大贡献的理解。
(3)教学重点:氧气实验室制法的原理和装置。
教学难点:制备物质的一般思路和方法的建立。
(4)①物质制备是实验化学的重要研究内容,也是人类利用化学改变社会的重要方式,氧气实验室制法的学习是学习研究物质制备的启蒙和基础。
②氧气实验室制法涉及的两套实验装置都是实验化学气体制备的基本装置,在制备很多气体时可以应用。
③学习前.学生知道空气中有氧气,我们的身边充斥着氧气,但是他们没有获得过纯净的氧气。如果需要得到氧气,学生首先想到的是物理方法,即从空气中分离。通过学习,学生获得了纯净的氧气.虽然外观上与空气没什么不同,但是这个过程会增强学生对自然的能动感,感受到科学的力量。通过化学方法制得氧气,能够促使学生建立物质转化的观点。在制备氧气的过程中形成制备物质的思路方法,这是学生后续学习的基础以及解决制备问题的基本途径。
(5)教学流程图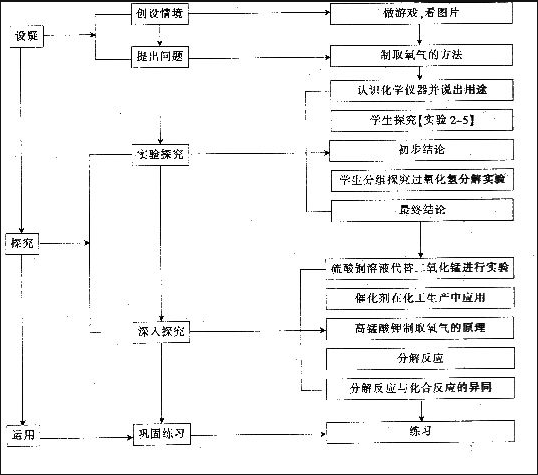
-
第6题:
在用二氧化锰和氯酸钾混合加热制取氧气的反应中,二氧化锰是氧化剂。
正确答案:错误 -
第7题:
下列固体加热制气体的装置试管口向下倾斜的是()
- A、没有加入MnO2的KClO3加热制氧气
- B、氯化汞加热制氧气
- C、草酸晶体加热制气体
- D、用氯化铵和碱石灰加热制氧气
正确答案:C -
第8题:
下列化学反应与实验现象相符合的是()
- A、硫在空气中燃烧——蓝紫色火焰
- B、木炭在空气中燃烧——生成有刺激性气味的气体
- C、镁在氧气中燃烧——生成白色固体
- D、氯酸钾受热分解——生成氧气
正确答案:C -
第9题:
下列关于金属钠性质的描述,正确的是()。
- A、金属钠不能直接与硫反应
- B、金属钠在空气中燃烧,生成白色的氧化钠粉末
- C、金属钠能直接与氯气化合
- D、碱金属与氧气在燃烧的情况下反应,生成过氧化钠白色固体
正确答案:C -
第10题:
写出锰在氧化剂存在下,同熔融碱反应的化学方程式()反应前后由灰色粉末变成()色.
正确答案:熔融2Mn+4KOH+3O2========2K2MnO4+2H2O;绿色 -
第11题:
单选题下列固体加热制气体的装置试管口向下倾斜的是()A没有加入MnO2的KClO3加热制氧气
B氯化汞加热制氧气
C草酸晶体加热制气体
D用氯化铵和碱石灰加热制氧气
正确答案: C解析: 暂无解析 -
第12题:
填空题实验室用浓盐酸跟MnO2反应制取氯气时,MnO2是____剂;用KClO3制取氧气时,MnO2是____剂.正确答案: 氧化剂,催化剂解析:
浓盐酸与MnO2反应制取氯气的反应中,氯离子失电子,作为还原剂,二氧化锰得电子作为氧化剂;在加热KClO3制取氧气的反应中,二氧化锰本身不参与反应,因此属于催化剂. -
第13题:
长期盛放澄清石灰水的试剂瓶内壁往往附着一层白色固体。这层白色固体是怎样
形成的?主要成分是什么?石灰水用完以后,如何除去瓶壁上的白色固体?写出
有关反应的化学方程式。
白色固体是氢氧化钙与空气中的二氧化碳反应生成的,主要成分为碳酸钙,石灰水用完后,加盐酸可除去瓶壁 上的白色固体。 CaCO3+2HCl=CaCl2+H2O+CO2↑ -
第14题:
在某些食品的包装袋内有一个装有白色颗粒状固体的小纸袋,上面写着“干燥剂,主要成分为生石灰”(如右图)。为什么生石灰能作干燥剂?如果将小纸袋拿出来放在空气中,经过一段时间后,会发现纸袋内的白色颗粒黏在一起成为块状。这是为什么?试写出有关反应的化学方程式。
①由于生石灰和水反应生成Ca(OH)2, 所以可做干燥剂。由于CaO能吸收 空气中的水分,生成Ca(OH)2。而 Ca(OH)2又能继续与空气中的C02 反应,生成难溶性的CaCO3,所以 结块。 ②CaO+H2O=Ca(OH)2 Ca(OH)2+CO2=CaCO3↓+H2O -
第15题:
在实验室制取氧气时,取MnO2和KClO3的固体混合物15.25g,加热至不再产生气体为止,收集到一定质量的氧气。某化学兴趣小组欲求得所制氧气的质量,他们将加热后剩余物冷却到一定温度后,通过多次加水测定剩余物质量的办法即可求出。加水的质量与剩余固体的质量见下表:(MnO2是不溶于水的固体粉末)
编号 1 2 3 4 加水的质量(g) 10 10 10 10 剩余固体的质量(g) 7.25 4.05 m 3试求:(1)表中m值为_____________ 。
(2)所制得氧气的质量。
正确答案:
3 (由1和2可知加入10g水最多溶解3.2g KCl,而第三、第四次加水后溶解KCl为4.05g-3g﹤3.2g,则第三次加水后KCl完全溶解,剩余的固体全部是不溶于水的MnO2,则m=3,原混合物中KClO3为15.25g-3g=12.25g 。 ) (1分)
解:(2) 设可制得氧气的质量为x
2KClO32KCl + 3O2↑
245 96
15.25g-3g x (2分)
答:可制得氧气4.8克。 (2分) -
第16题:
颗粒大小达到纳米级的单质铁具有很强的反应活性,俗称“纳米铁”。
⑴在高温条件下,用H2与FeCl2反应,可生成“纳米铁”和一种溶于水显强酸性的气体,写出该反应的化学方程式( ) 。
⑵“纳米铁”在空气中受撞击时会燃烧,其反应与铁在纯氧中燃烧相同,写出该反应的化学方程式( ) 。
⑶请你预测“纳米铁”的其他化学性质,用化学反应方程式表示( ) 。答案:解析:
-
第17题:
计算题:在催化剂作用下把490g氯酸钾加热使之完全溶解,标准状况下可得氧气多少升?
解:设可得氧气VL
2KClO=32KCl+3O2↑
2 3
490/122.5 V/22.4
即2:3=(490/122.5):(V/22.4)
则V=(3×490×22.4)÷(122.5×2)=134.4(L)
答:标准状况下可得氧气134.4L。
略 -
第18题:
实验室中加热氯酸钾以制取氧气时,要加一些二氧化锰,这是因为:()?
- A、二氧化锰不起作用
- B、二氧化锰促进氯酸钾分解
- C、二氧化锰极易分解
正确答案:B -
第19题:
固体KClO3是强()剂,KClO3溶液与KI溶液(),加稀硫酸后,并使KI溶液过量,则反应的主要产物是();若在酸性条件下,过量的KClO3与KI溶液反应的主要产物是()。
正确答案:氧化;不反应;I3-,Cl-;IO3-,Cl2 -
第20题:
加热氯酸钾制氧气时,错把高锰酸钾当作二氧化锰放入氯酸钾内,其结果与只加热氯酸钾相比,正确的是()。
- A、反应速率不变
- B、生成氧气质量不变
- C、反应速率加快,生成氧气质量不变
- D、反应速率加快,生成氧气质量增加
正确答案:D -
第21题:
加热氯酸钾制取氧气时,为什么要加入少量二氧化锰?
正确答案: 加入少量二氧化锰可以起催化作用,使氯酸钾在较低温度下就可以迅速分解放出氧气. -
第22题:
往某无色溶液中加入氯化钡溶液,生成不溶于硝酸的白色沉淀,试简答分析该无色溶液中可能含有的化合物类别是什么?并写出有关反应的化学方程式。
正确答案: 无色溶液可能是硫酸或硫酸盐溶液,也可能是硝酸银溶液.BaCl2+H2SO4==BaSO4↓+2HCl
BaCl2+Na2SO4==BaSO4↓+2NaCl
2ANO3+BaCl2==2AgCl↓+Ba(NO3)2 -
第23题:
单选题有m克KClO3与2克MnO2混合加热,完全反应后剩余固体残余物n克,则生成氧气的质量是( ).A(m-n)克
B(m-2-n)克
C(m+2-n)克
D(n-2)克
正确答案: D解析:
根据质量守恒定律,反应前反应物的质量等于反应后生成物的质量,由此得到生成氧气的质量m+2-n.
