在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:物质甲乙丙丁反应前的质量(g)20508030反应后的质量(g)010010x请根据质量守恒定律判断x的值A.50 B.40 C.10 D.70
题目
在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:
物质
甲
乙
丙
丁
反应前的质量(g)
20
50
80
30
反应后的质量(g)
0
100
10
x
请根据质量守恒定律判断x的值
A.50 B.40 C.10 D.70
相似考题
更多“在一密闭容器中,有甲、乙、丙、丁四种物质,一定条件下充分反应,测得反应前后各物质的质量如下表:物质甲乙丙丁反应前的质量(g)20508030反应后的质量(g)010010x请根据质量守恒定律判断x的值A.50 B.40 C.10 D.70”相关问题
-
第1题:
甲是初中化学中的常见物质。请根据下列叙述回答问题。
(1)若甲既能与稀盐酸反应生成X,又能与氢氧化钙溶液反应生成Y,且X与Y能反应。则甲的化学式可能是_______(写出一种即可),X与Y反应的化学方程式为______________。
(2)若甲能与水反应,将少量甲加到饱和石灰水中,溶液变浑浊,则下列说法正确的是______ (填序号)。
A.甲一定是二氧化碳 B.反应后溶质的质量一定减少
C.反应前后溶剂的质量保持不变 D.反应前后溶液中溶质的质量分数可能不变
(3)若甲可用于焊接或切割金属,把一定质量的纯净物A和40 g的纯净物B在一定条件下按下图所示充分反应,当B物质反应完时,可生成44g C物质和9 g D物质。
①参加反应的甲物质的质量是________。
②甲物质中各元素的质量比为________。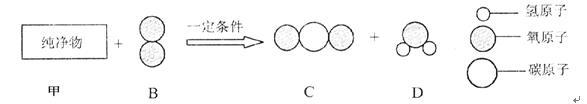 答案:解析:(1)碳酸钠 CO2+2NaOH=Na2CO3+H2O(2)BD(3)①13g ②碳、氢元素质量比为12:1
答案:解析:(1)碳酸钠 CO2+2NaOH=Na2CO3+H2O(2)BD(3)①13g ②碳、氢元素质量比为12:1 -
第2题:
一定条件下,3.4g甲物质和4.8g氧气恰好完全反应,生成5.4g乙物质和另一物质X。下列判断不正确的是( )。
 A.物质甲的化学式是NH3
A.物质甲的化学式是NH3
B.物质X的质量为2.8g
C.物质X含两种元素
D.该反应的化学方程式中物质X与O2的化学计量数之比为2:3答案:C解析:
-
第3题:
在一密闭容器中,反应aA(g)?bB(g)达平衡后,保持温度不变,将容器体积增加一倍,当达到新的平衡时,B的浓度变为原来的60%,则(?? ) ??A.平衡向逆反应方向移动了
B.物质A的转化率增大了
C.物质B的质量分数减小了
D.a>B.答案:B解析:先假设体积增加一倍时若平衡未移动,B的浓度应为原来的50%,实际平衡时B的浓度是原来的60%,比假设大,说明平衡向生成B的方向移动,即减小压强平衡向正反应方向移动,则a<b,
A、假设体积增加一倍时若平衡未移动,B的浓度应为原来的50%,实际平衡时B的浓度是原来的60%,大于原来的50%,说明平衡向生成B的方向移动,即向正反应移动,故A错误;
B、根据A的判断,平衡向正反应移动,反应物转化率增大,故B正确;
C、平衡向正反应移动,B的质量增大,混合气体的总质量不变,故物质B的质量分数增大,故C错误;
D、根据A的判断,平衡向生成B的方向移动,则a<b,故D错误;
故选B -
第4题:
一定温度下,在三个容积均为2.0 L的恒容密闭容器中发生反应:
各容器中起始物质的量浓度与反应温度如表1所示,反应过程中甲、丙容器中 C02的物质的量随时间变化关系如图2所示: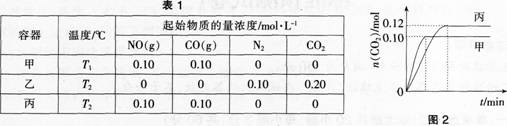
下列说法正确的是( )。
A.该反应的正反应为吸热反应
B.乙容器中反应达到平衡时,N2的转化率小于40%
C.达到平衡时,乙容器中的压强一定大于甲容器的2倍
D.丙容器中反应达到平衡后,再充入0.10 mol N0和0.10 molC02,此时v(正)<v(逆)答案:B解析:
中的气体相当于甲中气体的2倍,建立平衡后,相当于甲平衡后增大压强,平衡向右移动.气体的物质的量减少,压强小于甲容器的2倍,C项错误;丙容器中反应达到平衡后,再充人0.10 mol NO和0.10 mol CO2.相当于增大压强,平衡正向移动,此时υ(正)大于υ(逆),D项错误;故本题选B。 -
第5题:
对质量守恒定律的正确理解是()。
- A、参加反应的各种物质的质量不变
- B、化学反应前后各物质的质量不变
- C、化学反应前的各物质质量总和等于反应后生成的各物质质量总和
- D、参加化学反应的各物质质量总和与反应后生成的各物质质量总和相等
正确答案:D -
第6题:
在某化学反应中,下列说法正确的是()。
- A、参加化学反应的各物质,等于反应后生成的各种物质
- B、参加化学反应的反应物,等于反应后生成的生成物
- C、参加化学反应的各物质质量之和,等于反应后生成的各种物质质量之和
- D、参加化学反应的各种反应物质量之和,等于反应后生成的各种生成物质量之和
正确答案:C,D -
第7题:
化学反应前后各物质的质量总和不一定相等。
正确答案:错误 -
第8题:
质量守恒定律指的是反应前后物质的质量不发生变化。
正确答案:错误 -
第9题:
参加化学反应的各物质的质量总和等于反应后生成的各物质质量总和。
正确答案:正确 -
第10题:
质量守恒定律是指反应前参加反应的各物质的()等于反应后生成物的()。
正确答案:总质量;总质量 -
第11题:
判断题化学反应前参加反应的各物质的总质量等于反应后生成物各物质的总质量。A对
B错
正确答案: 错解析: 暂无解析 -
第12题:
填空题质量守恒定律是指反应前参加反应的各物质的()等于反应后生成物的()。正确答案: 总质量,总质量解析: 暂无解析 -
第13题:
将一定量的丙醇(C3H8O)和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表: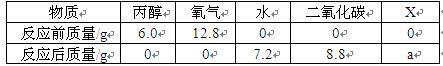
下列判断正确的是( )A.表中a的值为2.8
B.X一定是该反应的催化剂
C.X可能含有氢元素
D.若起始时氧气的质量是14.4g,则无X生成答案:A,D解析: -
第14题:
某些气体分子的微观示意图如表1所示:
表1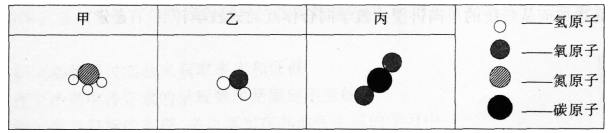
一定条件下,3.4g甲物质和4.8g氧气恰好完全反应,生成5.4g乙物质和另一物质X。下列判断不正确的是( )。
A.物质甲的化学式是NH3
B.物质X的质量为2.8 g
C.物质X含两种元素
D.该反应的化学方程式中物质X与02的化学计量数之比为2:3答案:C解析:

-
第15题:
密闭的容器内有A、B、C、D四种物质,在一定条件下充分反应,测的反应前后各物质的质量如表1所示。( )。
表1 反应前后各物质的质量
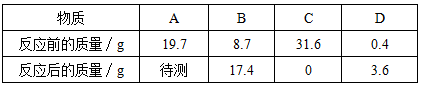 A.物质C可能是化合物,物质D一定是单质
A.物质C可能是化合物,物质D一定是单质
B.该反应属于复分解反应
C.反应过程中,物质B与物质D变化的质量比为87:32
D.反应后,密闭的容器中A的质量为19.7g答案:C解析:通过计算可得A物质反应后的质量为39.4克,此反应为分解反应,从题目的信息不能判断反应物与产物是化合物还是单质,因此不能确定是否为置换反应。 -
第16题:
化学反应前参加反应的各物质的总质量等于反应后生成物各物质的总质量。
A对
B错
对
略 -
第17题:
参加化学反应的各物质的质量总和不等于反应后生成的各物质的质量总和。
正确答案:错误 -
第18题:
甲、乙、丙三种物质各6g放在密闭的容器中,充分反应后测得容器内只剩甲、乙两种物质,其中甲为16g,乙的质量是()
- A、2g
- B、4g
- C、lOg
- D、16g
正确答案:A -
第19题:
化学反应前参加反应的各物质的总质量等于反应后生成物各物质的总质量。
正确答案:正确 -
第20题:
甲、乙、丙三种物质各6g放在密闭的容器中,充分反应后测得容器内只剩甲、乙两种物质,其中甲为16g,乙的质量是()。
- A、2g
- B、4g
- C、l0g
- D、16g
正确答案:A -
第21题:
在化学反应中,参加反应的各物质的质量总和等于反应后生成各物质的质量总和。()
正确答案:正确 -
第22题:
为什么反应前后各物质的质量总和一定相等?
正确答案: 在一切化学反应前后,原子的种类没有改变,各种原子的数目也没有增减,所以化学反应前后各物质的质量总和一定相等. -
第23题:
问答题根据下列材料,按要求完成任务。下列是某初中化学教师有关“质量守恒定律”的教学片段。 [教师]一天,小明看到蜡烛在燃烧的过程中会逐渐变短,这时他提出了一个问题:“为什么蜡烛在燃烧的过程中会逐渐变短?” [教师]化学反应前与化学反应后各物质的质量总和相比较,存在怎样的关系?猜想1:大于:猜想2:等于:猜想3:小于。 [分组实验]白磷燃烧前后质量的测定(A组)。硫酸铜溶液跟铁钉反应前后质量的测定(B组)。 [实验要求]认真记录实验现象、反应前后的总质量,并对实验结果进行分析。根据实验现象进行讨论,归纳,对实验做小结,得出结论。 [结果分析]反应前、后物质总质量是否发生变化?不变。 [教师]质量守恒定律:参加化学反应的各物质的质量总和,等于反应后生成的各物质的质量总和,这个规律就叫作质量守恒定律。 要求: (1)写出本课的教学目标。 (3)写出本课的教学主题。 (4)针对本课内容,设计两个反思作业题目。正确答案: (1)教学目标:①知识与技能:认识质量守恒定律,说出常见化学反应中的质量关系。②过程与方法:能用微粒的观点对质量守恒定律做出解释:能用质量守恒定律解释一些现象。③情感态度与价值观:反思我们对质量守恒定律的认识过程,并将其与人类发现质量守恒定律的历程进行比较,说明“定律”产生和发展的实质。
(2)教学方法:反思型探究活动和科学史料显性教学相结合。
(3)教学主题:
①运用已有知识推测得出参加化学反应的各物质的质量总和可能是守恒的;
②检验我们的推测是否合理;
③运用质量守恒定律解释一些实验现象;
④反思比较我们的认识过程与定律产生的过程。
(4)反思作业:
①在定律形成的过程中,实验、推理所起的作用是什么?实验、定律和推理三者之间有何关系?
②科学家把质量守恒定律和能量守恒定律合二为一,称为质能守恒定律。你从这个定律的发展得到什么启示?解析: 暂无解析
