问答题试计算10mol/L的稀盐酸溶液的PH值?
题目
相似考题
参考答案和解析
则(X+1×10)X=1×10
X+10X-10=0
X=0.995×10
P[OH]=7.002的PH=14-POH=6.998
更多“问答题试计算10mol/L的稀盐酸溶液的PH值?”相关问题
-
第1题:
有甲、乙两个不同浓度的同一有色物质的溶液,用同一厚度的比色皿,在同一波长下测得的吸光度分别为:甲0.20;乙0.30。若甲的浓度为4.0×10
 mol/L,则乙的浓度为
mol/L,则乙的浓度为A、8.0×10
 mol/L
mol/LB、2.0×10
 mol/L
mol/LC、4.0×10
 mol/L
mol/LD、6.0×10
 mol/L
mol/LE、3.0×10
 mol/L参考答案:D
mol/L参考答案:D
-
第2题:
将0.65g锌全部溶于200 mL稀盐酸中,然后加入80 mL 0.5 mol/L AgNO3溶液,恰好使Cl-沉淀完全。试计算:
(1)产生多少升(标准状况下)氢气。
(2)原稀盐酸的物质的量浓度为多少。答案:解析:
-
第3题:
常温下,在CH3COOH与CH3COONa的混合溶液中,若它们的浓度均为0. 10mol*L-1,测得pH是4.75,现将此溶液与等体积的水混合后,溶液的pH值是:A.2.38
B.5.06
C.4.75
D.5.25答案:C解析:
-
第4题:
c(NaOH)=0.0001mol/L的NaOH溶液的pH值为();c(HCl)=0.01mol/L的HCl溶液的pH值为()。
10;2
略 -
第5题:
细菌内毒素检查对供试品溶液的PH值没有要求。
正确答案:错误 -
第6题:
以下配制表述正确的是()。
- A、配制标准缓冲液和供试品溶液的水应是新沸过的热蒸馏水
- B、配制标准缓冲液和供试品溶液的水pH值应为5.0~7.0
- C、测定pH前要对仪器校正,校正时选择二种pH值相差3个单位的标准缓冲溶液
- D、测定pH前要对仪器校正,校正时选择二种pH值相差2个单位的标准缓冲溶液
- E、测定高pH值的供试品时,应注意酸误差的影响
正确答案:C -
第7题:
计算CKOH=0.0200mol/L的KOH溶液的PH值?
正确答案: OH=-lg0.0200=-lg2×10-2=-lg2+(-lg10-2)=1.70
PH=14-1.70=12.30
H值为12.30。 -
第8题:
计算题:计算0.01mol/LNaOH溶液的PH值。
正确答案:解:∵NaOH是强电解质,在溶液中完全电离
∴0.01mol/LNaOH溶液的〔OH-〕=0.01mol/L
=1(×)10-2mol/L
POH=-lg〔OH-〕=-lg(1×10-2)=2
∴PH=14-POH=14-2=12 -
第9题:
用玻璃电极作指示电极,以0.2mol·L-1的氢氧化钠溶液电位滴定0.0200mol·L-1的苯甲酸溶液,从滴定曲线上求得终点时溶液的pH为8.22,二分之一终点时溶液的pH为4.18,试计算苯甲酸的离解常数。
正确答案: 设HA为苯甲酸,其解离常数Ka=c(H3O+)c(A-)/c(HA)
二分之一终点时,c(HA)=c(A-)/Ka=c(H3O+)
PKa=pH=4.18 Ka=6.6×10-5
苯甲酸的离解常数Ka=6.6×10-5。 -
第10题:
计算题:已知NaOH溶液的浓度为400mg/L,求此溶液的PH值。
正确答案: 解:[OH-]=400÷1000÷40=0.01(mol/L)
POH=-lg[]OH-]=-lg0.01=2PH=14-POH=14-2=12
此溶液的PH值为12。 -
第11题:
问答题求0.001mol/L的氢氧化钠溶液的pH值和pOH值正确答案: pOH=-lg[OH-]=-lg0.001=3
pH=14-pOH=14-3=11解析: 暂无解析 -
第12题:
问答题计算0.25mol/L的组氨酸溶液在pH6.4时各种离子形式的浓度(mol/L)。正确答案: 解:
由pH=pK1+lg(His2+/10-6.4)=pKr+lg(His+/His2+)=pK2+lg(His0/ His+) 得His2+为1.78×10-4,His+为0.071,His0为2.8×10-4解析: 暂无解析 -
第13题:
以下表述正确的是
A.配制标准缓冲液和供试品溶液的水应是新沸过的热蒸馏水
B.配制标准缓冲液和供试品溶液的水pH值应为5.0~7.0
C.测定pH前要对仪器校正,校正时选择二种pH值相差3个单位的标准缓冲溶液
D.测定pH前要对仪器校正,校正时选择二种pH值相差2个单位的标准缓冲溶液
E.测定高pH值的供试品时,应注意酸误差的影响
正确答案:C
《中国药典》规定配制标准缓冲液和供试品溶液的水应是新沸过的冷蒸馏水,其pH值应为5.5~7.O。《中国药典》规定,测定pH前要对仪器校正,校正时应选择二种pH值相差3个单位的标准缓冲溶液,使供试品溶液的pH值处于二者之间。测定高pH值的供试品时,应注意碱误差的影响.因为当pH>9时,普通玻璃电极对Na+也有影响,使测得的pH值高于真实值。
-
第14题:
常见人体水解酶对其天然底物K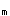 值A.与其他合成底物的K
值A.与其他合成底物的K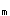 值相同
值相同
B.<10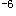 mol/L
mol/L
C.>1mol/L
D.>10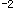 mol/L
mol/L
E.在10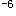 mol/L~10
mol/L~10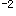 mol/L之间答案:E解析:
mol/L之间答案:E解析: -
第15题:
计算0.1mol/L(NaOH)氢氧化钠溶液的PH值?
NaOH为强碱,全部电离
NaOH→Na++OH-
POH=-lg[OH-]=-lg(10-1)=1
PH=14-1=13
求得0.1mol/L(NaOH)氢氧化钠溶液的PH值为13。
略 -
第16题:
试计算10mol/L的稀盐酸溶液的PH值?
正确答案: 因为此溶液为盐酸的极稀溶液此时PH值的计算应考虑溶液中水的电离所产生的[];设水离解产生的[]为Xmol/L,aH+=XmoL/L
则(X+1×10)X=1×10
X+10X-10=0
X=0.995×10
P[OH]=7.002的PH=14-POH=6.998 -
第17题:
将PH=1.0的强酸溶液与PH=13.0的强碱溶液等体积混合,计算混合后溶液的PH值。
正确答案:解:因为PH=13.0则POH=14-13=1[OH-]=10-1
PH=1[H+]=10-1
由于[OH-]=[H+]=10-1所以反应后生成水,则PH为7
答:混合后溶液的PH值为7。 -
第18题:
氢离子浓度等于10-3mmol/L时,溶液的PH值是(),氢氧根离子浓度等于10-3mmol/L时,溶液的PH值是()。
正确答案:3;11 -
第19题:
计算0.095mol/LNaOH溶液的PH值。
正确答案: 0.095mol/LNaOH溶液中[OH-]=9.5×10-2(mol/L)POH=—lg[OH-]=—lg9.5×10-2=2—lg9.5=2—0.92=1.02PH=14—1.02=12.98 -
第20题:
计算题:某溶液中的〔H+〕为0.00001mol/L,PH值为多少?
正确答案: 解:〔H+〕=0.00001=10-5 PH=-lg〔H+〕=5 -
第21题:
计算题: 用pH玻璃电极测定pH=5.0的溶液,其电极电位为43.5mV,测定另一未知溶液时,其电极电位为14.5mV,若该电极的响应斜率为58.0mV/pH,试求未知溶液的pH值。
正确答案: 用pH玻璃电极测定pH=5.0的溶液,其电极电位为43.5mV,测定另一未知溶液时,其电极电位为14.5mV,若该电极的响应斜率为58.0mV/pH,试求未知溶液的pH值。解:PH=5.0+(14.5-43.5)/58.0=4.5 -
第22题:
问答题验测得某水溶液[H+]=1×10-3 mol/L, 求溶液的PH值, 说明溶液的酸碱性。正确答案: [H+]=1×10-3 mol/LPH=—lg[H+]=3
P.H<7溶液呈酸性。解析: 暂无解析 -
第23题:
问答题用玻璃电极作指示电极,以0.2mol·L-1的氢氧化钠溶液电位滴定0.0200mol·L-1的苯甲酸溶液,从滴定曲线上求得终点时溶液的pH为8.22,二分之一终点时溶液的pH为4.18,试计算苯甲酸的离解常数。正确答案: 设HA为苯甲酸,其解离常数Ka=c(H3O+)c(A-)/c(HA)
二分之一终点时,c(HA)=c(A-)/Ka=c(H3O+)
PKa=pH=4.18 Ka=6.6×10-5
苯甲酸的离解常数Ka=6.6×10-5。解析: 暂无解析
