判断题Fe2+还原性比Mn2+强。A 对B 错
题目
对
错
相似考题
参考答案和解析
更多“Fe2+还原性比Mn2+强。”相关问题
-
第1题:
由电对MnO4-/Mn2+和电对Fe3+/Fe2+组成原电池,已知φ MnO4-/Mn2+,φ Fe3+/Fe2+,则电池反应的产物为:A. Fe3+和Mn2+
B. MnO4-和Fe3+
C. Mn2+和Fe2+
D. MnO4-和Fe2+答案:A解析:提示:电极电势高的电对作正极,电极电势低的电对作负极。正极发生的电极反应是氧化剂的还原反应,负极发生的是还原剂的氧化反应。即
MnO4-+8H++5e-=Mn2++4H2O
Fe2+-e-=Fe3+ -
第2题:
已知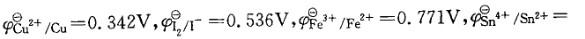 = 0.151V,试判断下列还原剂的还原性由强到弱的是:
= 0.151V,试判断下列还原剂的还原性由强到弱的是:
A. Cu、I- 、Fe2+、Sn2+ B. I-、Fe2+、Sn2+、Cu
C. Sn2+ 、Cu、I-、Fe2+ D. Fe2+、Sn2+、I-、Cu答案:C解析:提示:φΘ值越小,表示电对中还原态的还原能力越强。 -
第3题:
Fe2+还原性比Mn2+强。
正确答案:正确 -
第4题:
关于外加热重铬酸钾容量法测定土壤有机质含量,下列说法中错误的是()
- A、有机质氧化程度较低,只有77%
- B、Cl-可使有机质测定结果偏高
- C、水稻土中还原性物质(如Fe2+、Mn2+)较多时,测定结果偏高
- D、要求重铬酸钾的用量过量25%以上,以便使反应完全
正确答案:A -
第5题:
下列标出水合离子的颜色,其中正确的是()
- A、Ni2+()紫色
- B、Co2+()蓝色
- C、Ti2+()紫红
- D、Mn2+()绿色
- E、Fe2+()淡紫
正确答案:C -
第6题:
在溶液中,与浓HCl能共存的阳离子组是()
- A、Fe2+、Mn2+、Hg22+
- B、Cu2+、Fe3+
- C、Mn2+、Al3+、Hg22+
- D、Zn2+、Fe2+、Hg22+、Mn2+
正确答案:B -
第7题:
植物主要吸收土壤中()态养料,而()态养料,除NH4+、Fe2+、Mn2+外一般对植物无效,甚至有害。
正确答案:氧化;还原 -
第8题:
以电对MnO-4/Mn2+与Fe3+/Fe2+电对组成原电池,已知则反应产物是()。
- A、MnO4和Fe2+
- B、MnO4和Fe3+
- C、Mn2++和Fe2+
- D、Mn2+和Fe3+
正确答案:D -
第9题:
下列说法错误的是()
- A、抗原物质分子量越大,其免疫原性越强
- B、抗原物质分子中的对映体越少,其免疫原性越强
- C、球状蛋白比链状蛋白免疫原性强
- D、动物体内不含有的物质的免疫原性强
正确答案:B -
第10题:
填空题已知Eθ(Fe2+/ Fe)=-0.447V,Eθ(Sn2+/ Sn )=-0.1375V,Eθ(I2/I-)=+0.5355V,Eθ(MnO4/ Mn2+)=+1.507V,则氧化态物质的氧化性由强到弱的顺序为()>()>()>();还原态物质的还原性由强到弱的顺序 为()>()>()>()正确答案: MnO4-,I2,Sn2+,Fe2+,Fe,Sn,I-,Mn2+解析: 暂无解析 -
第11题:
单选题关于外加热重铬酸钾容量法测定土壤有机质含量,下列说法中错误的是()A有机质氧化程度较低,只有77%
BCl-可使有机质测定结果偏高
C水稻土中还原性物质(如Fe2+、Mn2+)较多时,测定结果偏高
D要求重铬酸钾的用量过量25%以上,以便使反应完全
正确答案: A解析: 暂无解析 -
第12题:
判断题Fe2+还原性比Mn2+强。A对
B错
正确答案: 错解析: 暂无解析 -
第13题:
已知E?(Fe3+/Fe2+)=0.77V,E?(MnO4-/Mn2+)=1.51V,当同时提高两电对电极的酸度时,两电对电极电势数值的变化是( )。
A.E?(Fe3+/Fe2+)变小,E?(MnO4-/Mn2+)变大
B.E?(Fe3+/Fe2+)变大,E?(MnO4-/Mn2+)变大
C.E?(Fe3+/Fe2+)不变,E?(MnO4-/Mn2+)变大
D.E?(Fe3+/Fe2+)不变,E?(MnO4-/Mn2+)不变答案:C解析:电极电势与物质的本性、物质的浓度、温度有关,一般温度的影响较小。Fe3++e_=Fe2+,与H+浓度无关;MnO4-+8H++5e_=Mn2++4H2O,H+参与了该反应。因此,E?(Fe3+/Fe2+)不变,E?(MnO4-/Mn2+)变大。 -
第14题:
由电对MnO4-/Mn2+和电对Fe3+/Fe2+组成原电池,已知φ MnO4-/Mn2+,φ Fe3+/Fe2+,
则电池反应的产物为:
A. Fe3+和Mn2+ B. MnO4-和Fe3+ C. Mn2+和Fe2+ D. MnO4-和Fe2+答案:A解析:提示:电极电势高的电对作正极,电极电势低的电对作负极。正极发生的电极反应是氧化剂的还原反应,负极发生的是还原剂的氧化反应。即
MnO4-+8H++5e-=Mn2++4H2O
Fe2+-e-=Fe3+ -
第15题:
Fe2+能加速KMnO4氧化Cl-的反应,这是一种()反应;Mn2+能加速KMnO4氧化C2O42-的反应,这是一种()反应。
正确答案:诱导;自身催化 -
第16题:
试解释下列现象。硅烷的还原性比烷烃强。
正确答案:因为硅烷的稳定性没有烷烃强,所以容易被氧化剂氧化。 -
第17题:
MnO4-与Fe2+反应的平衡常数()。已知jθ(MnO4-/Mn2+)=1.51V,jθ(Fe3+/Fe2+)=0.77V
- A、3.4×1012
- B、320
- C、3.0×1062
- D、4.2×1053
正确答案:C -
第18题:
下列说法不正确的是()。
- A、HCl还原性比HBr强
- B、氮气既有还原性又有氧化性
- C、碘具有氧化性
- D、氧气具有 氧化性。
正确答案:B -
第19题:
已知在1mol/LH2SO4溶液中,Eθ’(MnO4-/Mn2+)=1.45V,Eθ’(Fe3+/Fe2+)=0.68V。在此条件下用KMnO4标准溶液滴定Fe2+,期计量点的电位为()
- A、1.49V
- B、1.32V
- C、0.89V
- D、0.73V
正确答案:B -
第20题:
弱氧化剂遇到比其氧化性强的氧化剂时呈还原性。()
正确答案:正确 -
第21题:
在Cr3+、Mn2+、Fe2+、Fe3+、Co2+、Ni2+中,易溶于过量氨水的是()
正确答案:Co2+、Ni2+ -
第22题:
填空题Fe2+能加速KMnO4氧化Cl-的反应,这是一种()反应;Mn2+能加速KMnO4氧化C2O42-的反应,这是一种()反应。正确答案: 诱导,自身催化解析: 暂无解析 -
第23题:
单选题下列说法错误的是()A抗原物质分子量越大,其免疫原性越强
B抗原物质分子中的对映体越少,其免疫原性越强
C球状蛋白比链状蛋白免疫原性强
D动物体内不含有的物质的免疫原性强
正确答案: B解析: 暂无解析 -
第24题:
单选题已知Eϴ(Fe3+/Fe2+)=0.77V,Eϴ(MnO4-/Mn2+)=1.51V,当同时提高两电对电极的酸度时,两电对电极电势数值的变化是( )。[2019年真题]AEϴ(Fe3+/Fe2+)变小,Eϴ(MnO4-/Mn2+)变大
BEϴ(Fe3+/Fe2+)变大,Eϴ(MnO4-/Mn2+)变大
CEϴ(Fe3+/Fe2+)不变,Eϴ(MnO4-/Mn2+)变大
DEϴ(Fe3+/Fe2+)不变,Eϴ(MnO4-/Mn2+)不变
正确答案: B解析:
电极电势与物质的本性、物质的浓度、温度有关,一般温度的影响较小。Fe3++e_=Fe2+,与H+浓度无关;MnO4-+8H++5e_=Mn2++4H2O,H+参与了该反应。因此,Eϴ(Fe3+/Fe2+)不变,Eϴ(MnO4-/Mn2+)变大。
