问答题某同学在实验室里做了这样一个实验:他先向可能含有SO42-的溶液中加入BaCl2溶液,待生成白色沉淀后,又加入稀硝酸,该沉淀不溶解,于是他判定该溶液中一定含有SO42-。该同学的判断是否正确?为什么?正确检验SO42-的实验方法是什么?
题目
相似考题
更多“某同学在实验室里做了这样一个实验:他先向可能含有SO42-的溶液中加入BaCl2溶液,待生成白色沉淀后,又加入稀硝酸,该”相关问题
-
第1题:
其甲醇溶液中加入硝酸银试液后,则生成白色沉淀
正确答案:E
-
第2题:
将下列各组物质放入水中,生成白色沉淀,加入过量稀硝酸,则沉淀消失并有气泡产生,然后滴入AgN03溶液,又生成白色沉淀.则这组物质是( ) 答案:A解析:
答案:A解析: -
第3题:
某酸性溶液(可能含有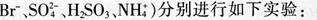
①加热时放出的气体可以使品红溶液褪色
②加碱调至碱性后,加热时放出的气体可以使湿润的红色石蕊试纸变蓝
③加入氯水时,溶液略显黄色,再加人BaCl2溶液时,产生的白色沉淀不溶于稀硝酸
对于下列物质不能确认其在溶液中是否存在的是( )。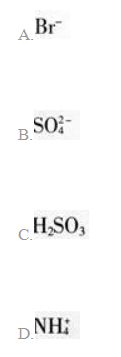 答案:B解析:
答案:B解析:
-
第4题:
现有一种含结晶水的淡绿色晶体,将其配成溶液,若加入BaCl2溶液,则产生不溶于酸的白色沉淀;若加入NaOH溶液,则生成白色胶状沉淀并很快变成红综色。再加入盐酸,此红综色沉淀又溶解,滴入硫氰化钾溶液显深红色。问该晶体是什么物质?
正确答案:A:FeSO4·7H2O -
第5题:
某钠盐A溶于水后加入BaCl2有白色沉淀B生成,在B中加稀盐酸B溶解得溶液C和气体D,D能使品红溶液褪色,在C中加KMnO4溶液,KMnO4紫色消失且有白色沉淀E生成.试判断A,B,C,D,E各为何物?写出各步反应方程式
正确答案:A为Na2SO3;B为BaSO3;C为Ba2+,SO32-,H+,Cl-;D为SO2;E为BaSO4
SO32-+Ba2+==BaSO3↓
BaSO3+2H+==H2O+SO2↑+Ba2+
5SO32-+2MnO4-+6H+==5SO42-+2Mn2++3H2O
Ba2++SO42-==BaSO4↓ -
第6题:
检验烧碱中含纯碱的最佳方法是()
- A、加热有气体生成;
- B、焰色反应为黄色火焰;
- C、加入CaCL2溶液有白色沉淀生成;
- D、加入BaCl2溶液有白色沉淀生成。
正确答案:C -
第7题:
往某无色溶液中加入氯化钡溶液,生成不溶于硝酸的白色沉淀,试简答分析该无色溶液中可能含有的化合物类别是什么?并写出有关反应的化学方程式。
正确答案: 无色溶液可能是硫酸或硫酸盐溶液,也可能是硝酸银溶液.BaCl2+H2SO4==BaSO4↓+2HCl
BaCl2+Na2SO4==BaSO4↓+2NaCl
2ANO3+BaCl2==2AgCl↓+Ba(NO3)2 -
第8题:
填空题有一无色、无气味的澄清液体,其中可能有OH-、SO42-、Cl-、NH4+、Al3+等离子.进行如下试验: (1)用PH试纸检验,pH值约为10: (2)取少量溶液加入硝酸酸化,再加BaCl2溶液,没有出现沉淀; (3)另取少量溶液,加入AgNO3溶液,有白色沉淀,再加硝酸,沉淀不消失; (4)又取少量溶液,稍加热,未发现任何变化. 根据实验现象判断有____离子存在,没有____离子存在.正确答案: OH-、Cl-,SO42-、NH4+、Al3+解析:
溶液pH值为10,呈碱性,则溶液中含有OH-,则不含Al3+;由(2)知,溶液不含SO42-;(3)中白色沉淀含AgOH,可能含有AgCl,加硝酸后沉淀不消失,则白色沉淀中含AgCl,溶液中含有Cl-,由(4)知,溶液不含NH4+,否则会产生刺激性气味的气体. -
第9题:
填空题某正盐和氢氧化钠共热,放出能使湿润的红色石蕊试纸变蓝色的气体;往该盐溶液中,加入Ba(NO3)2溶液,生成不溶于稀硝酸的白色沉淀,则该盐的分子式为____.正确答案: (NH4)2SO4解析:
使湿润红色石蕊试纸变蓝的气体是NH3;不溶于稀硝酸的白色沉淀是BaSO4,所以该正盐是(NH4)2SO4. -
第10题:
单选题以下实验能确定某溶液中一定含有SO42-的是( ).A加入硝酸酸化,再加入BaCl2溶液,产生白色沉淀
B加入硫酸酸化,再加入BaCl2溶液,产生白色沉淀
C加入用盐酸酸化的Ba(NO3)2溶液,产生白色沉淀
D加入Ba(NO3)2溶液,产生白色沉淀,再加入盐酸或硝酸,无反应现象
正确答案: B解析:
A项,硝酸有强氧化性,能把SO32-氧化成SO42-,而产生BaSO4沉淀;B项若用硫酸酸化,则引入了SO42-;C项,用盐酸酸化时,若溶液中不含SO42-,但含Ag+也会产生白色沉淀;D项,只有先加入Ba(NO3)2溶液产生白色沉淀,再加盐酸或稀硝酸沉淀不溶解,才能证明溶液中一定含有SO42-. -
第11题:
填空题有一瓶溶液,可能含有Na+、K+、NH4+、Cl-、SO42-、CO32-中的一种或几种,实验步骤及现象如下: (1)取少许溶液进行焰色反应,火焰呈黄色,透过蓝色钴玻璃,观察不到浅紫色. (2)取少许溶液加入NaOH溶液并加热,不产生刺激性气体. (3)取少许溶液盛于试管中,加入Ba(NO3)2溶液,生成白色沉淀,再加入稀HNO3,白色沉淀全部溶解,继续加入HNO3至溶液呈酸性,并加热,然后加入AgNO3溶液,有白色沉淀生成. 根据以上实验,可以判断,这瓶溶液中肯定含有____;肯定不含有____.正确答案: Na+、Cl-、CO32-,NH4+、K+、SO42-解析:
(1)从焰色反应实验可断定这瓶溶液中肯定含有Na+,不含有K+;
(2)从加入少许NaOH溶液加热不产生刺激性气体,可断定这瓶溶液中不含有NH4+;
(3)加入Ba(OH)2溶液产生白色沉淀,沉淀可能是BaSO4,也可能是BaCO3,再加入稀硝酸,沉淀全部溶解,则可以断定溶液中不含有SO42-(因BaSO4不溶于稀硝酸),含有CO32-,加入稀HNO3后再加入AgNO3,生成不溶于稀HNO3的AgCl,可以断定溶液中含有Cl-. -
第12题:
填空题有一包固体粉末,由下列物质中若干种均匀混合而成:Ba(NO3)2、CaCO3、Na2S、CuSO4、BaCl2,有关实验过程及记录如下:(1)将粉末溶于水,得到蓝色溶液和白色沉淀.过滤后将沉淀洗涤、烘干,称重质量为m克;(2)向滤出的沉淀中加入盐酸,沉淀不溶解;(3)把滤液分成三等份,第一份加稀HNO3和AgNO3溶液,无白色沉淀生成;第二份加入稀H2SO4,无明显现象:第三份加入过量Ba(NO3)2溶液,有白色沉淀生成,把沉淀滤出后洗涤,烘干,称重质量为m克.试判断此白色粉末由____混合而成,它们的物质的量之比为____.正确答案: Ba(NO3)2和CuSO4,1:4解析:
含Cu2+的溶液颜色为蓝色,粉末溶于水后得到蓝色溶液,则粉末中有CuSO4;既然含有CuSO4,则必然不含Na2S,否则两者之间会反应生成黑褐色沉淀CuS,由(2)知,粉末中不含有CaCO3;滤液加稀HNO3和AgNO3溶液,无白色沉淀生成,则溶液中不含有BaCl2;滤液加入稀H2SO4,无明显现象,说明沉淀过滤后,溶液中已经不含有Ba2+;由于粉末溶于水后得白色沉淀,则粉末中含有Ba(NO3)2.滤液加入过量的Ba(NO3)2溶液有白色沉淀生成,说明溶液中仍然含有SO42-,CuSO4是过量的,反应方程式为Ba(NO3)2+CuSO4=BaSO4↓+Cu(NO3)2,刚开始溶于水时产生白色沉淀BaSO4为m克,则各自消耗Ba(NO3)2和CuSO4一份,过滤后剩余的滤液分成三等份,其中一份加入过量Ba(NO3)2溶液,仍然有白色沉淀为m克,则滤液中含CuSO4三份,故Ba(NO3)2和CuSO4的物质的量之比为1:4. -
第13题:
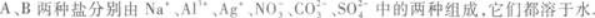
(1)往两种溶液中分别加入盐酸,A溶液不反应,B溶液产生无色无味气体.
(2)往两种溶液中分别加入过量NaOH溶液,A溶液先产生白色沉淀,然后沉淀消失,B溶液与NaOH不反应.
(3)往两种盐溶液中分别加入BaCl2溶液,都产生白色沉淀.再分别加入稀HNO3,A中沉淀不消失,B中沉淀消失.由此可知,A的化学式为____________,B的化学式为____________.答案:解析:Al2(SO4)3 Na2CO3 【解题指要】 解答此类题目,应熟知各种离子的鉴别反应及反应的特殊现象.另外,分析时应全面照顾,不要漏掉条件.
(1)加入盐酸,B溶液产生无色无味气体.在给出的6种离子中只

即B一定是碳酸盐.
(2)加入过量NaOH溶液,A溶液先产生白色沉淀,然后沉淀消失,显然这是Al3+的特征反应.其反应方程式为
即A中一定含有Al3+,是铝盐.
(3)向A、B溶液中分别加入BaCl2溶液,都有白色沉淀生成.再分别加入稀HNO3,A中沉淀

-
第14题:
向某溶液中加入过量盐酸生成白色沉淀,过滤后向滤液中加入过量的氨水(使溶液呈碱性).又有白色沉淀生成:再过滤后向滤液中加入碳酸钠溶液,又生成白色沉淀。则原溶液中含有的离子可能是()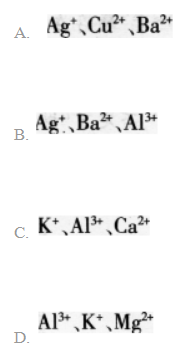 答案:B解析:
答案:B解析:
-
第15题:
有一种白色固体,可能是KI、CaI2、KIO3、BaCl2中的一种或两种的混合物,试根据下述实验判别白色固体的组成。 (1)将白色固体溶于水得到无色溶液; (2)向此溶液加入少量的稀H2SO4后,溶液变黄并有白色沉淀,遇淀粉立即变蓝; (3)向蓝色溶液加入NaOH到碱性后,蓝色消失而白色并未消失。
正确答案:白色固体的组成为:CaI2,KIO3的混合物 -
第16题:
有一种铝盐是白色晶体,溶于水,溶液混浊,滴加少量盐酸混浊消失,在清液中加入硝酸银溶液生成白色沉淀A,此沉淀不溶于稀硝酸;过滤后在滤液中滴加氢氧化钠溶液,生成白色沉淀,继续滴加过量NaOH,白色沉淀消失形成澄清溶液B,由此推断白色晶体是(),沉淀A是()
正确答案:AlCl3;AgCl -
第17题:
在含有氯化锌和氯化汞的混合液中,加入过量稀氨水产生白色沉淀物().生成()离子仍存在于溶液中
正确答案:HgNH2Cl;Zn(NH3)42+ -
第18题:
向某溶液中加入过量盐酸,生成白色沉淀,过滤后向滤液中加入过量氨水使溶液呈碱性,又有白色沉淀生成,在过滤后又向溶液中加入Na2CO3溶液,再次生成白色沉淀。原溶液中含有的离子是()()()
正确答案:Ag+;Al3+;Ba2+ -
第19题:
在未知溶液中加入氯化钡和稀硝酸,析出白色沉淀,未知溶液中可能含有()
- A、碳酸根
- B、磷酸根
- C、硫酸根
- D、氯离子
正确答案:C -
第20题:
单选题往某金属溶解于稀硝酸后所得的溶液中加入NaOH溶液,出现白色沉淀,再加入NaOH溶液,沉淀消失,该金属是( ).AMg
BAg
CAl
DFe
正确答案: D解析:
由于该金属溶于酸形成的酸式盐与氢氧化钠反应生成白色沉淀,且该白色沉淀能继续与氢氧化钠反应,并生成可溶物质,可以断定该金属为铝. -
第21题:
单选题下列离子的检验方法合理的是()。A向某溶液中滴加KSCN溶液呈红色,说明不含Fe2+
B向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
C向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+
D向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+
正确答案: C解析: 暂无解析 -
第22题:
填空题4种正盐A、B、C、D,它们由Na+、Ca2+、Al3+、NH4+、Cl-、SO32-、SO42-和CO32-8种离子组成,鉴别步骤及实验现象如下: (1)取少量A放入试管中,然后加入水,A不溶解. (2)取少量B放入试管中,然后加入水,B全部溶解,其水溶液呈酸性. (3)取少量C放入试管中,然后加入盐酸并加热,反应产生的气体使品红溶液褪色. (4)取少量D放入试管中,然后加入适量稀NaOH溶液,生成白色沉淀;继续加入过量NaOH溶液后沉淀全部溶解.另取少量D放入盛有BaCl2溶液的试管中,生成白色沉淀,加入稀HNO3,沉淀不溶解. 根据以上实验现象,可判断A为____,B为____,C为____,D为____.正确答案: CaCO3,NH4Cl,Na2SO3,Al2(SO4)3解析:
从实验(4)可首先判断出D是Al2(SO4)3.因为其阳离子表现出两性,所以阳离子是Al3+.其阴离子生成钡盐白色沉淀,又不溶于稀HNO3,必为SO42-;
再看实验(1),A化合物不溶于水.因钠盐、铵盐都易溶于水,所以A必是钙盐.因CaCl2溶于水,故只可能是CaSO3,CaSO4或CaCO3.根据实验(3),知道C是亚硫酸盐(因与盐酸反应生成了能漂白品红溶液的SO2;因由(4)排除了CaSO4),从而可以断定A是CaCO3而不是CaSO4或CaSO3.
从实验(2)可知B溶于水,水解后溶液呈酸性,B必为强酸弱碱盐.剩下的离子的组合中只有 NH4Cl符合此条件,故B为NH4Cl.最后,C就是Na2SO3. -
第23题:
单选题在未知溶液中加入氯化钡和稀硝酸,析出白色沉淀,未知溶液中可能含有()A碳酸根
B磷酸根
C硫酸根
D氯离子
正确答案: A解析: 暂无解析
