下列与化学反应能量变化相关的叙述正确的是()。A、生成物总能量一定低于反应物总能量B、放热反应的反应速率总是大于吸热反应的反应速率C、应用盖斯定律,可计算某些难以直接测量的反应焓变D、同温同压下,H2>(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
题目
下列与化学反应能量变化相关的叙述正确的是()。
- A、生成物总能量一定低于反应物总能量
- B、放热反应的反应速率总是大于吸热反应的反应速率
- C、应用盖斯定律,可计算某些难以直接测量的反应焓变
- D、同温同压下,H2>(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
相似考题
更多“下列与化学反应能量变化相关的叙述正确的是()。A、生成物总能量一定低于反应物总能量B、放热反应的反应速率总是大于吸热反应的反应速率C、应用盖斯定律,可计算某些难以直接测量的反应焓变D、同温同压下,H2(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同”相关问题
-
第1题:
下列说法正确的是( )。
A.在化学反应中物质发生化学变化的同时.不一定发生能量变化
B.△H>0表示放热反应,△H<0表示吸热反应
C.放热反应,使体系的温度降低;吸热反应,使体系的温度升高
D.生成物释放的总能量大于反应物吸收的总能量时,该反应的△H<0答案:D解析:化学反应过程中既有物质变化又有能量变化,A项错误;△H>0,表示的是吸热反应,△H <0表示的是放热反应,B项错误;放热反应中,因为有热量的放出,所以使体系的温度升高;吸热反应中,因为要吸收热量,所以使体系的温度降低,C项错误;在化学反应中,生成物释放的总能量大于反应物吸收的总能量时,反应为放热反应,该反应的△H <0。D项正确。 -
第2题:
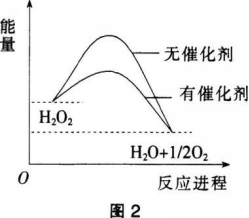
已知H2O2在催化剂作用下分解速率加快,其能量随反应进程的变化如图2所示。下列说法正确的是( )。
 A.催化剂减小了反应的热效应
A.催化剂减小了反应的热效应
B.加入催化剂,可提高H2O2的平衡转化率
C.因为H2O2的分解反应△H<0、△S>0,所以该反应的△G<0
D.因为反应物的总能量高于生成物的总能量,所以该反应属于自发进行的反应答案:C解析:催化剂是通过改变活化能来改变反应速率的,其不改变反应的热效应,A项错误。催化剂只能改变反应速率,不改变化学平衡,反应体系中加入催化剂不改变H20:的平衡转化率,B项错误。由图2中的能量变化可知,H2O2的分解反应,反应物的总能量大于生成物的总能量,即△H<0,又因为△S>0,所以该反应的△G<0,C项正确。由图2可知该反应是放热反应,所以反应物的总能量高于生成物的总能量,但不能据此判断该反应属于自发进行的反应.是否属于自发进行的反应则应该根据吉布斯自由能来判断,D项错误。 -
第3题:
什么是化学能?怎样判断化学反应中反应物和生成物的能量变化?
正确答案: ①这种潜藏在物质内部,只有在化学反应时才释放出来的能量,称之为化学能。
②在放热反应中反应物释放出能量后转变为生成物,可见生成物的总能量一定低于反应物的总能量。
③在吸热反应中,由于反应物吸收外界提供的能量才能转化为生成物,可见生成物的能量总和一定高于反应物的能量总和。 -
第4题:
反应C(s)+ H2O(g)=CO(g)+H2(g)ΔrHm>0,下列叙述正确的是()
- A、此反应为吸热反应,升高温度则正反应速率增加,逆反应速率减少,所以平衡右移
- B、增大压力不利于H2O(g)的转化
- C、升高温度使其KØ减少
- D、加入催化剂可以增加单位时间内的产量
正确答案:B -
第5题:
对于盖斯定律,下列表述不正确的是()
- A、盖斯定律反应了体系从一个状态变化到另一状态的总能量变化;
- B、盖斯定律反应了体系状态变化时其焓变只与体系的始态.终态有关,而与所经历的步骤和途径无关;
- C、盖斯定律反应了体系状态变化时其熵变只与体系的始终态有关,而与所经历的步骤和途径无关;
- D、盖斯定律反应了体系状态变化时其自由能变只与体系的始终态有关,而与所经历的步骤和途径无关.
正确答案:A -
第6题:
研究指出下列反应在一定温度范围内为基元反应: 2NO(g)+Cl2(g)→2NOCl(g) (1)写出该反应的速率方程; (2)该反应的总级数是多少? (3)其他条件不变,如果将容器的体积增加到原来的2倍,反应速率如何变化? (4)如果容器体积不变而将NO的浓度增加到原来的3倍,反应速率又将怎样变化?
正确答案: (1)v=kc(NO)2c(Cl)2
(2)(2+1)=3
(3)反应的初速率为原来的1/8倍
(4)反应的初速率为原来的9倍 -
第7题:
已知:①1molH2分子中化学键断裂时需要吸收436kJ的能量 ②1molCl2分子中化学键断裂时需要吸收243kJ的能量 ③由H原子和Cl原子形成1molHCl分子时释放431kJ的能量。 下列叙述正确的是()。
- A、氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)2HCl(g)
- B、氢气和氯气反应生成2mol氯化氢气体,反应的ΔH=+183kJ·mol-l
- C、氢气和氯气反应生成2mol氯化氢气体,反应的ΔH=-183kJ·mol-l
- D、氢气和氯气反应生成1mol氯化氢气体,反应的AH=+183kJ·mol-l
正确答案:C -
第8题:
某温度下,化学反应2NO(g)+O2(g)=2NO2(g)达平衡,下列说法中正确的()。
- A、反应物已消耗完
- B、不再有产物生成
- C、正逆反应速率相等
- D、反应已停止
正确答案:C -
第9题:
H2+Cl2→2HCl,其反应速率公式为r=K[H2][Cl2]1/2,总反应级数为()。
正确答案:1.5 -
第10题:
单选题在298K时,H2(g)+1/2O2(g)=H2O(L),△H=-285.8kJ/mol。若温度升高,则有下列中何种变化?()A正反应速率增大,逆反应速率减小
B正反应速率增大,逆反应速率增大
C正反应速率减小,逆反应速率增大
D正反应速率减小,逆反应速率减小
正确答案: B解析: 无论是吸热反应还是放热反应,温度升高时由阿仑尼乌斯公式得出,速率常数均增加。因此反应速率也都增加。 -
第11题:
单选题下列与化学反应能量变化相关的叙述正确的是()。A生成物总能量一定低于反应物总能量
B放热反应的反应速率总是大于吸热反应的反应速率
C应用盖斯定律,可计算某些难以直接测量的反应焓变
D同温同压下,H2>(g)+Cl2(g)=2HCl(g)在光照和点燃条件下的△H不同
正确答案: C解析: 从能量变化的角度可将化学反应分为放热反应和吸热反应,放热反应产物的能量降低,吸热反应产物的能量升高;化学反应的速率由反应物的性质决定,也与某些外界条件有关,但与反应是否吸热、放热无关;盖斯定律是能量守恒原理的具体体现,因此只要确定反应物(温度、状态)和生成物(温度、状态),无论反应进行的途径如何,其总能量变化保持不变。 -
第12题:
填空题在标准状态下的反应H2(g)+Cl2(g)→2HCl(g),其ΔrHmθ=-184.61kJ•mol-1,由此可知HCl(g)的标准摩尔生成焓变应为()kJ•mol-1正确答案: -92.30kJ.mol-1解析: 暂无解析 -
第13题:
下列说法正确的是( ? )。A.一定条件下某吸热反应能自发进行,说明该反应是熵增大的反应 ? ?
B.增大反应物浓度可加快反应速率,因此可用浓硫酸与铁反应增大生成H2的速率 ?
C.催化剂可加快反应速率并影响平衡的移动 ??
D.增大反应物固体的量可促使平衡正向移动答案:A解析:根据ΔG=ΔH-T·ΔS,如ΔH>0,则只有ΔS>0,才能使ΔG<0,A正确;
增大反应物浓度可加快反应速率,浓硫酸与铁反应不能生成H2,B错误;
催化剂可加快反应速率,但不会影响平衡的移动,C错误;
增大反应物固体的量不会使平衡移动,D错误。 -
第14题:
在298K时,H2(g)+(1/2)O2(g)=H2O(L),ΔH=-285.8kJ/mol。若温度升高,则有下列中何种变化?A.正反应速率增大,逆反应速率减小
B.正反应速率增大,逆反应速率增大
C.正反应速率减小,逆反应速率增大
D.正反应速率减小,逆反应速率减小答案:B解析:提示:无论是吸热反应还是放热反应,温度升高时由阿仑尼乌斯公式得出,速率常数均增加。因此反应速率也都增加。 -
第15题:
以下关于化学反应速率的论述中,正确的是()
- A、化学反应速率可用某时刻生成物的物质的量来表示
- B、在同一反应中,用反应物或生成物表示的化学反应速率数值是相同的
- C、化学反应速率是指反应进行的时间内,反应物浓度的减少或生成物浓度的增加
- D、可用单位时间内氢离子物质的量浓度的变化来表示NaOH和H2SO4的反应速率
正确答案:D -
第16题:
若下列反应都在298K下进行,则反应的ΔrHm与生成物的ΔfHm相等的反应是:()
- A、1/2H2(g)+1/2I2(g)→HI(g)
- B、H2(g)+Cl2(g)→2HCl(g)
- C、H2(g)+1/2O(g)→H2O(g)
- D、C(金刚石)+O2(g)→CO2(g)
- E、HCl(g)+NH3(g)→NH4Cl(s)
正确答案:C -
第17题:
反应C(s)+H2O(g)=CO(g)+H2(g) ΔrHθm>0,下列叙述正确的是()
- A、此反应为吸热反应,升高温度则正反应速率增加,逆反应速率减少,所以平衡右移
- B、增大压力不利于H2O(g)的转化
- C、升高温度使其Kθ减少
- D、加入催化剂可以提高反应物的转化率
正确答案:B -
第18题:
反应2HCl(g)→Cl2(g)+H2(g)的ΔrHm°=184.9kJ.mol-1,这意味着:()
- A、该反应为吸热反应
- B、HCl(g)的ΔfHm°为负值
- C、该反应体系是均相体系
- D、上述三种说法均正确
正确答案:D -
第19题:
在298K时,H2(g)+1/2O2(g)=H2O(L),△H=-285.8kJ/mol。若温度升高,则有下列中何种变化?()
- A、正反应速率增大,逆反应速率减小
- B、正反应速率增大,逆反应速率增大
- C、正反应速率减小,逆反应速率增大
- D、正反应速率减小,逆反应速率减小
正确答案:B -
第20题:
已知反应H2(g)+O2(g)H2O(l)△H=-285.8KJ/mol则下列结论正确的是()
- A、H(反应物)>H(生成物)
- B、H(反应物)<h(生成物)
- C、H(反应物)=H(生成物)
- D、反应吸热
- E、反应放热
正确答案:A,E -
第21题:
反应H2(g)+Cl2(g)=2HCl(g)在等温等压下完成时放出的热称为()
- A、 HCl(g)的生成热
- B、 H2(g)的燃烧热
- C、 Cl2(g)的燃烧热
- D、 该化学反应的摩尔等压反应热效应
正确答案:D -
第22题:
单选题阿累尼鸟斯定律阐明了()A化学反应速率常数与温度之间的关系
B化学反应速率与反应物浓度的关系
C化学反应的活化能与温度的关系
正确答案: C解析: 暂无解析 -
第23题:
单选题对给定的化学反应,下列说法正确的是()。AΔG越负,反应速率越快
BΔH越负,反应速率越快
CΔS越负,反应速率越快
D活化能Ea越小,反应速率越快
正确答案: C解析: 暂无解析
