中国工业报2007年7月2日报道,国际投行瑞士信贷发布报告称,由于中国对铁矿石的需求增长超过预期,国际矿业巨头明年可能再度提高铁矿石售价。下列有关铁及其化合物的说法中正确的是()。A、赤铁矿的主要成分是Fe3O4B、铁与水蒸气在高温下的反应产物为Fe2O3和H2C、除去FeCl2溶液中的FeCl4杂质可以向溶液中加入铁粉,然后过滤D、Fe3+与KSCN产生红色沉淀
题目
中国工业报2007年7月2日报道,国际投行瑞士信贷发布报告称,由于中国对铁矿石的需求增长超过预期,国际矿业巨头明年可能再度提高铁矿石售价。下列有关铁及其化合物的说法中正确的是()。
- A、赤铁矿的主要成分是Fe3O4
- B、铁与水蒸气在高温下的反应产物为Fe2O3和H2
- C、除去FeCl2溶液中的FeCl4杂质可以向溶液中加入铁粉,然后过滤
- D、Fe3+与KSCN产生红色沉淀
相似考题
更多“中国工业报2007年7月2日报道,国际投行瑞士信贷发布报告称,由于中国对铁矿石的需求增长超过预期,国际矿业巨头明年可能再度提高铁矿石售价。下列有关铁及其化合物的说法中正确的是()。A、赤铁矿的主要成分是Fe3O4B、铁与水蒸气在高温下的反应产物为Fe2O3和H2C、除去FeCl2溶液中的FeCl4杂质可以向溶液中加入铁粉,然后过滤D、Fe3+与KSCN产生红色沉淀”相关问题
-
第1题:
在铁矿石中不含铁的化合物称( )。
A.岩石
B.脉石
C.矿石
D.烧结矿
正确答案:B
-
第2题:
某选厂处理的铁矿石只含有赤铁矿,且赤铁矿的含量为80%,该铁矿石的含铁量为( )%。
正确答案:56.0
-
第3题:
下列各组物质相互反应后,再滴入KSCN溶液,显红色的是( )A.过量铁粉与稀盐酸
B.过量铁粉与CuCl2溶液
C.过量氯水与FeCl2溶液
D.过量铁粉与FeCl3溶液答案:C解析:(1)“反应后滴入KSCN溶液,呈现红色”,说明溶液中应有Fe3+存在.另外, 因Fe有+2价和+3价两种价态,所以反应产物究竟是什么,与氧化剂氧化性的强弱及反应物的相对数量,即哪种物质过量有直接关系.
Fe3+.所以只要有Fe3+生成,加入KSCN溶液后就能显示血红色.这与氯水过量与否关系不大,只是若氯水过量,可将FeCl2全部变成FeCl3.而与KSCN反应显示血红色,不必全部转化成FeCl3.所以,C选项为正确选项. -
第4题:
某化学学习小组欲探究铁及其化合物的氧化性和还原性。
(1)实验试剂及仪器:?
氯化亚铁溶液、氯化铁溶液、氯水、KSCN溶液、铁粉、锌片、铜片、稀硫酸、胶头滴管、试管?
(2)实验记录?
根据上述材料回答下列问题:?
(1)在实验②中,有部分同学在氯化亚铁溶液中滴入KSCN溶液后,就出现了血红色,可能的原因是什么?
(2)在配制氯化铁溶液时,由于实验员失误,可能导致溶液中含有少量的Fe2+,如何检验是否有少量Fe“的存在?
(3)作为教师,在进行实验探究教学时,应注意哪些方面?答案:解析:(1)可能的原因是氯化亚铁溶液中的Fe2+被氧化,Fe3+与KSCN反应显红色,若实验中出现红色,说明有Fe3+,所以可能是这些同学的溶液已经发生了变质。
(2)可向此溶液中加入酸性高锰酸钾,由于高锰酸钾与Fe2+反应,若酸性高锰酸钾溶液褪色,则说明含有Fe3+。
(3)实验探究教学,是在教师指导下,学生应用已学过的知识与技能,通过实验来探索化学概念或规律,从而获得知识的方法。在实验探究过程中主要注意以下问题:①指导学生做好实验方案设计;②指导学生做好探究;③指导学生做好表达交流;④对学生的探究做好总结。 -
第5题:
在铁矿石中不含铁的化合物称()。
- A、岩石
- B、脉石
- C、矿石
- D、烧结矿
正确答案:B -
第6题:
用KSCN溶液鉴定溶液中Fe3+离子的现象是()。
- A、溶液变蓝色
- B、溶液变橙色
- C、溶液变红色
- D、产生白色沉淀
正确答案:C -
第7题:
下列铁矿石中理论含铁量最高的是()。
- A、磁铁矿
- B、赤铁矿
- C、菱铁矿
正确答案:A -
第8题:
混合溶液A为紫红色。向A中加入浓盐酸并微热得兰色溶液B和气体C。A中加入NaOH溶液则得棕黑色沉淀D和绿色溶液E。向A中通入过量SO2则溶液最后变为粉红色溶液F,向F加入过量氨水得白色沉淀G和棕黄色溶液H。G在空气中缓慢转变为棕黑色沉淀。将D与G混合后加入硫酸又得溶液A。给出A~H所代表的主要化合物或离子。
正确答案:A.MnO4-+Co2+
B.[CoCl4]2-
C.Cl2
D.Co(OH)3
E.MnO42-
F.Mn2++Co2+
G.Mn(OH)2
H.[Co(NH3)6]2+ -
第9题:
下列离子的检验方法合理的是()。
- A、向某溶液中滴加KSCN溶液呈红色,说明不含Fe2+
- B、向某溶液中通入Cl2,然后再加入KSCN溶液变红色,说明原溶液中含有Fe2+
- C、向某溶液中加入NaOH溶液,得红褐色沉淀,说明溶液中含有Fe3+
- D、向某溶液中加入NaOH溶液得白色沉淀,又观察到颜色逐渐变为红褐色,说明该溶液中只含有Fe2+,不含有Mg2+
正确答案:C -
第10题:
溶液中若含有Fe3+,加入KSCN溶液后,溶液将变成什么颜色()。
- A、蓝色
- B、红色
- C、白色
- D、绿色
正确答案:B -
第11题:
单选题蛇纹石由MgO、A12O3、SiO2、Fe2O3组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加入NaOH溶液至过量。下列叙述不正确的是()A沉淀X的成分是SiO2
B将蛇纹石试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3
C在溶液Y中加入过量的NaOH溶液,过滤得到的沉淀的主要成分是Fe(OH)3和Mg(OH)2
D溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
正确答案: B解析: 暂无解析 -
第12题:
单选题溶液中若含有Fe3+,加入KSCN溶液后,溶液将变成什么颜色()。A蓝色
B红色
C白色
D绿色
正确答案: B解析: 暂无解析 -
第13题:
在铁矿石中不含铁的化合物称( )。
A.岩石
B.脉石
C.硅石
D.矿石
正确答案:B
-
第14题:
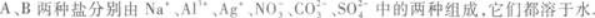
(1)往两种溶液中分别加入盐酸,A溶液不反应,B溶液产生无色无味气体.
(2)往两种溶液中分别加入过量NaOH溶液,A溶液先产生白色沉淀,然后沉淀消失,B溶液与NaOH不反应.
(3)往两种盐溶液中分别加入BaCl2溶液,都产生白色沉淀.再分别加入稀HNO3,A中沉淀不消失,B中沉淀消失.由此可知,A的化学式为____________,B的化学式为____________.答案:解析:Al2(SO4)3 Na2CO3 【解题指要】 解答此类题目,应熟知各种离子的鉴别反应及反应的特殊现象.另外,分析时应全面照顾,不要漏掉条件.
(1)加入盐酸,B溶液产生无色无味气体.在给出的6种离子中只

即B一定是碳酸盐.
(2)加入过量NaOH溶液,A溶液先产生白色沉淀,然后沉淀消失,显然这是Al3+的特征反应.其反应方程式为
即A中一定含有Al3+,是铝盐.
(3)向A、B溶液中分别加入BaCl2溶液,都有白色沉淀生成.再分别加入稀HNO3,A中沉淀

-
第15题:
已知铁与浓硝酸在加热的条件下反应,生成硝酸铁,硝酸铁溶液与铁粉反应,生成硝酸亚铁。某同学受此启发,提出一个类似的观点:浓硫酸与铁粉在加热条件下反应生成硫酸铁,硫酸铁溶液与铁粉反应,生成硫酸亚铁。该同学运用的思维方法是( )。
A.类比
B.分类
C.归纳
D.综合答案:A解析:类比法是根据两个或者两类对象有某些共有或者相似属性推出一个研究对象可能具有另一个研究对象所具有的属性。浓硝酸和浓硫酸都是强氧化性酸,具有相似的化学性质,所以学习了浓硝酸与铁的相关反应,再学习浓硫酸与铁的相关反应时,提出类似的观点,利用的是类比的思维方法,故本题选A。 -
第16题:
蛇纹石由MgO、A12O3、SiO2、Fe2O3组成。现取一份蛇纹石试样进行实验,首先将其溶于过量的盐酸,过滤后,在所得的沉淀X和溶液Y中分别加入NaOH溶液至过量。下列叙述不正确的是()
- A、沉淀X的成分是SiO2
- B、将蛇纹石试样直接溶于过量的NaOH溶液后过滤,可得到红色颜料Fe2O3
- C、在溶液Y中加入过量的NaOH溶液,过滤得到的沉淀的主要成分是Fe(OH)3和Mg(OH)2
- D、溶液Y中的阳离子主要是Mg2+、Al3+、Fe3+、H+
正确答案:B -
第17题:
铁和铁合金是生活中常用的材料,下列说法正确的是()。
- A、不锈钢是铁合金.只含金属元素
- B、一定条件下,铁粉可与水蒸气反应
- C、铁与盐酸反应.铁合金不与盐酸反应
- D、在空气中,铁板比镀锌板更耐腐蚀
正确答案:B -
第18题:
高炉铁矿石中理论含铁量最高的是赤铁矿。
正确答案:错误 -
第19题:
下列各组物质中,滴入KCNS显红色的是()
- A、铁与稀盐酸
- B、过量铁与稀硫酸
- C、氯水与氯化亚铁
- D、铁粉与氯化铜
- E、过量铁粉与硫酸铁溶液
正确答案:C -
第20题:
在某化合物的溶液中加入铁粉,溶液的质量增加,该溶液中可能含有()
- A、Cu2+
- B、Al3+
- C、Ag+
- D、Fe3+
正确答案:D -
第21题:
背景材料: 阅渎下列三段高中化学教学中有关“铁的重要化合物”的材料。 材料一《普通高中课程标准(实验)》的内容标准:根据生产、生活中的应用实例或通过实验探究,了解钠、铝、铁、铜等金属及其重要化合物的主要性质,能列举合金材料的重要应用。 材料二“铁的重要化合物”内容属于高中化学必修阶段的无机元素化合物教学内容,必修化学课程中的无机元素化合物知识安排在《化学1》的“主题3常见无机物及其应用”中。普通高中课程标准使用教科书《化学1》的目录: 第一章从实验学化学 第二章化学物质及其变化 第三章金属及其化合物 第一节金属的化学性质 第二节几种重要的金属化合物 第三节用途广泛的金属材料 第四章非金属及其化合物 材料三以下是某教师设计的教学活动: 【学生活动】阅读教材关于铁的氧化物的介绍,利用分类法归纳FeO、Fe2O3、Fe3O4的性质,并填写表格。 【学生实验1】氢氧化铁、氢氧化亚铁的制备与Fe3+离子检验(整合实验)。 【问题情景1】阅读课文,结合实验现象,思考与讨论: 1.利用KSCN溶液,可以根据什么现象检验溶液中Fe3+的存在?Fe2+离子遇到KSCN会产生相同的现象吗? 2.FeSO4溶液滴加KSCN溶液一段时间后,再次观察溶液的颜色,出现了什么变化?该变化说明了什么?由此你可以得出什么结论? 3.Fe(OH)2沉淀是什么颜色?为什么往FeSO4溶液中滴加NaOH溶液后生成的沉淀会出现颜色变化? 【师生小结】 【问题情景2】 1.从Fe2+被O2氧化为Fe3+,体现了Fe2+的什么性质?除了O2,还有哪些物质可以氧化Fe2+? 2.若要实现从Fe3+转为Fe2+的变化,需要加入什么物质? 【学生实验2】Fe2+与Fe3+的转化,按照教材P)61科学探究进行实验,观察与记录实验现象。 【问题情景3】结合实验探究的现象,思考与讨论: l.Fe3+与铁粉充分反应后的产物是什么?如何证明? 2.回忆前面有关Fe2+的实验,为什么用Fe与稀硫酸制备FeSO4溶液,并保持铁过量? 3.实验中如何判断Fe3+已充分反应?反应不充分对实验结果有何影响? 【师生小结】 【问题情景3】学生课后思考与讨论 通过学习我们知道,Fe2+离子和Fe(OH)2中+2价的铁均易被氧化。根据所学的知识,思考:利用FeSO4溶液和NaOH溶液时,如何通过实验条件的控制,制备较纯净的Fe(OH)2白色沉淀? 请根据上述材料,完成“铁的化合物”这一教学片段的有关任务: 问题: (1)试确定本课的三维教学目标。 (2)说明本节课的教学策略。 (3)请对本课内容进行板书设计。 (4)请对本课内容设计导入。 (5)请写出氢氧化铁、氢氧化亚铁的制备与检验Fe3+离子的实验步骤。
正确答案: (1)知识与技能:
①了解铁的氧化物和铁的氢氧化物的物理性质。
②初步掌握铁的氧化物和铁的氢氧化物的化学性质,通过对灰绿色沉淀成因的分析,认识+2价铁的化合物易被氧化的性质。
③知道溶液中Fe3+的检验方法。
④知道Fe3+与Fe2+之间能够相互转化,能从氧化还原的角度分析转化发生的条件。
过程与方法:
①初步学会从物质分类和氧化还原的角度研究物质性质的方法。
②通过对铁的化合物氧化还原性的预测,初步学会用氧化还原反应理论研究物质的氧化还原性。
③通过对铁的化合物实验演示与探究活动,初步学会通过实验研究物质化学性质的思路和方法。
④通过对“氢氧化亚铁制备”实验条件的思考与交流,初步培养综合分析问题的能力。
情感态度与价值观:
①通过实验现象的观察,培养实事求是的科学品质。
②体验学习过程中新旧知识的衔接和运用,逐步培养主动运用知识、迁移知识解决实际问题的意识。
(2)①运用分类的方法,根据物质所属类别(金属氧化物、碱、盐)预测物质性质。
②整合实验过程,设计问题情景进行引导、启发式教学。
本节课安排了3个实验,氢氧化铁与氢氧化亚铁的制备、Fe3+离子的检验以及Fe3+与Fe2+的转化。相对而言本节课实验的内容较多,而不管是Fe(OH)2的性质或是Fe2+与Fe3+的转化,均涉及到+2价铁元素的还原性这一特点,以及都使用到Fe2+溶液。为此,在授课过程中,可以通过把“Fe(OH)2的制备与性质实验”“Fe3+离子的检验”和“Fe2+与Fe3+的转化”三个实验进行整合,同时设计几个问题情景,以起到优化课堂效率,形成知识系统的作用。同时,通过问题情景的创设,能够引导学生对实验现象进行分析与思考,发挥学生课堂学习的主动性。
(3)板书设计
铁的重要化合物
1.氧化物
2.氢氧化物
3.铁盐和亚铁盐
4.Fe2+与Fe3+的检验
(4)利用问题引入课题,集中学生的注意力,提高学习兴趣。
①学校红墙上红色油漆中的红色物质是什么?②红砖为什么呈现红色?
(5)实验步骤:
①取两支试管分别加入2mLFeCl3溶液,另取两支试管分别加入2mL新制FeSO4液(在大烧杯加入铁钉与稀硫酸反应得到,并保持Fe与H2SO4反应不断进行,放在公共药品台上,学生自行取用)。
②先往两支FeSO4溶液中滴加氢氧化钠溶液和KSCN溶液(动作要迅速),观察与记录现象,再往两支FeCl3溶液中滴加氢氧化钠溶液和KSCN溶液,观察与记录现象。 -
第22题:
单选题铁和铁合金是生活中常用的材料,下列说法正确的是()。A不锈钢是铁合金.只含金属元素
B一定条件下,铁粉可与水蒸气反应
C铁与盐酸反应.铁合金不与盐酸反应
D在空气中,铁板比镀锌板更耐腐蚀
正确答案: D解析: 不锈钢是在普通钢中加入铬、镍等多种元素炼成的,另外里面还含有碳元素,A错误;铁是一种较活泼的金属单质,在高温的条件下可以与水蒸气反应,B正确;铁合金主要成分是铁,能与盐酸反应生成氢气,C错误;镀锌铁板比铁板耐腐蚀,D错误。故选B。 -
第23题:
单选题中国工业报2007年7月2日报道,国际投行瑞士信贷发布报告称,由于中国对铁矿石的需求增长超过预期,国际矿业巨头明年可能再度提高铁矿石售价。下列有关铁及其化合物的说法中正确的是()。A赤铁矿的主要成分是Fe3O4
B铁与水蒸气在高温下的反应产物为Fe2O3和H2
C除去FeCl2溶液中的FeCl4杂质可以向溶液中加入铁粉,然后过滤
DFe3+与KSCN产生红色沉淀
正确答案: D解析: 暂无解析
