在比较同一药物口服试验制剂和参比制剂(上市制剂)的生物等效性试验后,观察到试验制剂比上市制剂有更大的生物利用度。 (1)能否批准该试验制剂上市,并认为它优于注册制剂? (2)能否认为两个制剂有一致的药效? (3)服用试验制剂是否会引起服用上市制剂不会出现的治疗问题?
题目
在比较同一药物口服试验制剂和参比制剂(上市制剂)的生物等效性试验后,观察到试验制剂比上市制剂有更大的生物利用度。 (1)能否批准该试验制剂上市,并认为它优于注册制剂? (2)能否认为两个制剂有一致的药效? (3)服用试验制剂是否会引起服用上市制剂不会出现的治疗问题?
相似考题
更多“在比较同一药物口服试验制剂和参比制剂(上市制剂)的生物等效性试”相关问题
-
第1题:
根据《中国上市药品目录集》规定,治疗等效相关术语包括()。A.参比制剂和标准制剂
B.药学等效药品
C.治疗等效药品
D.治疗等效性评价代码
参考答案:BCD
解析:治疗等效相关术语包括:药学等效药品;治疗等效药品;治疗等效性评价代码(简称TE代码);选项BCD当选。
-
第2题:
下列关于生物利用度与生物等效性试验描述错误的是A、对于个体变异较大的制剂,受试者应选健康成年男性18~24例
B、绝对生物利用度研究应选静脉注射剂为参比制剂
C、相对生物利用度研究应首选考虑国内外已上市的相同剂型的制剂或被仿制的原制剂为参比制剂
D、一个受试试验制剂和一个参比制剂的研究一般采用双交叉试验设计
E、受试制剂必须是中试放大产品,经省或国家药检部门检验合格,体外释放度、稳定性、含量合格及安全性均符合要求
参考答案:A
-
第3题:
制剂生物利用度研究中关于参比制剂的说法错误的是
A.参比制剂安全性和有效性应合格
B.进行相对生物利用度研究时,参比制剂为在研新制剂
C.进行绝对生物利用度研究时应选择上市的静脉注射剂作为参比制剂
D.进行相对生物利用度研究时应选择国内外同类上市主导产品作为参比制剂
E.参比制剂与受试制剂一般应为等剂量
正确答案:B
-
第4题:
A.以静脉注射为参比制剂,两种制剂的药时曲线下面积比
B.血管外给药,药物进入体循环相对数量和相对速率
C.指同一药物相同剂量制成同一剂型,但非活性成分不一定相同,含量、纯度、崩解、溶出速率符合同一规定标准的制剂
D.指一种药物的不同制剂在相同的实验条件下,给予相同剂量,其吸收速度和程度没有明显差别
E.以市售质量较好的制剂为参比制剂,两种制剂的药时曲线下面积比生物等效性答案:D解析: -
第5题:
当参比制剂是静脉注射剂时,试验制剂与参比制剂AUC的比值代表查看材料A.相对生物利用度
B.绝对生物利用度
C.生物等效性
D.肠-肝循环
E.生物利用度答案:B解析:本组题考查生物利用度。生物利用度是指剂型中的药物进入体循环的速度和程度,根据参比制剂的不同,分为绝对生物利用度和相对生物利用度。绝对生物利用度是以静脉制剂为参比制剂获得的药物活性成分吸收进入血液循环的相对量,通常用于原料药和新剂型的研究;相对生物利用度是以其他非静脉途径给药的制剂为参比制剂获得的药物活性成分吸收进入血液循环的相对量,用于剂型之间或同种剂型不同制剂之间的比较。 -
第6题:
A.相对生物利用度
B.绝对生物利用度
C.生物等效性
D.肠肝循环
E.生物利用度当参比制剂是静脉注射剂时,试验制剂与参比制剂AUC的比值代表答案:B解析:本组题考查生物利用度和生物等效性。生物利用度是指剂型中的药物进入体循环的速度和程度,根据参比制剂的不同,分为绝对生物利用度和相对生物利用度。生物等效性是指一种药物的不同制剂在相同条件下,给以相同剂量,反映其吸收程度和速度的主要药物动力学参数,无统计学差异。故本组题答案应选C。 -
第7题:
关于生物利用度叙述正确的是()
- A、系指药物被吸收进入血液循环的程度
- B、相对生物利用度是试验制剂与静脉注射制剂相比较
- C、绝对生物利用度是试验制剂与参比制剂相比较
- D、生物利用度常用AUC表示
- E、研究所用的参比制剂必须安全有效
正确答案:D,E -
第8题:
单选题关于口服制剂人体生物等效性试验的一般要求,叙述错误的是()A通常选择健康男性
B通常采用双周期两制剂交叉试验设计
C给药剂量大于临床常规剂量
D受试者应禁食过夜
E应选择同类上市主导产品作为参比制剂
正确答案: B解析: 暂无解析 -
第9题:
单选题试验制剂与参比制剂的血药浓度-时间曲线下面积的比率是A生物利用程度
B生物利用速度
C相对生物利用度
D绝对生物利用度
E生物等效性评价
正确答案: B解析: -
第10题:
单选题下列关于生物利用度和生物等效性试验的说法,正确的是( )。A绝对生物利用度试验可以不用参比制剂作对照
B生物利用度试验和生物等效性试验都必须用参比制剂作对照
C生物利用度试验和生物等效性试验都可以不用参比试剂作对照
D生物利用度试验可以不用参比制剂作对照,生物等效性试验则必须用参比制剂作对照
E生物利用度试验必须用参比制剂作对照,生物等效性试验则可以不用参比制剂作对照
正确答案: A解析: 暂无解析 -
第11题:
单选题A供试制剂的相对生物利用度为105.9%,超过100%,可判定供试制剂与参比制剂生物不等效
B根据AUC0-∞和Cmax的试验结果,可判定供试制剂与参比制剂生物等效
C根据tmax和t1/2的试验结果,可判定供试制剂与参比制剂生物等效
D供试制剂与参比制剂的Cmax均值比为97.0%,判定供试制剂与参比制剂生物不等效
E供试制剂与参比制剂的tmax均值比为91.7%,判定供试制剂与参比制剂生物不等效
正确答案: C解析: -
第12题:
单选题当参比制剂是静脉注射剂时,试验制剂与参比制剂AUC的比值代表( )。A相对生物利用度
B绝对生物利用度
C生物等效性
D肠肝循环
E生物利用度
正确答案: D解析: -
第13题:
符合生物利用度和生物等效性实验要求的选项为
A.仿制缓控释制剂生物等效性试验的参比制剂必须选用国外市售相同产品
B.创新缓控释制剂生物等效性试验的参比制剂可以选用符合国家标准的自制普通制剂
C.多次给药实验判断达稳态时,应当测定服药后的达峰浓度
D.多次给药实验判断达稳态时,应当测定服药前的峰谷浓度
E.缓控释制剂生物等效性试验的受试制剂应当选用实验室自制样品,并经药品检验所复核批准
正确答案:D
-
第14题:
制剂生物利用度研究时,关于参比制剂的说法错误的是
A、参比制剂应具有安全性和有效性
B、进行相对生物利用度研究时,参比制剂为在研新制剂
C、进行绝对生物利用度研究时应选择上市的静脉注射剂作为参比制剂
D、进行相对生物利用度研究时应选择国内外同类上市主导产品作为参比制剂
E、参比制剂与受试制剂的剂量应相同
参考答案:B
-
第15题:
生物等效性是
A.药物随胆汁进入小肠后被小肠重吸收的现象
B.药物在进入体循环前被肝代谢的现象
C.一种药物的不同制剂在相同的试验条件下,给予同剂量,其吸收速度和程度无明显差异
D.以静脉注射剂为参比制剂所得的生物利用度
E.以非静脉制剂为参比制剂所得的生物利用度
正确答案:C
略 -
第16题:
制剂生物利用度研究时,关于参比制剂的说法错误的是A.参比制剂应具有安全性和有效性
B.进行相对生物利用度研究时,参比制剂为在研新制剂
C.进行绝对生物利用度研究时应选择上市的静脉注射剂作为参比制剂
D.进行相对生物利用度研究时应选择国内外同类上市主导产品作为参比制剂
E.参比制剂与受试制剂的剂量应相同答案:B解析:进行相对生物利用度研究时,应选择国内外同类上市主导产品为参比制剂,故B项不正确。 -
第17题:
某临床试验机构进行罗红霉素片仿制药的生物等效性评价试验,单剂量(250mg)给药。经24名健康志愿者试验,测得主要药动学参数如下表所示。
经统计学处理,供试制剂的相对生物利用度为105.9%;供试制剂与参比制剂的C 和AUC
和AUC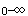 几何均值比的90%置信区间分别在82%~124%和93%~115%范围内。根据上述信息,关于罗红霉素片仿制药生物等效性评价的说法,正确的是
几何均值比的90%置信区间分别在82%~124%和93%~115%范围内。根据上述信息,关于罗红霉素片仿制药生物等效性评价的说法,正确的是
A.供试制剂的相对生物利用度为105.9%,超过100%,可判定供试制剂与参比制剂生物不等效
B.根据AUC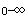 和C
和C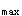 的试验结果,可判定供试制剂与参比制剂生物等效
的试验结果,可判定供试制剂与参比制剂生物等效
C.根据t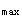 和t
和t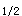 的试验结果,可判定供试制剂与参比制剂生物等效
的试验结果,可判定供试制剂与参比制剂生物等效
D.供试制剂与参比制剂的C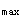 均值比为97.0%,可判定供试制剂与参比制剂生物不等效
均值比为97.0%,可判定供试制剂与参比制剂生物不等效
E.供试制剂与参比制剂的t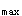 均值比为91.7%,可判定供试制剂与参比制剂生物不等效答案:B解析:AUC几何均值比在80%~125%,C
均值比为91.7%,可判定供试制剂与参比制剂生物不等效答案:B解析:AUC几何均值比在80%~125%,C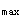 几何均值比在75%~133%之间时,可判定供试制剂与参比制剂生物等效。
几何均值比在75%~133%之间时,可判定供试制剂与参比制剂生物等效。 -
第18题:
关于口服制剂人体生物等效性试验的一般要求,叙述错误的是()
- A、通常选择健康男性
- B、通常采用双周期两制剂交叉试验设计
- C、给药剂量大于临床常规剂量
- D、受试者应禁食过夜
- E、应选择同类上市主导产品作为参比制剂
正确答案:C -
第19题:
下列有关生物利用度含义的叙述,不正确的是()
- A、是指剂型中的药物被吸收进入血液的速度与程度
- B、是指制剂在胃肠道崩解或溶散的程度
- C、生物利用的程度是指与标准参比制剂比较,试验制剂中被吸收药物总量的相对比值
- D、生物利用的速度是指与标准参比制剂比较,试验制剂中药物被吸收速度的相对比值
- E、生物利用速度常用吸收常数ka或吸收半衰期来衡量
正确答案:B -
第20题:
多选题关于生物利用度叙述正确的是()A系指药物被吸收进入血液循环的程度
B相对生物利用度是试验制剂与静脉注射制剂相比较
C绝对生物利用度是试验制剂与参比制剂相比较
D生物利用程度常用AUC表示
E研究所用的参比制剂必须安全有效
正确答案: A,E解析: 暂无解析 -
第21题:
问答题在比较同一药物口服试验制剂和参比制剂(上市制剂)的生物等效性试验后,观察到试验制剂比上市制剂有更大的生物利用度。 (1)能否批准该试验制剂上市,并认为它优于注册制剂? (2)能否认为两个制剂有一致的药效? (3)服用试验制剂是否会引起服用上市制剂不会出现的治疗问题?正确答案: (1)从题中已知试验制剂的生物利用度好于上市制剂,但茌决定能否批准上市前应首先考虑两制剂是否生物等效,若统计结果显示两者具有生物等效性,按照SFDA的相关规定则可以批准试验制剂生产上市。若结果为两制剂生物不等效,则不能认为试验制剂优于上市制剂而批准其上市。
(2)若结果判断为两制剂生物不等效,则两制剂不具有一致的药效。
(3)因为生物利用度的指标包括AUC、tmax和Cmax等,当AUC和Cmax都有显著提高时,服用该试验制剂,对于某些治疗窗狭窄的药物有可能会出现因生物利用度提高而导致的毒副反应。解析: 暂无解析 -
第22题:
单选题下列关于生物利用度与生物等效性试验描述错误的是()A对于个体变异较大的制剂,受试者应选健康成年男性18~24例
B绝对生物利用度研究应选静脉注射剂为参比制剂
C相对生物利用度研究应首选考虑国内外已上市的相同剂型的制剂或被仿制的原制剂为参比制剂
D一个受试试验制剂和一个参比制剂的研究一般采用双交叉试验设计
E受试制剂必须是中试放大产品,经省或国家药检部门检验合格,体外释放度、稳定性、含量合格及安全性均符合要求
正确答案: B解析: 本题主要考查生物利用度试验与生物等效性试验的基本要求。受试者的选择:对于一般制剂,选择健康成年男性18~24例,个体内变异较大的制剂,应适当增加受试者的人数。参比制剂:绝对生物利用度研究应选静脉注射剂为参比制剂;相对生物利用度研究应首选考虑国内外已上市的相同剂型的制剂或被仿制的原制剂为参比制剂。当无相应的参比制剂时,可考虑用其他类型的制剂为参比制剂。受试制剂:必须是中试放大产品,经省或国家药检部门检验合格,体外释放度、稳定性、含量合格及安全性均符合要求。试验设计:一个受试试验制剂和一个参比制剂的研究一般采用双交叉试验设计。两个周期至少间隔7~10个半衰期作为清洗期。 -
第23题:
单选题下列有关生物利用度含义的叙述,不正确的是()A是指剂型中的药物被吸收进入血液的速度与程度
B是指制剂在胃肠道崩解或溶散的程度
C生物利用的程度是指与标准参比制剂比较,试验制剂中被吸收药物总量的相对比值
D生物利用的速度是指与标准参比制剂比较,试验制剂中药物被吸收速度的相对比值
E生物利用速度常用吸收常数ka或吸收半衰期来衡量
正确答案: A解析: 暂无解析
