IA族元素,最外层为1个电子,容易失去,性质活泼。
题目
IA族元素,最外层为1个电子,容易失去,性质活泼。
相似考题
参考答案和解析
正确答案:正确
更多“IA族元素,最外层为1个电子,容易失去,性质活泼。”相关问题
-
第1题:
某元素最高氧化数为+6,最外层电子数为1,原子半径是同族元素中最小的。下列叙述中不正确的是( )。A.外层电子排布为3d54s1
B.该元素为第四周期、ⅥB族元素铬
C.+3价离子的外层电子排布式为3d24s1
D.该元素的最高价氧化物的水合物为强酸答案:C解析:根据题意,最高氧化数为+6的元素有VIA族和VIB族元素;而已知最外层只有一个电子,故只能是VIB族元素;在由已知中最后一个条件“原子半径是同族元素中最小的”,可确定该元素是VIB组中的Cr,Cr的电子排布式为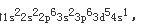
,可得出以下结论:
外层电子排布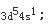
因为周期数等于电子层数,等于最高主量子数,即第四周期。他的最后一个电子填充在d亚层上,所以它是副族元素,其族数等于[(n-1)d+ns]电子层上的电子数,对Cr来讲为5+1=6,即ⅥB族元素;
因为原子失去电子时,首先失去最外层上的电子,继而再失去次外层上的d电子。所以+3价离子的外层电子排布为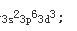
Cr的最高价氧化物CrO3,其水合物为H2CrO4或H2Cr2O7均为强酸。 -
第2题:
某元素最高氧化数为+6,最外层电子数为1,原子半径是同族元素中最小的。 下列叙述中哪一个不正确?A.外层电子排布为3d54s1
B.该元素为第四周期、ⅥB族元素铬
C. +3价离子的外层电子排布式为3d2s1
D.该元素的最高价氧化物的水合物为强酸答案:C解析:解:本题涉及核外电子排布与周期表的问题,根据题意,最高氧化数为+6的元素有ⅥA族和ⅥB族元素;而最外层只有一个电子的条件就排除了ⅥA族元素;最后一个条件是原子半径为同族中最小,可确定该元素是ⅥB族中的铬。Cr的电子排布式为1s22s22p63s23p63d54s1, 所以得出以下结论。
A正确。外层电子排布为3d54s1。
B正确。因为周期数等于电子层数,等于最高主量子数,即第四周期。它的量后一个电子填充在d亚层上,所以它是副族元素,而副族元素的族数等于[(n-1)d+ns]层上的电子数,对 铬来讲为5+1 = 6,即ⅥB族元素。
C错误。因为原子失去电子时,首先失去最外层上的电子,继而再失去次外层上的d电子。所以+3价离子的外层电子排布为3s23p63d3。
D正确。Cr的最高氧化物CrO3,其水合物为H2CrO4或H2Cr2O7均为强酸。
所以答案应为C。 -
第3题:
周期表中,主组元素所在族序数等于最外层电子数。
正确答案:正确 -
第4题:
下列哪一族元素原子的最外层s电子都未占满? ()
- A、ⅠB族
- B、ⅢB族
- C、ⅥB族
- D、ⅤB族
正确答案:A -
第5题:
元素的性质主要决定于()的排布,特别是核外最外层电子的排布。
正确答案:核外电子 -
第6题:
元素的化学性质主要由()决定。
- A、质子数
- B、中子数
- C、核外电子数
- D、最外层电子数
正确答案:D -
第7题:
稀有气体元素最外层为8个电子,化学性质都非常稳定。
正确答案:错误 -
第8题:
原子核最外层电子数为8的元素,其特征()。
- A、为金属元素
- B、化学性质很稳定
- C、为非金属元素
- D、两性元素
正确答案:B -
第9题:
当卤素的原子序数增加时,卤素将:()
- A、更不易失去最外层的电子
- B、变得较不密实
- C、颜色变浅
- D、更不易获得电子
- E、更活泼
正确答案:D -
第10题:
惰性气体不活泼,是因为原子的最外层电子数目是8,化学性质稳定。
正确答案:正确 -
第11题:
某元素其原子最外层有2个电子,次外层有13个电子,问此元素在周期表中应属哪族?最高正价是多少?是金属还是非金属?
正确答案:应该属于ⅦB簇,最高正价+7,金属。 -
第12题:
单选题原子核最外层电子数为8的元素,其特征()。A为金属元素;
B化学性质很稳定;
C为非金属元素;
D两性元素
正确答案: C解析: 暂无解析 -
第13题:
根据右表提供的信息,下列判断正确的是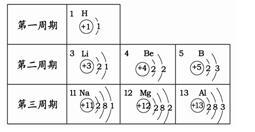 A.元素所在的周期数等于其原子的最外层电子数
A.元素所在的周期数等于其原子的最外层电子数
B.钠离子核外有三个电子层
C.第二、三周期元素的原子从左至右最外层电子数逐渐增多
D.在化学变化中镁元素容易失去最外层2个电子形成镁离子,其离子符号是Mg+2答案:C解析: -
第14题:
下列哪一族元素原子的最外层s轨道上电子都已占满:()。
- A、VIB族
- B、VIII族
- C、IIB族
- D、IB族
正确答案:C -
第15题:
下列关于铝族元素通性的叙述,不正确的是()
- A、都可以失去三个最外层电子生成M3+的离子化合物
- B、都可以失去最外层的P电子生成M+较稳定的化合物
- C、它们的低氧化态化合物都不稳定
正确答案:A,B,C -
第16题:
元素周期表与原子结构关系()。
- A、原子序数=核电荷数
- B、周期序数=电子层数
- C、主族序数=最外层电子数
- D、族元素最外层电子数为8
正确答案:A,B,C -
第17题:
氮族元素的最外层电子数为5,随着核电荷数的递增,得电子的能力逐渐减弱,非金属性逐渐增强。
正确答案:错误 -
第18题:
某元素的非金属性强,一般是指()。
- A、该元素的原子易火去电子的趋势强
- B、该元素的原子易得到电子的趋势强
- C、该元素的原子最外层电子数少于4个
- D、该元素的原子很活泼
正确答案:B -
第19题:
主族元素的性质主要由其原子的最外层电子数和电子层数决定,若元素的最外层电子数为m,电子层数为n,一般具有这样的规律:m>n的元素为非金属元素;m≤n的元素为金属元素。下列有关结论正确的是()
- A、主族元素的性质随着原子量的递增而呈周期性变化
- B、元素的金属性与非金属性递变规律最显著的是第三周期元素和第ⅣA族元素
- C、ⅠA族和ⅦA族元素的单质一般都没有同素异形体
- D、原子最外层电子数等于电子层数的元素均为金属元素
正确答案:B,C -
第20题:
原子核最外层电子数为8的元素,其特征是()。
- A、为金属元素;
- B、化学性质很不活泼;
- C、为非金属元素;
- D、两性元素
正确答案:B -
第21题:
期表中,主组元素所在族序数等于最外层电子数
正确答案:正确 -
第22题:
某些元素原子最外层有两个电子,次外层有13个电子,这些元素在周期表中应属于()族,最高氧化数是(),是()(金/非金)属。
正确答案:ⅦB;+7;金 -
第23题:
判断题期表中,主组元素所在族序数等于最外层电子数A对
B错
正确答案: 对解析: 暂无解析
