98K时,反应A(g)+B(g)2C(g)+D(g)的,若A、B、C、D的起始压分别为100kPa、200kPa、33.5kPa、67kPa,则298K时反应()。A、正向自发B、逆向自发C、处于平衡态D、不能确定
题目
98K时,反应A(g)+B(g)2C(g)+D(g)的,若A、B、C、D的起始压分别为100kPa、200kPa、33.5kPa、67kPa,则298K时反应()。
- A、正向自发
- B、逆向自发
- C、处于平衡态
- D、不能确定
相似考题
更多“98K时,反应A(g)+B(g)2C(g)+D(g)的,若A、B、C、D的起始压分别为100kPa、200kPa、33.5kPa、67kPa,则298K时反应()。A、正向自发B、逆向自发C、处于平衡态D、不能确定”相关问题
-
第1题:
判断常温下,以下气相反应能否自发进行()(1)Na(g)+Rb(g)-Na(g)+Rb(g)(2)F(g)+C1(g)-Cl(g)+F(g)A反应1能自发进行,反应2能自发进行
B反应1不能自安进行,石应2不自三进行
C反应1能目发进行,反应2不能自发进行
D反应1不能自发进行,反应2能自发进行
参考答案:D
-
第2题:
 A.正向自发
A.正向自发
B.逆向自发
C.处于平衡态
D.不能确定答案:A解析: -
第3题:
若298K时反应N2O4(g)=2NO2(g)的Kq=0.1132,则当p(N2O4)=p(NO2)=100kPa时,反应将()
- A、向生成N2O4的方向进行
- B、向生成NO2的方向进行
- C、正好达化学平衡状态
- D、难于判断其进行方向
正确答案:A -
第4题:
正反应能自发进行和反应达平衡的条件分别为()
- A、Qp>Kp,△G<0
- B、Qp>Kp,△G>0
- C、Qp〈Kp,△G〈0
- D、Qp〈Kp,△G>0
- E、Qp=Kp,△G=0
正确答案:C,E -
第5题:
某电池的电动势E是正值,则该电池反应()
- A、逆向自发进行
- B、正向自发进行
- C、处于平衡状态
- D、无法判断反应方向
正确答案:B -
第6题:
反应CH2Cl2(l)+O2(g)CO2(g)+2HCl(g)在常温常压下能否自发进行?怎样判断?已知298K时△G(kJ·mol-1分别为CH2Cl2(l):-67;CO2(g):-394;HCl(g):-95
正确答案:常温常压下可认为K=298,P=101.325KPa即标准状况,反应是否自发,由△G判断:
△G=△G(CO2,g)+2△G(HCl,g)-△G(CH2Cl2,l)
=-517kJ·mol
∵△G<0∴反应可自发进行 -
第7题:
根据ΔGf(NO,g)=86.5KJ/mol,ΔGf(NO2,g)=51.3KJ/mol判断反应(1)N2(g)+O2(g)=2NO(g),(2)2NO(g)+O2(g)=2NO2(g)的自发性,结论正确的是()
- A、(2)自发(1)不自发
- B、(1)和(2)都不自发
- C、(1)自发(2)不自发
- D、(1)和(2)都自发
正确答案:A -
第8题:
在298.15K和标准态时,下列反应均为非自发反应,其中在高温下仍为非自发反应的是()(不必计算)
- A、Ag2O(s) = 2Ag(s) + 1/2O2(g)
- B、N2O4(g) = 2NO2(g)
- C、Fe2O3(s) +3/2C(s) = 2Fe(s) +1/2CO2(g)
- D、6C(s) + 6H2O(g) = C6H12O6(s)
正确答案:D -
第9题:
在298K时N2O4(g)=2NO2(g)的Kø=0.142,当p(N2O4)=101.325kPa,p(NO2)=10.133kPa时,判断反应的方向为()
- A、Qa〈Kø,自发
- B、Qa〉Kø,非自发
- C、Qa=Kø,平衡
- D、Qa〈Kø,非自发
正确答案:A -
第10题:
单选题在等温等压下,某一反应的ΔrHmθ0,则此反应()。A低温下才能自发进行
B正向自发进行
C逆向自发进行
D处于平衡态
正确答案: B解析: 暂无解析 -
第11题:
单选题若298K时反应N2O4(g)=2NO2(g)的KΘ=0.1132,则当p(N2O4)=p(2NO2)=100kPa时,反应将()A向生成N2O4的方向进行
B向生成NO的2方向进行
C正好达化学平衡状态
D难于判断其进行方向
正确答案: A解析: 暂无解析 -
第12题:
单选题若298K时反应N2O4(g)=2NO2(g)的Kq=0.1132,则当p(N2O4)=p(NO2)=100kPa时,反应将()A向生成N2O4的方向进行
B向生成NO2的方向进行
C正好达化学平衡状态
D难于判断其进行方向
正确答案: D解析: 暂无解析 -
第13题:
已知25℃时BaCrO4与BaSO4的KSP分别为1.17×10-10和1.07×10-10,此时关于下述反应方向的说法正确的是( )。A、一定正向自发进行
B、一定逆向自发进行
C、若 、、、浓度足够,反应正向自发
、、、浓度足够,反应正向自发
D、若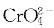 、、、浓度足够,反应正向自发答案:C解析:
、、、浓度足够,反应正向自发答案:C解析: 其中反应②的KSP为1/1.07×10-10,反应③的KSP为1.17×10-10×1/1.07×10-10
其中反应②的KSP为1/1.07×10-10,反应③的KSP为1.17×10-10×1/1.07×10-10
反应③的△G=△rGm=RTlnKSP=-RTln1.09<0,所以反应可以自发进行,但是,能否自发进行还与实际条件有关 -
第14题:
298K时,反应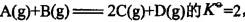 ,若A、B、C、D 的起始压分别为 100kPa、200kPa、33.5kPa、67kPa,则 298K时反应( )。
,若A、B、C、D 的起始压分别为 100kPa、200kPa、33.5kPa、67kPa,则 298K时反应( )。
A.正向自发 B.逆向自发 C.处于平衡态 D.不能确定答案:A解析: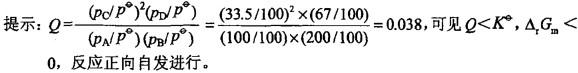
-
第15题:
已知298K下,下列反应的相关条件为: 2NH3(g)→N2(g)+3H2(g) 起始压力/kPa1011011.01 ΔfGm(NH3(g))=-16.64kJ.mol-1, 由此可判断,该反应:()
- A、不能自发进行
- B、处于平衡状态
- C、能自发进行
- D、无法判断
正确答案:C -
第16题:
已知298K时,Ag2O(s)的△fGθ=-10.82kJ·mol-1,则Ag2O(s)分解为Ag(s)和O2(g)的反应可能是()。
- A、在标准状态时是非自发反应
- B、在标准态时是自发反应
- C、在室温标准态时是自发反应
- D、在室温标准态时是非自发反应
正确答案:D -
第17题:
已知298K时,NH3(g)的ΔfHmΘ= –46.19 kJ·mol–1,反应N2(g)+3H2(g) ===2NH3(g)的ΔrSmΘ=–198 J·mol–1·K–1,欲使此反应在标准态下能自发进行,所需温度为()
- A、<193 K
- B、<466 K
- C、>193 K
- D、466 K
正确答案:B -
第18题:
根据数据ΔfGθm(NO,g) =86.5KJ.mol-1,ΔfGθm(NO2,g)=51.3KJ.mol-1,反应 (1)N2(g)+O2(g)= 2NO(g);(2)2NO(g)+O2(g)=2NO2(g),在标准状态下进行的情况说明正确的是()
- A、(1)能自发(2)不能
- B、(1)和(2)都能自发
- C、(2)能自发(1)不能
- D、(1)和(2)都不能自发
正确答案:C -
第19题:
某化学反应A(g)+2B(s)→2C(g)的ΔrHm°<0,则下列判断正确的是:()
- A、仅在常温下,反应可以自发进行
- B、仅在高温下,反应可以自发进行
- C、任何温度下,反应均可以自发进行
- D、任何温度下,反应均难以自发进行
正确答案:B -
第20题:
在一定温度下,可逆反应C(s)+CO2(g)==2CO(g)的KΘ=2.0;当CO2(g)与CO(g)的分压皆为100kPa时,则该反应在同样温度时自发进行的方向为()。
正确答案:正向自发 -
第21题:
若已知H2O(g)和CO(g)在298K时的标准生成焓ΔHf.2980分别为:-242kJ.mol-1及-111kJ.mol-1,则反应H2O(g)+C(s)→H2(g)+CO(g)的反应热为()kJ。
正确答案:131 -
第22题:
单选题已知反应N2(g)+3H2(g)→2NH3(g)的ΔrHm<0,ΔrSm<0,则该反应为( )。[2014年真题]A低温易自发,高温不易自发
B高温易自发,低温不易自发
C任何温度都易自发
D任何温度都不易自发
正确答案: A解析:
判断化学反应自发性的条件参数为吉布斯函数ΔG=ΔH-TΔS,当ΔG<0,反应正向自发;当ΔG=0,反应处于平衡状态;当ΔG>0反应逆向自发。考虑ΔH和ΔS两个因素的影响,分以下4种情况:
①∆H<0,∆S>0,则ΔG<0,反应在任何温度下均能正向自发;
②∆H>0,∆S<0,则ΔG>0,反应在任何温度下均能正向非自发;
③∆H>0,∆S>0,升高至某温度时ΔG由正值变为负值,反应在低温时正向非自发,在高温时正向自发;
④∆H<0,∆S<0,降低至某温度时ΔG由正值变为负值,反应在高温时正向非自发,在低温时正向自发。
本题中,∆H<0,∆S<0,反应低温易自发,高温不易自发。 -
第23题:
填空题反应2N2(g)+O2(g)→2N2O(g),在298K时,ΔrHmθ为164.0kJ.mol-1,则反应ΔU=()。正确答案: 166.5kJ.mol-1解析: 暂无解析
