金属()不能把活动性较弱的金属从其盐溶液中置换出来。A、钠B、锌C、铁D、铜
题目
金属()不能把活动性较弱的金属从其盐溶液中置换出来。
- A、钠
- B、锌
- C、铁
- D、铜
相似考题
参考答案和解析
正确答案:A
更多“金属()不能把活动性较弱的金属从其盐溶液中置换出来。”相关问题
-
第1题:
X、Y、Z 3种金属,已知x可以从Y的盐溶液中置换出Y,X和Z作原电池电极时Z为正极,Y离子的氧化性强于Z离子,则这三种金属的活动性由强到弱的顺序是( )A.X>Y>Z
B.X>Z>Y
C.Z>X>Y
D.Z>Y>X答案:B解析:(1)根据“X可以从Y的盐溶液中置换出Y”,可知金属活动性是X>Y. (2)根据“X和Z作原电池电极时,Z为正极”和活泼金属作负极的判断依据,可知金属活动性是X>Z.
(3)“Y离子的氧化性强于Z离子.”根据金属活动性越强,其阳离子的氧化性越弱;金属活动性越弱,其阳离子的氧化性越强,可知金属活动性是Z>Y.
综上分析可得:X>Z>Y. -
第2题:
某化学教师在一次初三化学考试中设计了下面试题。
【试题】小明同学在学习金属活动性顺序时,对某本书上的‘:活动性较强的金属一般可以将位于其后面的金属从它们的盐溶液中置换出来”这句话产生了疑问.为什么用“一般”这个词呢难道还有例外吗
于是他查阅资料得知:金属钠很活泼。可以与水反应生成氢氧化钠和氢气。同时。他还做了如下实验:往碳酸铜溶液中投入一小块钠,出现蓝色沉淀,没有红色物质析出。
①请写出金属钠与硫酸铜溶液反应的化学方程式。
②通过上述探究.小明对其疑问得到的解答是什么
【考试结果】经统计分析,学生在本试题②上的得分偏低。
问题:
(1)该试题的正确答案是什么
(2)试分析学生在②上得分偏低的可能原因。
(3)如果你来讲评该试题,你将给予学生哪些学法指导答案:解析:(1)①反应方程式: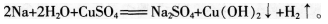 ②小明通过实验可以得出,不是所有的活动性较强的金属都可以将位于其后面的金属从它们的盐溶液中置换出来:钠是不能从硫酸铜当中置换出单质铜的,生成氢氧化铜说明是硫酸铜与碱溶液反应制得。
②小明通过实验可以得出,不是所有的活动性较强的金属都可以将位于其后面的金属从它们的盐溶液中置换出来:钠是不能从硫酸铜当中置换出单质铜的,生成氢氧化铜说明是硫酸铜与碱溶液反应制得。
(2)一方面多数学生对化学反应的反应过程和反应机理不清楚,即对概念原理知其然不知其所以然,由于钠和水极易发生反应,钠与盐的反应其实是钠先和水反应生成碱溶液,碱再与盐发生复分解反应;另一方面学生容易被已有的规律形成思维定式.当出现认知冲突的时候.对基本概念和反应规律的掌握缺乏探究精神 。
(3)针对化学一般原理和知识的教学,在教学中可以采取概念原理的教学方法.提倡学生通过活动主动建构,形成并应用概念。概念原理知识在课堂教学中的方法策略:①突出证据的作用.帮助学生形成新概念,通过钠不能置换出单质铜让学生明白不是所有的活泼金属都能从盐溶液中置换出对应的不活泼金属。⑦关注学生的原有知识,建立概念间的联系;③制造认知冲突,促进学生转变错误概念.让学生明白活泼金属置换不活泼金属是有特例的.不是所有的活动性较强的金属都可以将位于其后面的金属从它们的盐溶液中置换出来;④抽象概念形象化,减少学生的学习障碍,通过对反应过程的讲解.说明钠与盐的反应其实是钠先和水反应生成碱溶液。碱再和盐发生复分解反应,帮助学生理解实验现象:⑤优化推理过程,发展学生抽象思维能力。 -
第3题:
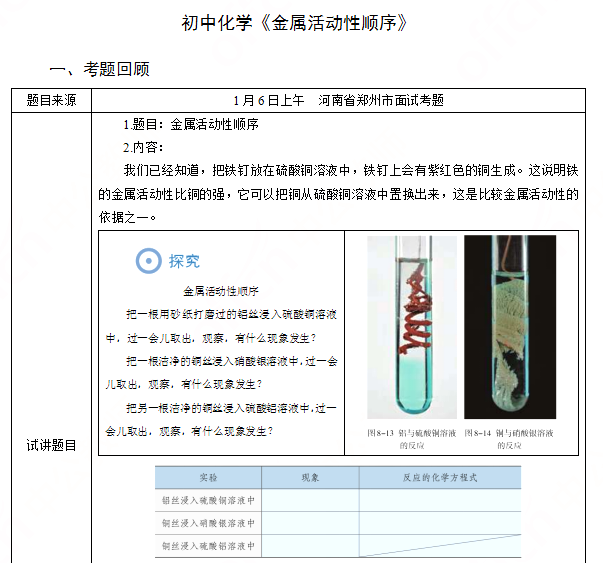


【学生回答】锌与硫酸生成氢气和硫酸锌。通过上节课的实验可以知道铜与硫酸不发生反应。
【教师引导】既然锌能与酸反应,铜不能与酸反应,由此可知金属的活泼性是不同的。那么金属的活动性强弱是怎样的顺序呢,这节课我们就一起来探究金属的活动性。
(二)新课讲授
【学生实验】①铁与硫酸铜的反应;②铁、铜分别与盐酸的反应
【提出问题】通过实验,思考铁与铜,哪种金属更加活泼?为什么?
【学生回答】铁比铜活泼,因为铁与盐酸发生了反应,有气泡产生,而铜与盐酸不反应,并且铁能把铜从硫酸铜溶液中置换出来,说明铁更活泼。
【提出问题】通过这两组实验,你能说说我们在证明金属活动性强弱时采取的实验方法吗?
【学生回答】第一种方法是让金属与另一金属的盐溶液反应,根据能否发生置换反应判断金属活泼性强弱;第二种方法是让金属与酸反应,根据能否发生反应、发生反应的剧烈程度来判断金属活泼性强弱。
【教师引导】现有镁、铜、锌三种金属,利用上述实验方法,你能设计方案并通过实验来判断镁、铜、锌三种金属谁的活动性更强吗?
(药品:镁条、铜丝、锌粒、稀盐酸、稀硫酸、氯化镁溶液、硫酸锌溶液、硫酸铜溶液。)
(小组讨论5分钟)
【提出问题】哪个小组愿意说一下自己小组的实验方案?
【学生回答】
小组①:将镁条、铜丝、锌粒分别与稀盐酸反应,观察反应的剧烈程度来判断活动性强弱。

【提出问题】根据金属活动性顺序表来看,金属所处的位置与活泼性有什么关系?排在H前面的金属有什么特点?排在前面的金属与后面金属的盐溶液能否发生反应?
【学生回答】
(1)在金属活泼性顺序里,金属的位置越靠前,它的活泼性就越强;
(2)在金属活泼性顺序里,位于氢前面的金属能置换出盐酸、稀硫酸中的氢;
(3)在金属活泼性顺序里,位于前面的金属能把位于后面的金属从其盐溶液中置换出来。
(三)巩固提高
请根据金属活动性顺序表判断下列反应能否发生?
(1)铁和稀盐酸
(2)铝和硫酸锌溶液
(3)铁与硫酸铜晶体
解析:(1)反应;(2)反应;(3)不反应
(四)小结作业
请学生回答本堂课的收获:金属活动性顺序。
布置作业:有一种“黄铜”又称为“愚人金”,实为铜、锌合金。“黄铜”外观与黄金相似,常被不法商贩用来冒充黄金牟取暴利。能不能利用所学知识,设计实验来鉴别金与“愚人金”?
【板书设计】

【答辩题目解析】
1.铝的化学性质很活泼,为什么通常铝制品却很耐腐蚀?为什么不宜用钢刷、沙等来擦洗铝制品?
2.请谈一谈你这样设计导入的原因?答案:解析:1.
铝在空气中与氧气反应,其表面生成一层致密的氧化铝薄膜,阻止铝进一步氧化,因此,铝制品具有耐腐蚀性。如果用钢刷、沙等来擦洗铝制品,很容易破坏铝制品表面致密的氧化铝薄膜。
2.
导入我采用的是通过大屏幕出示三个置换反应的反应物,让学生来判断产物。学生根据上节课做过的实验能够准确地得出结论,由此引出金属具有不同的活泼性,从而进入本节课的学习。采用这种复习的导入方法既可以检测学生对上节课置换反应内容的掌握程度,又可以降低学习新知识的难度,帮助学生克服心理上的恐惧,使学生在学习新内容时既有了思想准备,又有了知识基础,学习起来轻松自如。 -
第4题:
氯气的化学性质极为活泼,它可以把氟从其熔融化合物中置换出来。
正确答案:错误 -
第5题:
酸能跟()反应,生成盐和氢气。
- A、惰性金属
- B、活泼金属
- C、)不活泼金属
- D、过渡金属
正确答案:B -
第6题:
沸石的阳离子交换在()情况下,可在水溶液中进行。
- A、需交换的金属处于阳离子中
- B、需交换的金属为阳离子,但它的盐类不溶于水
- C、金属离子的盐溶于水,但溶液呈强酸性
- D、金属离子是阳离子,其盐溶于水且溶液不呈强酸性
正确答案:D -
第7题:
当水和碱金属反应时,生成()。
- A、酸溶液
- B、不溶性的金属氢氧化物
- C、碱溶液
- D、盐和氢气
- E、碱金属的氧化物
正确答案:C -
第8题:
一般情况下,金属单质与盐溶液反应生成()。
- A、另一种金属和水
- B、一种非金属和盐
- C、另一种金属和盐溶液
- D、一种非金属和盐溶液
正确答案:C -
第9题:
将金属Pt插入FeCl3和FeCl2溶液中所组成的电极属于()
- A、金属电极
- B、金属一金属难溶盐电极
- C、氧化还原电极
- D、气体电极
正确答案:C -
第10题:
单选题当水和碱金属反应时,生成哪种以下哪种物质()。A盐和氢气
B酸溶液
C碱溶液
D不溶性的金属氢氧化物
E碱金属的氧化物
正确答案: C解析: 碱金属可置换水中的H,生成强碱性的氢氧化物。 -
第11题:
单选题已知钡的活动性处于钾和钠之间,下列反应可以实现的是()A钡可以从氯化钾溶液中置换出钾
B钡可以从冷水中置换出氢而得到氢气
C钡可以从氯化钠溶液中置换出钠
D在溶液中钡离子可氧化金属锌
正确答案: B解析: 钡的活动性处于钾和钠之间,钾、钠均可以从冷水中置换出氢气,故也可以从冷水中置换出氢气,B项正确。 -
第12题:
判断题氯气的化学性质极为活泼,它可以把氟从其熔融化合物中置换出来。A对
B错
正确答案: 错解析: 氯气的化学性质极为活泼,但它不能把氟从其熔融化合物中置换出来,因为氟比它更活泼。 -
第13题:
X、Y、Z、M四种金属,已知X可以从Y的盐溶液中置换出Y:X和Z组成原电池时,Z为正极;Y和Z两种离子在同一溶液中被电解时.阴极只能得到Y单质:M离子的氧化性强于Y离子。则这四种金属的活动性由强到弱的顺序是:( )。A、X>Z>Y>M
B、X>Y>Z>M
C、M>Z>X>Y
D、X>Z>M>Y答案:A解析:金属活动性强的单质可以置换出金属活动性较弱的单质,X可以从Y的盐溶液中置换出Y,说明金属活动性X>Y;原电池中,负极金属的活动性较强,X和Z组成原电池时,Z为正极,说明金属活动性X>Z;电解池中。阴极是得电子被还原的一极,氧化性强的最先放电,Y和Z两种离子在同一溶液中被电解时.阴极只能得到Y单质,说明金属活动性Z>Y;M离子的氧化性强于Y离子,说明金属活动性Y>M。这四种金属的活动性顺序为X>Z>Y>M,本题选A。 -
第14题:
金属活动性是反映金属在水溶液里形成水合离子倾向大小的标志,判断金属活动性大小的依据是( )。A.标准电极电势
B.电离能
C.升华能
D.水合能答案:A解析:金属的活动性是反映金属在水溶液里形成水合离子倾向的大小,也就是反映金属在水溶液里起氧化反应的难易,它是以金属的标准电极电位为依据的。从能量角度来看,金属的标准电极电位除了与金属元素原子的电离能有关外,同时还与金属的升华能、水合能等多种因素有关。
标准电极电势:可逆电极在标准状态及平衡态时的电势,也就是标准态时的电极电势。
电离能:基态的气态原子或气态离子失去一个电子所需要的最小能量称为元素的第一电离能。
升华能:固态单质变为气态原子时所需的能量。
水合能:金属阳离子与水化合时所放出的能量。 -
第15题:
所谓盐垢是指从溶液中直接析出并附着金属表面的沉积物。
正确答案:错误 -
第16题:
为探究Zn和Cu的金属活动性强弱,提供的试剂有:Zn、Cu、H2SO4溶液、ZnSO4溶液、CuSO4溶液。下列说法正确的是()
- A、选用两种试剂可实现实验目的
- B、ZnSO4溶液中加人Cu不能探究金属活动性强弱
- C、最多只能设计一种实验方案
- D、根据Zn和Cu的硬度能判断金属活动性强弱
正确答案:A -
第17题:
金属—金属难溶盐的电极电位随溶液中( )离子活度的变化而变化。
- A、难溶盐阴
- B、金属
- C、待测
- D、共存
正确答案:A -
第18题:
在金属活动顺序表中,排在氢()的金属,能从()中置换出氢。
正确答案:前面;酸 -
第19题:
下面金属排列顺序,前者能把后者从某溶液里置换出来是()
- A、Zn、Al、Mg
- B、Fe、Zn、Al
- C、Ag、Cu、Hg
- D、Zn、Cu、Hg
正确答案:D -
第20题:
将一金属片放入盐溶液中时,由于金属的活动性,金属有失去()并成为离子进入溶液的一种倾向。
- A、电子
- B、原子
- C、分子
- D、离子
正确答案:A -
第21题:
填空题在金属活动顺序表中,排在氢()的金属,能从()中置换出氢。正确答案: 前面,酸解析: 暂无解析 -
第22题:
单选题将一金属片放入盐溶液中时,由于金属的活动性,金属有失去()并成为离子进入溶液的一种倾向。A电子
B原子
C分子
D离子
正确答案: A解析: 暂无解析 -
第23题:
单选题当水和碱金属反应时,生成()。A酸溶液
B不溶性的金属氢氧化物
C碱溶液
D盐和氢气
E碱金属的氧化物
正确答案: A解析: 暂无解析
