莫尔法适用的溶液PH范围是多少?为什么?
题目
莫尔法适用的溶液PH范围是多少?为什么?
相似考题
更多“莫尔法适用的溶液PH范围是多少?为什么?”相关问题
-
第1题:
为什么缓冲溶液能稳定溶液的pH值?
正确答案:
-
第2题:
莫尔法适用的pH范围一般为6.5~10.5,若酸度过高,则( )。
A. AgCl沉淀不完全
B. Ag2CrO4沉淀滞后形成
C. 终点提前出现
D. AgCl沉淀吸附Cl-增多答案:B解析:由: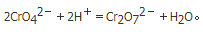
当pH值偏低呈酸性时,平衡向右移动,[CrO42-]减少,Ag2CrO4沉淀滞后形成,导致终点拖后而引起滴定误差较大(正误差)。当pH值增大呈碱性时,Ag+将生成Ag2O沉淀。如有NH4+存在,需控制pH=6.5~7.2,因碱性条件下NH+转化为NH3,Ag+与NH3反应形成配离子。 -
第3题:
一般玻璃电极PH值适用范围是多少?
一般玻璃电极适用于PH值1—9范围内。
略 -
第4题:
莫尔法只能在酸性溶液中进行。
正确答案:错误 -
第5题:
莫尔法滴定要求PH值的范围是()。
正确答案:6.5~10.5 -
第6题:
为什么在使用莫尔法测定氯离子时要控制pH值?
正确答案: ①莫尔法测定CL-必须在pH值为6.5—10.5的溶液中进行,最好pH值控制在6.5-7.2范围内
②若酸度过大,CrO42-与H+形成HCrO4-、H2Cr04,不能形成红色的Ag2CrO*4沉淀,不能指示终点;
③若碱度太强,Ag+会水解成AgOH,甚至形成A2O沉淀。如果水样中含有NH4+,在强碱性下转变为NH3,它能和Ag+形成[Ag(NH3)]+、[Ag(NH3)2]+等络离子,也使测定产生较大的正误差。 -
第7题:
莫尔法要求溶液的PH值为()。
正确答案:6.5-10.5 -
第8题:
应用莫尔法时,溶液的pH值应控制在()。
- A、3.5~6.5
- B、6.5~10.5
- C、8~11
- D、10.5~12
正确答案:B -
第9题:
直接电位法的依据是什么?为什么用此法测定溶液pH时,必须使用标准pH缓冲溶液?
正确答案: 直接电位法是通过测量电池电动势来确定待测离子活度的。该法是建立在pHX=pHS+2.303(EX-ES)RT/F基础上的,即pH的测定是以标准缓冲溶液的pH为基准,通过比较待测溶液和标准溶液之间的电势差得出的,因此此法测定pH值时,必须使用标准pH缓冲溶液。 -
第10题:
向1L1mol/L的处于等电点的甘氨酸溶液加入0.3molHCl,问所得溶液的pH是多少,如果加入0.3mol NaOH以代替HCl时,pH将是多少?
正确答案: 解:
P.H1=pKa1+lg(7/3)=2.71
P.H2=pKa2+lg(3/7)=9.23 -
第11题:
问答题为什么在使用莫尔法测定氯离子时要控制pH值?正确答案: ①莫尔法测定CL-必须在pH值为6.5—10.5的溶液中进行,最好pH值控制在6.5-7.2范围内
②若酸度过大,CrO42-与H+形成HCrO4-、H2Cr04,不能形成红色的Ag2CrO*4沉淀,不能指示终点;
③若碱度太强,Ag+会水解成AgOH,甚至形成A2O沉淀。如果水样中含有NH4+,在强碱性下转变为NH3,它能和Ag+形成[Ag(NH3)]+、[Ag(NH3)2]+等络离子,也使测定产生较大的正误差。解析: 暂无解析 -
第12题:
填空题以莫尔法硝酸银为标准溶液滴定Cl—,若溶液中的PH=4,则分析结果将()正确答案: 偏高解析: 暂无解析 -
第13题:
莫尔法使用的pH值范围一般为6.5~10.5,若酸度过高,则( )。A.AgCl沉淀不完全
B.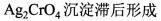
C.终点提前出线
D.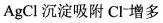 答案:B解析:
答案:B解析: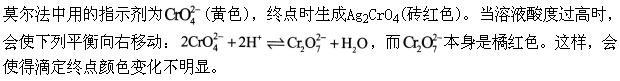
-
第14题:
莫尔法适用的pH范围一般为6.5~10.5,但应用于NH4Cl中氯含量时,其适用的pH为6.5~7.2,这主要是由于碱性稍强时,( )。
A. 易形成Ag2O沉淀
B. 易形成AgCl沉淀
C. 易形成Ag(NH3)2+配离子
D. Ag2CrO4沉淀提早形成答案:C解析:莫尔法适用的pH范围一般为6.5~10.5,但应用于NH4Cl中氯含量时由于有NH4+存在,需控制pH=6.5~7.2,因碱性条件下NH4+转化为NH3,Ag+与NH3反应形成配离子:Ag++2NH3=Ag(NH3)2+。 -
第15题:
沉淀滴定中的莫尔法可用于Cl-的测定,介质的pH控制在()范围为宜,若酸度过高,则测定结果()。
正确答案:6.5-10.5;偏大 -
第16题:
莫尔法为什么不能用氯离子滴定银离子?
正确答案:莫尔法是用硝酸银作滴定剂、铬酸钾作指指示剂,终点时略过量的硝酸银与铬酸钾生成砖红色指示终点。如用氯离子滴定硝酸银,加入铬酸钾就会生成铬酸银沉淀,就不能指示终点了。 -
第17题:
在应用莫尔法时,一般地应控制溶液的pH值在6.5-10.5范围内。
正确答案:正确 -
第18题:
莫尔法测定Cl-时,为什么要在中性或弱碱性溶液中进行?
正确答案:因为以H2CrO4为二元弱酸、酸性较弱,因此Ag2CrO4易溶于酸Ag2CrO4+H+=2Ag++HCrO4-故滴定不能在酸性溶液中进行。另外,酸性溶液中,CrO42-发生下面的反应:2CrO42-+2H+=2HCrO4-=H2O+Cr2O72-,故而在酸性溶液中,很难生成Ag2CrO4沉淀。
但如果溶液碱性太强,将使AgNO3沉淀为AgOH并逐步为褐色的Ag2O,影响终点观察,2Ag++2OH-=2AgOH→Ag2O+H2O
故而莫尔法测定Cl-时,只能在中性或弱碱性溶液中进行。 -
第19题:
为什么莫尔法只能在中性或弱碱性(PH=6.5~10.5)溶液中进行?
正确答案:因为Ag2CrO4易溶于酸,在酸性溶液中不能生成Ag2CrO4沉淀,滴定没有终点;在强碱性溶液中,Ag+会发生水解,生成黑色的Ag2O沉淀。 -
第20题:
清净塔次氯酸钠有效氯及PH值控制范围是多少?为什么?
正确答案:补充次氯酸钠有效氯一般在0.085±0.12%,PH值在7左右。清净塔内次氯酸钠有效氯在0.06%以上为宜.实验证明,当次氯酸钠溶液有效氯在0.05%以下和PH值在8以上时,清净效果明显下降.而当有效氯在0.15%以上时,容易生成氯乙炔有发生爆炸的危险,故从安全和清净效果以及分析有效氯的可能误差来考虑上述最佳控制范围为宜. -
第21题:
简述莫尔法和佛尔哈德法的适用范围和滴定方式。
正确答案: 莫尔法适用于测氧化物和溴化物,不能用于测磺化物和硫氰化物,只能用AgNO3做滴定剂,不能返滴定。佛尔哈德法用于返滴定法。 -
第22题:
用莫尔法测Cl-时的适宜pH范围是(),滴定剂是(),指示剂是()。
正确答案: 6.5-10.5;AgNO3;铬酸钾 -
第23题:
填空题沉淀滴定中的莫尔法可用于Cl-的测定,介质的pH控制在()范围为宜,若酸度过高,则测定结果()。正确答案: 6.5-10.5,偏大解析: 暂无解析
