氯气杀菌主要是氯气与水反应生成()。A、次氯酸B、Cl2C、Cl-D、HCl
题目
氯气杀菌主要是氯气与水反应生成()。
- A、次氯酸
- B、Cl2
- C、Cl-
- D、HCl
相似考题
更多“氯气杀菌主要是氯气与水反应生成()。A、次氯酸B、Cl2C、Cl-D、HCl”相关问题
-
第1题:
阅读下列材料,按要求完成教学设计任务。
材料一《普通高中化学课程标准(实验)》内容标准为:“通过实验了解氯、氮、硫、硅等非金属及其重要化合物的主要性质,认识其在生产中的应用和对生态环境的影响”。活动与探究建议:“实验氯气的漂白性”。
材料二某高中化学教科书《化学1》“氯气与水的反应”的教学片段。
目前,很多自来水厂用氯气来杀菌、消毒,我们偶尔闻到的自来水散发出的刺激性气味就是余氯的气味。
氯气溶于水为什么能杀菌消毒呢在25 0C时.1体积的水可溶解约2体积的氯气.氯气的水溶液称为氨水。在常温下,溶于水中的部分Cl2与水发生如下反应: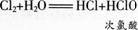
次氯酸(HClO)具有强氧化性,因此,次氯酸能杀死水中的病菌,起到消毒的作用。氯水也因为含有次氯酸而具有漂白作用。
次氯酸是很弱的酸,不稳定,只存在于水溶液中,在光照下易分解放出氧气:
近年来有科学家提出,使用氯气对自来水消毒时,氯气会与水中的有机物发生反应,生成的有机氯化物可能对人体有害。因此,人们已开始研究并试用新的自来水消毒剂。如二氧化氯(C102)、臭氧等。

最初,人们直接用氯气作漂白剂,但因氯气的溶解度不大,而且生成的HCl0不稳定,难以保存,使用起来很不方便,效果也不理想,在C12与水反应原理的基础上,经过多年的实验、改进,才有了今天常用的漂白液和漂白粉。
材料三教学对象为高中一年级学生,他们已经学过了实验的基本方法,物质的量,氧化还原反应.金属及其化合物的相关知识。
要求:
结合上述材料,完成“氯气与水的反应”片段的教学设计,包括教学目标,教学重、难点,教学过程,板书设计(不少于300字)。答案:解析:(1)教学目标 【知识与技能目标】了解氯气与水反应的实质及产物;知道氯水的成分;认识次氯酸的性质和应用。
【过程与方法目标】通过观察、比较化学现象和反应,学会善于从实验中发现问题、分析问题、解决问题的方法。
【情感态度与价值观目标】通过实验激发学习化学的兴趣,树立将化学知识应用于生活、生产的意识。
(2)教学重、难点
【重点】氯气和水的反应、氯水的漂白性。
【难点】氯水的成分和漂白性。
(3)教学过程
环节一:导入新课
创设情景:有时候我们打开水龙头会闻到一股刺激性的气味,这种刺激性的气味来源于氯气,目前有很多自来水都采用氯气来杀菌、消毒,你知道这是为什么吗
导入:今天我们就来探索氯气和水的作用。
环节二:探究新知
对比启迪:我们知道二氧化碳能溶于水,与水反应生成碳酸,氯气能不能溶于水实验表明l体积的水大约溶解2体积的氯气.氯气的水溶液称之为氯水。氯气可以和水反应吗请同学们提出假设或猜想。
提问:如何证明氯气和水发生了反应请大家进行讨论。
【实验探究1】方案l:检验溶液的酸碱性,用玻璃棒蘸取少量的氯水点到紫色石蕊试纸上;方案2:检验氯离子,用胶头滴管吸取少量硝酸银置于小试管中,再用胶头滴管吸取少量氯水滴加到硝酸银溶液里。
请学生进行实验探究1并观察实验现象、得出结论。
设疑:在实验探究l中观察到湿润的蓝色石蕊试纸周围是红色的,它的中间部分是白色的,这意味着氯水中含有漂白性的物质。那氯水中具有漂白性的物质是什么首先我们要知道氯水中都存在哪些离子和分子。请大家根据已有知识进行讨论、推测。
这里我们考虑HCIO(次氯酸)和Cl---2到底是谁具有漂白性呢请学生思考讨论实验方案。
请学生进行实验探究并观察实验现象、得出结论。
【实验探究2】将氯气分别通入盛有干燥的红布条和湿润的红布条的广l:3瓶中,盖上玻璃片。
归纳:干燥的氯气无漂白性.潮湿的氯气有漂白性,所以可得具有漂白性的物质是HClO。
环节三:巩固练习
1.以下物质中,含有氯分子的是()。
A.液氯
B.氯水
C.盐酸
D.食盐
2.能使干燥有色布条褪色的物质是()。
A.氯气
B.氯化氢
C.氯水
D.液氯
环节四:小结作业
小结:这节课我们学习了哪些知识,请同学说一说。学生总结:氯气与水的反应原理,次氯酸的化学性质及应用。
作业:思考如何证明次氯酸的酸性比碳酸弱调研生活生产中还有哪些物质可以作为漂白剂,它们有什么区别
四、板书设计
-
第2题:
氯的消毒原理是因为氯气在水中与水反应生成()的缘故。
正确答案:次氯酸 -
第3题:
氯气理化特性错误的是()
- A、常温常压下为无色
- B、微溶于水,生成次氯酸和盐酸
- C、有刺激性气味的气体
正确答案:A -
第4题:
通往氯气精炼时,起精炼作用的是氯气与AL及H反应生成的气体。
正确答案:正确 -
第5题:
氯气常用于自来水消毒是因为次氯酸是强氧化剂,可以杀菌。
正确答案:正确 -
第6题:
氯气杀菌,Cl2+H2O→HCl+HOCl→HCl+[O],真正起杀菌作用的是()。
- A、HCl
- B、HOCl
- C、[O]
- D、Cl2
正确答案:C -
第7题:
氯气与碱反应生成()、次氯酸钠。
正确答案:氯化钠 -
第8题:
对氯的杀菌作用的解释是氯与水作用生成的()具有杀菌作用
- A、盐酸
- B、氯气
- C、次氯酸
- D、氯酸
正确答案:C -
第9题:
下列关于氯气的描述中,正确的是()。
- A、氯气以液态形式存在时,可称为氯水或液氯;
- B、氯气不能与非金属反应;
- C、氯气无毒;
- D、氯气有杀菌消毒作用。
正确答案:A -
第10题:
单选题对氯的杀菌作用的解释是氯与水作用生成的()具有杀菌作用A盐酸
B氯气
C次氯酸
D氯酸
正确答案: B解析: 暂无解析 -
第11题:
填空题()量是由需氯量和余氯量组成的。氯气杀菌主要是氯气与水反应生成()。正确答案: 加氯,次氯酸解析: 暂无解析 -
第12题:
单选题氯气杀菌主要是氯气与水反应生成()。A次氯酸
BCl2
CCl
DHCl
正确答案: C解析: 暂无解析 -
第13题:
下面是针对同一化学学习任务设计的三种不同教学活动。
【学习任务】认识氯气与水反应及次氯酸的漂白性。
【教学活动1】教师通过讲授告诉学生,氯气与水发生反应生成盐酸和次氯酸,次氯酸是一种有强氧化性的酸.能使部分有色物质褪色。
【教学活动2】教师进行演示实验,把氯气通入装有湿润的有色布条的试管中,让学生观察布条是否褪色:教师告诉学生,氯气与水反应生成的次氯酸使布条褪色。
【教学活动3】
①教师演示氯气使湿润的有色布条褪色的实验。
⑦教师引导学生推测氯气与水反应可能生成的物质。
③学生猜测有色布条褪色的原因.并设计实验验证猜想。
根据上述案例.回答问题:
(1)对比三个教学活动,评价各自的优缺点。(6分)
(2)根据案例.概括出化学学习任务与化学教学活动的关系(3分),并说明对教学活动设计的启示(5分)。
(3)在教学活动3中,你认为学生猜测使有色布条褪色的物质是什么?如何检验这些猜想的真伪?(6分)答案:解析:(1)【教学活动1】主要采用了讲授法进行教学,教师通过口头语言系统连贯地向学生传授知识。
优点:可以充分利用时间.使学生在短时间内获得大量的系统连贯的知识.便于教师按计划有条理地完成教学任务,充分发挥教师的主导作用。
缺点:学生在学习活动中处于消极被动的地位.不能体现出学生的主体地位:对基础不同的学生均用相同方式对待,不能照顾学生的个别差异性;学生的学习方式相对单一,形式枯燥。不利于提高学生的学习积极性。
【教学活动2】主要采用演示法进行教学,教师在课堂上通过演示化学实验进行教学,通过实际观察获得感性知识.以说明和印证所传授的知识。
优点:使学生获得生动而直观的感性知识,加深对学习对象的印象.把书本上理论知识和实际事物联系起来,形成正确而深刻的概念;有利于培养学生的观察能力:使教学内容更加丰富多彩。从而激发学生主动参与教学活动的兴趣。
缺点:演示实验后直接呈现结论的做法,把演示单纯变成教师演示,忽学生的主体地位,不能充分调动学生的主动性思维.
【教学活动3】主要采用启发探究式的教学模式,通过创设情境,引导学生积极主动地在自主、合作、探究的学习过程中努力地发现问题,提出问题,探寻解决问题的方法和途径.获得终身学习所必备的基础知识和基本技能,学会学习.并形成正确的价值观.
优点:改变了单向的师“授”生“受”的教学方式,突显了学生的主体地位.尊重和发展学生的自主性、能动性;学生设计、操作、猜想、解释,运用信息资料、运用知识解决实际问题.提高了学生的动手能力和解决问题的能力,进而培养学生的创新精神和实践能力:学生在探究中增加了与人合作交流的机会.有利于培养其合作交流的能力.
缺点:由于学生的个体差异,素质不同的学生学习效果明显不同:课堂难以预测的情况较多,教学进度难以控制.课堂秩序难以维持:对教师的能力要求较高.
(2)学习任务与教学活动的关系:教学活动是师生之间、生生之间交往互动、共同发展的过程,是为了实现学习任务而设计实施的一系列师生活动.
对教学活动设计的启示:教学活动应当在一定理论基础之上进行设计,应当结合学习任务、学生的实际情况、教学环境、教师自身的能力、教学时间和效率等因素综合考量,制订合理的教学活动,全面完成教学任务。
(3)学生猜测使有色布条褪色的物质可能是氯气.也可能是氯气与水反应生成的HClO。
①将干燥的有色布条放进装满干燥氯气的集气瓶中,观察布条有没有褪色。②将氯水滴在pH试纸上,若试纸先变红后褪色.证明使有色布条褪色的物质是HClO。 -
第14题:
氯气加入水中之后,其杀菌作用主要是靠次氯酸。
正确答案:正确 -
第15题:
氯气和()可发生化学反应,生产次氯酸和盐酸。
- A、水
- B、酸
- C、化学品
正确答案:A -
第16题:
通入氯气精炼时,起精炼作用的是氯气与Al和H反应生成的气体。
正确答案:正确 -
第17题:
在下列反应中,光照对反应几乎没有影响的是()。
- A、氯气与氢气的反应
- B、氯气与甲烷反应
- C、氧气与甲烷反应
- D、次氯酸的分解
正确答案:C -
第18题:
()量是由需氯量和余氯量组成的。氯气杀菌主要是氯气与水反应生成()。
正确答案:加氯;次氯酸 -
第19题:
对氯气钢瓶泄漏,不宜用水直接对瓶喷射,以免生成次氯酸和盐酸。
正确答案:正确 -
第20题:
当氯加入废水中时会发生水解反应,这种水解反应是指氯气与水结合生成次氯酸。
正确答案:正确 -
第21题:
填空题氯气与碱反应生成()、次氯酸钠。正确答案: 氯化钠解析: 暂无解析 -
第22题:
判断题氯气加入水中之后,其杀菌作用主要是靠次氯酸。A对
B错
正确答案: 错解析: 暂无解析 -
第23题:
判断题当氯加入废水中时会发生水解反应,这种水解反应是指氯气与水结合生成次氯酸。A对
B错
正确答案: 对解析: 暂无解析
